Поверхностное натяжение.
Молекулы, находящиеся на поверхности отличаются по силам молекулярного притяжения от молекул, находящихся внутри жидкости. Дело в том, что молекулы в объёме жидкости равномерно окружены такими же молекулами и поэтому их силовые поля скомпенсированы. Поверхностные же молекулы, взаимодействуют как с молекулами одной фазы (жидкость), так и с молекулами другой фазы (газ), в результате чего равнодействующая молекулярных сил в поверхностном слое не равна нулю и направлена внутрь той фазы, с которой взаимодействие больше.

Рис. 12.Схема действия межмолекулярных сил внутри жидкости и на ее поверхности.
Особенно велика равнодействующая, если одной из фаз является газ (собственный пар): молекулы в газе чрезвычайно удалены друг от друга, интенсивность молекулярных сил со стороны газа очень мала.
Нескомпенсированность молекулярных сил приводит к тому, что поверхностные молекулы обладают большей свободной энергией, чем молекулы внутри фаз (рис.12). Следовательно, чтобы переместить молекулы из глубины фазы на поверхность, необходимо совершить работу против равнодействующей силы, т.е. образование новой поверхности раздела фаз требует совершения работы. Величина работы, отнесенная к единице поверхности 1см2 и выраженная в эрг/см2, получила название поверхностного натяжения:
-dА =dG = s dS
где dА – затраченная работа, dG –приращивание свободной энергии при увеличении поверхности на dS; s- поверхностное натяжение, являющееся мерой нескомпенсированности межмолекулярных сил в поверхностном (межфазном) слое.
Единица поверхностного натяжения [s] = 1 Дж/м2 = 1 Н/м; в литературе можно встретить и внесистемную единицу [s] = 1 эрг/см2 = 1 дин/см.
Поверхностное натяжение определяется силами межмолекулярного взаимодействия жидкости: чем они интенсивнее, тем больше равнодействующая поверхностных сил и тем больше s. Например, между атомами ртути действуют очень интенсивные металлические связи (разновидность химических сил) – нескомпенсированность сил в поверхностном слое велика и s ртути при комнатной температуре превышает поверхностное натяжение всех известных жидкостей и равно 470×10-3 Дж/м2. Напротив, между молекулами предельных углеводородов действуют очень слабые дисперсионные силы (составляющие сил Ван-дер-Ваальса) - s таких жидкостей мала. Например, поверхностное натяжение гексана при 200С равно 18,46×10-3 Дж/м2.
Стремление системы к уменьшению свободной энергии, кроме сокращения поверхности раздела фаз реализуется снижением поверхностного натяжения вследствие процессов адсорбции, адгезии, смачивания и др.
Связь между адсорбцией веществ и поверхностным натяжением установил Гиббс:
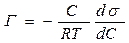 ,
,
где R - универсальная газовая постоянная, С – концентрация адсорбата, Т - абсолютная температура, ºК, 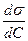 - поверхностная активность. Из этого уравнения следует важный вывод. Измерения адсорбции на твердых адсорбентах обычно производят по убыли концентрации адсорбата в растворе (DC). Поверхность адсорбента, как правило, невелика и DC составляет лишь несколько процентов от самой концентрации. Поэтому для получения достоверных значений Г необходимо измерять концентрации с очень большой точностью. В отличие от этого, измерения адсорбции на поверхности жидкость - газ крайне просты. Они сводятся к изучению зависимости поверхностного натяжения от концентрации адсорбата, графическому дифференцированию кривой s = f(C) и расчету Г по уравнению Гиббса.
- поверхностная активность. Из этого уравнения следует важный вывод. Измерения адсорбции на твердых адсорбентах обычно производят по убыли концентрации адсорбата в растворе (DC). Поверхность адсорбента, как правило, невелика и DC составляет лишь несколько процентов от самой концентрации. Поэтому для получения достоверных значений Г необходимо измерять концентрации с очень большой точностью. В отличие от этого, измерения адсорбции на поверхности жидкость - газ крайне просты. Они сводятся к изучению зависимости поверхностного натяжения от концентрации адсорбата, графическому дифференцированию кривой s = f(C) и расчету Г по уравнению Гиббса.
Работами Ленгмюра, Харкинса, Шишковского было установлено, что все вещества по их действию на поверхностное натяжение жидкостей можно разделить на два класса: поверхностно - активные и поверхностно - инактивные.
Дата добавления: 2016-09-26; просмотров: 2450;











