Второе начало термодинамики
Энтропия изолированной системы может только возрастать, а затем, по достижении максимального значения, оставаться неизменной:
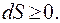 (9.19)
(9.19)
При протекании обратимого процесса энтропия возрастает: 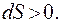 В состоянии равновесия изолированной системы энтропия максимальна,
В состоянии равновесия изолированной системы энтропия максимальна, 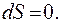 Если в системе протекает обратимый процесс, сопровождающийся сообщением системе количества теплоты
Если в системе протекает обратимый процесс, сопровождающийся сообщением системе количества теплоты  (модель 1), энтропия растёт по закону:
(модель 1), энтропия растёт по закону:
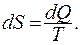 (9.20)
(9.20)
где T - температура системы в процессе передача тепла.
Если в системе протекает необратимый процесс, сопровождающийся сообщением тепла  , то энтропия растёт как за счёт необратимости процесса, так и за счёт сообщения системе тепла:
, то энтропия растёт как за счёт необратимости процесса, так и за счёт сообщения системе тепла:
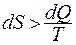
или
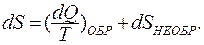 (9.21)
(9.21)
Большинство реальных процессов, происходящих в природе, являются необратимыми. Если молекулы находились сначала в одной половине сосуда, а затем равномерно распределились по некоторому объёму (необратимый процесс), то обратный процесс, когда они сосредоточатся снова в половине сосуда, мало вероятен. Пусть тело помещено в термостат (модель 2) и обменивается теплом с газом, находящимся внутри цилиндра. В результате произойдёт охлаждение тела до температуры 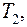 равной температуре газа и процесс прекратится. Если температура тела
равной температуре газа и процесс прекратится. Если температура тела 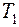 была ниже, чем температура газа, то направление протекания процесса, сопровождающееся охлаждением, запрещается вторым началом термодинамики в формулировке Р. Клаузиуса(1850 г.):
была ниже, чем температура газа, то направление протекания процесса, сопровождающееся охлаждением, запрещается вторым началом термодинамики в формулировке Р. Клаузиуса(1850 г.):
Невозможны такие процессы, единственным конечным результатом которых был бы переход тепла от тела, менее нагретого, к телу, более нагретому.
Подчеркнём, что при этом не должно происходить изменение энергии внешней среды.
Если же возможен обмен теплом с внешней средой (модели 1 и 4), то процессы с уменьшением энтропии ( 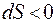 )вполне возможны. Поддержание жизни требует постоянной борьбы с ростом энтропии. Для этого используется энергия химических реакций, в которых энтропия возрастает.
)вполне возможны. Поддержание жизни требует постоянной борьбы с ростом энтропии. Для этого используется энергия химических реакций, в которых энтропия возрастает.
Если система помещена в термостат, то единственным обратимым процессом, сопровождающимся теплообменом с другими телами системы, является изотермический процесс: T2 = T1. При отсутствии теплообмена между телами обратимым будет адиабатический процесс, при котором энтропия остаётся постоянной ( 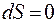 ).
).
Применяя первое начало термодинамики, запишем изменение энтропии изолированной системы: тело, нагретое до температуры 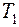 в газе с температурой
в газе с температурой 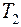 :
:
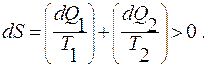 (9.22)
(9.22)
Между телом и газом происходит теплообмен, следовательно 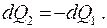 Пусть
Пусть 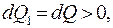 а
а 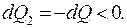 Таким образом, процесс не запрещается вторым началом термодинамики, если выполняется условие:
Таким образом, процесс не запрещается вторым началом термодинамики, если выполняется условие: 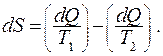 Отсюда следует
Отсюда следует 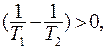 или
или 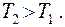 При установлении теплового равновесия
При установлении теплового равновесия 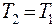 и
и 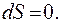
Дата добавления: 2019-09-30; просмотров: 865;











