Зависимость коэффициента диффузии от концентрации диффундирующего элемента может быть выражена уравнением
D = DO • СT / ( СT -СX ) , (6.8)
где Ст—предельная концентрация, соответствующая насыщению твердого раствора;
Сх — концентрация диффундирующего элемента;
Do — предельное значение коэффициента диффузии при уменьшении концентрации растворенного компонента до нуля.
Уравнение () показывает, что с увеличением Сх возрастает и, следовательно, на различных расстояниях от поверхности раздела значения этого коэффициента будут различны.
Влияние третьего компонента.
Наличие в твердом растворе кроме основного и диффундирующего вещества третьего компонента существенно сказывается на скорости процесса. Влияние это может быть различным. С одной стороны растворение третьего компонента, занимающего вакантные места, может затруднить диффузию; с другой — наличие инородных атомов в кристаллической решетке искажает ее и тем самым облегчает диффузию.
М. Е. Блантер установил, что при диффузии углерода в γ-железе те легирующие (третьи) элементы, которые не образуют стойких карбидов, а только искажают кристаллическую решетку растворителя, уменьшают работу разрыхления Q и ускоряют процесс диффузии. К числу этих элементов относятся, например, Ni и Со. Если легирующие элементы образуют карбиды более стойкие, чем карбид железа, то наличие их в твердом растворе в качестве третьего компонента увеличивает работу разрыхления и затрудняет диффузию. Такими элементами являются, например, Мп, Сг, Мо.
Исследование влияния легирующих элементов на коэффициент диффузии D углерода в а-железе при 700 °С показало, что некоторые из них (Ni; Со) повышают D, тогда как другие (Мп; Сг; V; Мо)— снижают (рис. 6.1). Значительно ускоряется диффузия по границам зерен металла, где структура, как правило, чрезвычайно сильно искажена. Например, в поликристаллической латуни цинк диффундирует быстрее, чем в монокристалле, причем скорость диффузии возрастает с измельчением зерна. Значения D для поликристаллической латуни со средним размером зерна 0,13 мм при 700 °С оказались в 40 раз больше, чем для монокристалла.
Атомные слои, расположенные у поверхности металла, имеют искаженную кристаллическую решетку и повышенный запас энергии, вследствие чего диффузия с поверхности всегда протекает быстрее, чем во внутренних объемах (рис. 6.2).
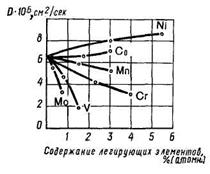
Рис.6.1 Влияние легирующих (третьих) компонентов на коэффициент диффузии D углерода в а-железе при Т = 700 "С.
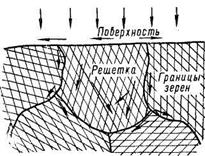
Рис. 6.2. Схема диффузии по поверхности, вдоль границ зерен и в кристаллической решетке.
Поверхностную диффузию, кроме того, ускоряет большая подвижность поверхностных слоев атомов. В качестве примера на рис. 6.3 показаны кривые температурной зависимости коэффициентов диффузии тория в вольфрам: 1 — поверхностной, 2 — по границам зерен и 3 — объемной. Максимальные значения во всех областях температур имеют коэффициенты поверхностной диффузии, несколько меньшие — коэффициенты диффузии по границам зерен; наиболее медленно протекают объемные диффузионные процессы.
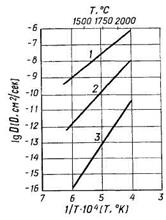
Рис. 6.3. Кривые температурной зависимости коэффициентов диффузии D тория в вольфрам.
Лекция 7. Особенности процесов диффузии в условиях сварки плавлением.
Диффузионные явления играют важную роль во многих процессах, протекающих при сварке. К числу таких процессов относится газонасыщение расплавленного металла капель и сварочной ванны; от диффузии в значительной мере зависит обмен между металлом и шлаком, т. е. раскисление, легирование металла и очищение его от вредных примесей. Диффузия вызывает перераспределение элементов в зоне сварного соединения, с диффузионными процессами связывают возникновение микронеоднородности сварных швов, наконец без учета диффузии нельзя объяснить такие важнейшие процессы, как рост зерен, перераспределение напряжений по объему тела, рекристаллизацию, ползучесть сварных соединений и т. д.
При сварке плавлением взаимодействуют между собой газообразная, жидкая и твердая фазы, вследствие чего протекание диффузионных процессов возможно по следующим схемам:
1) между газовой и жидкой фазами;
2) в жидкой фазе;
3) на границе между несмешивающимися жидкостями;
4) на границе между жидкостью и твердой фазой;
5) в твердой фазе.
Во всех перечисленных случаях условия протекания диффузии, а следовательно и активность диффузионных процессов, различны. Рассмотрим каждую из этих схем в отдельности:
1. Составляющие атмосферу дуги газы, адсорбированные поверхностью жидкого металла, диффундируют в него как в каплях, так и в сварочной ванне. В каплях наиболее благоприятны условия для диффузии газов.
Выше отмечалось влияние температуры на процессы диффузии. Так, повышение температуры с 21 до 950 °С увеличивает коэффициент диффузии азота в ос-железе на 10 порядков (с 1,1 • 10-16 до 3,1 • 10-6 см2/сгк). Очевидно при температуре капель, составляющей для железа 2300 °С, величина этого коэффициента возрастает во много раз.
В рассматриваемом случае имеем дело с поверхностной диффузией, активность которой значительно выше активности аналогичных процессов, протекающих внутри жидкого или твердого тела. Ускорению диффузии газов в капли электродного металла способствует также интенсивный отвод диффундирующего элемента в глубь металла, обусловленный активным перемещением внутренних и наружных объемов капли. Вследствие этого вблизи фазовой границы создаются высокие градиенты концентраций, в свою очередь способствующие активизации диффузии.
Диффузионные процессы между газовой средой и металлом сварочной ванны идут менее активно, чем в каплях, что связано с более низкой температурой металла ванны и меньшей относительной поверхностью реакции.
Таким образом, максимальное газонасыщение металла при сварке плавлением обычно наблюдается в каплях, тогда как в сварочной ванне избыточная часть газов стремится выделиться из металла.
В некоторых случаях имеет значение диффузия газов в твердый металл. Так, при сварке титана водород и азот окружающей среды могут активно диффундировать в глубь твердого металла на участках, нагретых до высокой температуры, и резко снижать качество сварных соединений. Чтобы избежать этого, приходится защищать не только расплавленный металл, но и всю зону нагрева от контакта с окружающей атмосферой.
2. Процессы диффузии элементов в расплавленных металлах изучены пока не достаточно.
Коэффициенты диффузии элементов в жидкий металл близки между собой, тогда как по отношению к твердым металлам они отличаются друг от друга на несколько порядков. Для диффузии углерода в жидкую сталь при температуре 1550 °С ориентировочно можно принимать D = 5 • 10 -5 см2/сек. Близкие значения получены и для диффузии Mn, Ni и S.
3. Примером двух несмешивающихся жидкостей в условиях сварки могут служить расплавленные металл и шлак. На границе между ними постоянно осуществляется диффузионный обмен элементами, т.е. переход элементов из металла в шлак или наоборот. Если такой обмен протекает достаточно длительное время, элемент распределяется между жидкостями по закону Нернста.
Следует иметь в виду, что константа распределения элемента в зависимости от температуры жидкостей принимает различные значения, поскольку растворимость элемента в этих различных жидкостях при повышении или понижении температуры может изменяться неодинаково.
Диффузия между жидким металлом и шлаком протекает активнее в каплях и несколько менее активно в сварочной ванне, особенно в низкотемпературной ее части. Причиной этого является высокая температура и большая относительная поверхность реакции у капель.
4. Диффузионные процессы на границе между твердым и жидким телом обладают той особенностью, что скорость их определяется интенсивностью диффузии в твердом теле, так как она обычно во много раз меньше скорости диффузии в жидкости.
Скорость диффузии на границе раздела жидкой и твердой фаз зависит от разности концентрации диффундирующего элемента в них, но определяется не только этим фактором. Даже если контактируют твердая и жидкая фазы одного химического состава, диффузия вполне возможна, если растворимость какого-либо элемента в твердой и жидкой фазах различна. Предположим, что мы имеем образец, изготовленный из сплава с концентрацией Со исследуемого элемента. Допустим, что этот элемент обладает большей растворимостью в жидком расплаве, чем в твердом растворе, как обычно и бывает на практике. Расплавим часть исследуемого образца и рассмотрим процессы на границе раздела твердого и жидкого тела.
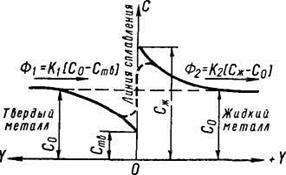
Рис. 7.1. Схема диффузионных процессов вблизи границы твердого и жидкого металла, имеющего одинаковый средний химический состав.
Поскольку исследуемый элемент лучше растворим в жидкой фазе, он начнет переходить из поверхностных слоев твердой фазы в жидкую, причем твердая фаза будет обедняться им, а жидкая обогащаться до тех пор, пока на границе не установятся равновесные соотношения концентраций. В связи с тем, что вблизи линии сплавления твердая фаза обеднена элементом, в глубинных слоях металла возникнет направленный к поверхности раздела диффузионный поток элемента Ф1 (рис. 7.1). Одновременно от жидкого слоя, имеющего повышенную концентрацию элемента, в глубь жидкой фазы будет идти противоположный диффузионный поток Ф2. При достаточно быстром охлаждении образца неравномерное распределение элемента, показанное на рис. 7.1, может быть зафиксировано и установлено спектральным локальным анализом. Приведенные соображения указывают на возможность большой химической неоднородности металла вблизи границы сплавления. Однако последующая диффузия в затвердевшем охлаждающемся металле значительно выравнивает концентрацию элемента, что изображено на рис. 7.1 штриховой линией.
Таким образом, в результате описанных процессов вблизи границы раздела твердого и жидкого металла образуются тонкие слои металла, обогащенного и обедненного диффундирующими элементами. На рис. 7.2 показана неоднородность распределения серы вблизи линии сплавления: белая полоса соответствует зоне

Рис. 7.2. Неоднородность распределения серы вблизи линии сплавления
основного металла, обедненного серой, темная полоса со стороны шва — зоне с повышенным содержанием серы. В условиях сварки, когда время контакта твердой и жидкой фаз сравнительно мало, результаты диффузии наблюдаются в малых объемах, прилегающих к поверхности раздела фаз.
5. В твердом металле диффузия протекает довольно медленно. Тем не менее при сварке она может существенно влиять на его структуру и свойства. В этом случае основные причины диффузии такие:
αрастворителя;
2) неравномерный нагрев и связанная с температурой различная растворимость элемента в разных объемах металла;
3) выпадение из твердого раствора химических соединений, приводящее к обеднению его и появлению диффузионных процессов выравнивания;
4) наличие неоднородности концентрации металла к моменту его затвердевания.
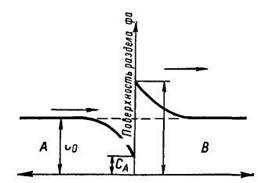
Рис 7.3. Схема диффузионных процессов вблизи поверхности раздела фаз в твердом металле.
Если считать, что фазовые превращения из В в А в твердом металле протекают при некоторой определенной температуре Тф, то изотермическая поверхность, соответствующая этой температуре, будет служить поверхностью раздела фаз (например, γ -Fe и α -Fe). В связи с тем что растворимость элемента в фазах А и В вобщем случае может быть различной, возникает диффузионный поток (левая стрелка) элемента от фазы А с меньшей растворимостью к фазе В с большей растворимостью (рис. 7.3). Изотермическая поверхность Тф, а следовательно и поверхность раздела фаз, перемещается при сварке (правая стрелка) вместе с источником тепла, поэтому результат диффузионных процессов заметен только тогда, когда скорость диффузии соизмерима со скоростью сварки. Расчеты и эксперименты показывают, что отмеченный эффект может наблюдаться только для водорода, диффузионная способность которого в 10— 100 раз больше, чем способность других элементов.
Растворимость элементов в металле сильно зависит от его температуры. В условиях неравномерного нагрева при сварке градиенты температур очень высоки, вследствие чего в непосредственной близости друг от друга оказываются объемы металла с различной растворимостью диффундирующих элементов. Возникновение диффузионных потоков атомов между этими объемами вообще возможно. Однако в результате перемещения температурного поля со скоростью сварки и кратковременности термодиффузионных процессов они успевают проявиться лишь в очень малых объемах.
Причиной неоднородности концентрации и возникновения диффузионных потоков выравнивания может служить и выпадение из раствора химических соединений. В этом случае концентрация выпавших элементов в металле-растворителе резко снижается и возникают диффузионные потоки выравнивания. Диффундирующие элементы могут и далее образовывать химические соединения, вследствие чего будет наблюдаться обеднение этими элементами начальной структуры на границе раздела зон. Если, например, в наплавленном металле шва много сильных карбидообразователей, а в основном металле их мало, то выпадение карбидов в наплавленном металле вызовет диффузию углерода в шов из основного металла. Конечным результатом этих процессов будет образование обезуглероженной прослойки в основном металле и цепочки («гряды») карбидов в шве вблизи поверхности сплавления.
Возможны и другие причины неравномерного распределения элементов в металле шва. Например, избирательность кристаллизации вызывает неоднородность состава внутренних слоев дендритов, периодичность процесса кристаллизации — химическую неоднородность слоев и т. д.
Есть основания полагать, что к моменту окончания кристаллизации металл шва неоднороден по своему химическому составу как в микро-, так и в макрообъемах. Вместе с тем исследования металла сварных соединений показывают, что в подавляющем большинстве случаев эта неоднородность совсем не так велика, как можно было ожидать. Основной причиной значительного выравнивания концентраций элементов в сварных соединениях является диффузия этих элементов в процессе охлаждения металла после сварки. Отмечено, что полнее выравниваются концентрации тех элементов, у которых более высокий коэффициент диффузии. Например, в сварных соединениях из малоуглеродистой стали углерод обычно распределяется равномерно по сечению шва, тогда как сера, имеющая при Т = 950 °С коэффициент диффузии, в 500 раз меньший, чем у углерода, распределяется в металле шва неравномерно.
Дата добавления: 2016-10-26; просмотров: 4042;











