Диффузионная и кинетическая области протекания реакций.
Гетерогенная химическая реакция может протекать только в том случае, если происходит непрерывная молекулярная или конвективная диффузия реагирующих веществ к поверхности, на которой идет данная реакция, и непрерывная обратная диффузия продуктов реакции.
Скорость процесса в целом будет определяться скоростью наиболее медленной стадии. Если скорость реакции на поверхности катализатора больше скорости диффузии, то скорость процесса в целом будет определяться скоростью диффузии. Наблюдаемая макроскопическая кинетика реакции будет подчиняться уравнениям, которые можно получить, рассматривая только процессы диффузии, и, следовательно, не будет отражать истинной скорости химической реакции на поверхности катализатора. В этом случае говорят, что процесс лежит в диффузионной области. Процесс при этом чаще всего описывается уравнением реакции первого порядка, так как скорость диффузии прямо пропорциональна концентрации.
Если скорость химической реакции значительно меньше, чем скорость диффузии, то скорость процесса в целом будет определяться скоростью химической реакции. В этом случае процесс лежит в кинетической области и описывается уравнением кинетики той реакции, которая протекает на поверхности катализатора.
Если скорость диффузии и скорость химической реакции, рассмотренные независимо друг от друга, соизмеримы, то имеется переходная область. Один и тот же процесс в зависимости от условий его проведения может лежать в различных областях. Большое влияние на характер протекания гетерогенного химического процесса оказывают давления реагирующих веществ, скорости потоков, пористость катализатора и температура.
При изменении температуры на 10 °С скорость диффузии, как показывает опыт, изменяется приблизительно в 1,2 раза, а скорость химической реакции — в 3—4 раза. Поэтому при понижении температуры скорость химической реакции убывает быстрее, чем скорость диффузии, и при низких температурах процесс чаще протекает в кинетической области.
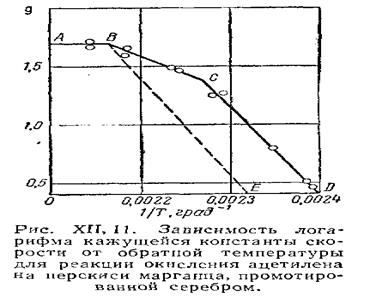
Типичная форма зависимости логарифма константы скорости гетерогенного процесса от величины обратной температуры показана на рис. XII, 11. Участок кривой АВ, отвечающий практически постоянной k (k не зависит от температуры), соответствует диффузионной области протекания процесса. Участок СD соответствует кинетической области протекания процесса. Этот участок обычно характеризуется значительной величиной энергии активации. Участок ВС соответствует переходной области. Обычно переходы из одной области в другую не так резки, как показано на рисунке, и описываются плавной кривой. Такой ход кривой наблюдается для пористых катализаторов. На кривых, характеризующих непористые поверхности, переходная область практически отсутствует. Кривая в точке В резко изменяет направление (ВЕ), характеризуя кинетическую область протекания процесса.
|
Дата добавления: 2016-10-26; просмотров: 13646;











