Уравнение первого закона термодинамики
В соответствии с формулировкой первого закона можно составить уравнение энергетического баланса термодинамической системы, достаточно лишь установить, какое направление для переноса энергии при работе и при теплообмене будет положительным. При совершении работы положительным принимают направление из термодинамической системы во внешнюю среду. В отношении теплообмена общепринято положительным считать теплообмен, направленный от внешней среды к термодинамической системе, т.е. теплоприток к системе.
Примем обозначения:
Q - теплоприток к термодинамической системе, Дж (джоуль);
U1, U2 - начальное и конечное значения внутренней энергии системы, Дж;
L – совершаемая над внешней средой работа, Дж
Теперь можно записать уравнение энергетического баланса для закрытой термодинамической системы, или, как его называют, уравнение первого закона термодинамики:
Q = U2 - U1 + L , (1-3)
т.е. теплоприток к закрытой термодинамической системе расходуется на увеличение ее внутренней энергии и на совершение работы.
Для удобства записи часто пользуются обозначением:
U2 - U1 = 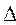 U.
U.
Тогда
Q = 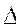 U + L.
U + L.
То же в дифференциальной форме -
dQ = dU + dL. (1-3а)
Полученные равенства выражают закон сохранения энергии в природе и поэтому абсолютно верны. На их основе будут получены большинство расчетных формул термодинамики.
Согласно СИ единицами измерения теплопритока, внутренней энергии и работы являются Дж (джоуль) и кратные ему единицы: 103Дж = кДж (килоджоуль), 106Дж = МДж (мегаджоуль). Однако применяются и другие единицы. Так, счетчики электроэнергии измеряют работу L электрического тока, подводимую к потребителю через счетчик, в киловаттчасах (1кВт.ч=3,6МДж), в диетологии энергетическая ценность продуктов указывается обычно в калориях (кал) или килокалориях (1ккал=4,19кДж). В системах теплоснабжения горячей водой и паром единицей принимают гигакалорию.
Дата добавления: 2016-10-18; просмотров: 2063;











