Отверждение солевых отходов в содалите
Льюис с соавторами из Аргоннской Национальной Лаборатории предложили способ иммобилизации солевых отходов в цеолитовую матрицу без предварительного изменения их химической формы. Контакт соли с порошком цеолита приводит к захвату молекул соли в полостной структуре цеолита с последующим внедрением катиона в решетку в результате реакции ионного обмена. Преимуществом этого метода иммобилизации солевых отходов является отсутствие корродирующих газов и селективность цеолита по отношению к щелочным элементам, но реализация метода требует добавочной ступени для изготовления цеолита.
Для иммобилизации солевых отходов был предложен способ включения их в содалит, Na8[(AlO2)6(SiO2)6]Cl2, существующий в природе минерал типа полевого шпата, который прочно удерживает хлориды и иодиды щелочных металлов в полостях структуры алюминосиликатной матрицы. Синтез может быть осуществлен простым сухим методом из порошков NaAlO2 и SiO2 с добавками хлоридов лития и калия, моделирующих солевые отходы.
При температуре выше 973 К протекает реакция:
6NaAlO2 + 6SiO2 + 2(LiCl-KCl) → Na6(Li, K)2[(AlO2)6(SiO2)6]Cl2.
Организация эксперимента по иммобилизации солевых отходив пирохимической технологии приведена на рис. 3.8.15.
Исследования методом рентгеновской дифракции показали, что при стехиометрическом смешивании конечный продукт реакции состоит из содалита, NaCl, нефелина (Na, Li, K)AlSiO4, санидина (Na, Li, K)AlSi3O8 и NaAlO2. При этом санидин обнаруживается лишь при более низких температурах. Содержание содалита увеличивается при повышении времени реакции за счет снижения содержания других компонентов.
Выщелачиваемость калия и хлора из содалита, синтезированного при стехиометрическом смешивании исходных материалов, уменьшается с увеличением времени спекания при любой температуре, тогда как выщелачиваемость кремния и стронция уменьшается с увеличением времени спекания при температуре 1073 К и увеличивается с ростом времени спекания при температуре 973 К и 1173 K. Такое поведение не вполне ясно, хотя при более низких температурах оно может быть объяснено присутствием санидина.
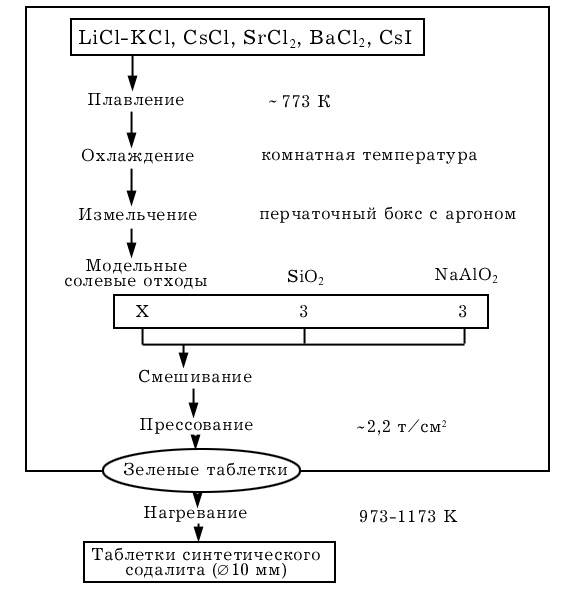
Рис. 3.8.15 Схема синтеза содалита
При нестехиометрическом смешивании (x < 1) выщелачиваемость кремния и стронция оказывается выше при всех прочих условиях, чем при стехиометрическом смешивании исходных продуктов. Для оптимальных условий синтеза содалита, x=1,0, 1073K и продолжительности реакции 200 часов, определены, представленные табл. 3.8.9, нормализованные скорости выщелачивания разных элементов и сравнены со скоростью выщелачивания этих же элементов из цеолита и боросиликатного стекла.
Как видно из таблицы, по скорости выщелачивания содалит не уступает другим матрицам для иммобилизации солевых отходов. Следует, однако, отметить, что в таблице для содалита приведены краткосрочные значения выщелачиваемости. Можно ожидать, что, будучи измеренной по прошествии большего времени, выщелачиваемость окажется меньше, так как часть элементов будет растворена на начальных этапах процесса выщелачивания.
Таблица 3.8.9
Скорости выщелачивания из разных матриц (г/м2·сутки)
| Элемент | Содалит | Цеолит | Боросиликатное стекло |
| K | 1,1·10-2 | 3,1·10-2 | 2,2·10-1 |
| Sr | 8,3·10-5 | 1,0·10-5 | не определено |
| Si | 2,1·10-4 | 4,1·10-3 | 2,3·10-1 |
| Cl | 2,0·10-2 | не определено | не присутствует |
Таким образом, можно полагать, что синтетический содалит можно рассматривать среди других перспективных матриц для иммобилизации солевых отходов пирохимической переработки ОЯТ и ВАО.
Дата добавления: 2019-05-21; просмотров: 762;











