Обмен газов в легких и их транспорт кровью
Переход О2 из альвеолярного воздуха в кровь и СО2 из крови в альвеолы происходит только путем диффузии. Никакого механизма активного транспорта газов здесь не существует. Движущей силой диффузии являются разности (градиенты) парциальных давлений (напряжений) О2 и СО2 по обе стороны альвеолярно-капиллярной мембраны или аэрогематического барьера.
Кислород и углекислый газ диффундируют только в растворенном состоянии, что обеспечивается наличием в воздухоносных путях водяных паров, слизи и сурфактантов. В ходе диффузии через аэрогематический барьер молекулы растворенного газа преодолевают большое сопротивление, обусловленное слоем сурфактанта, альвеолярным эпителием, мембранами альвеол и капилляров, эндотелием сосудов, а также плазмой крови и мембраной эритроцитов.
Диффузионная способность легких для кислорода очень велика. Это обусловлено огромным числом (сотни миллионов) альвеол и большой их газообменной поверхностью (около 100 м 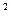 ), а также малой толщиной (около 1 мкм) альвеолярно-капиллярной мембраны. Диффузионная способность легких у человека примерно равна 25 мл О2 в 1 мин в расчете на 1 мм рт. ст. градиента парциальных давлений кислорода.
), а также малой толщиной (около 1 мкм) альвеолярно-капиллярной мембраны. Диффузионная способность легких у человека примерно равна 25 мл О2 в 1 мин в расчете на 1 мм рт. ст. градиента парциальных давлений кислорода.
Дыхательная функция крови прежде всего обеспечивается доставкой к тканям необходимого им количества О2. Кислород в крови находится в двух агрегатных состояниях: растворенный в плазме (0,3 об.%) и связанный с гемоглобином (около 20 об.%) — оксигемоглобин.
Отдавший кислород гемоглобин считают восстановленным или дезоксигемоглобином. Поскольку молекула гемоглобина содержит 4 частицы гема (железосодержащего вещества), она может связать четыре молекулы О2. Количество О2, связанного гемоглобином в 100 мл крови, носит название кислородной емкости крови и составляет около 20 мл О2. Кислородная емкость всей крови человека, содержащей примерно 750 г гемоглобина, приблизительно равна 1 л.
В различных условиях деятельности может возникать острое снижение насыщенности крови кислородом — гипоксемия. Причины гипоксемии весьма разнообразны. Она может развиваться вследствие снижения парциального давления О2 в альвеолярном воздухе (произвольная задержка дыхания, вдыхание воздуха с пониженным содержанием О2), при физических нагрузках, а также при неравномерной вентиляции различных отделов легких. СО2, образующийся в тканях, диффундирует в тканевые капилляры, откуда переносится венозной кровью в легкие, где переходит в альвеолы и удаляется с выдыхаемым воздухом. Углекислый газ в крови (как и О2) находится в двух состояниях: растворенный в плазме (около 5% всего количества) и химически связанный с другими веществами (95%). СО2 в виде химических соединений имеет три формы: угольная кислота (Н2СО2), соли угольной кислоты (NaHCО2) ив связи с гемоглобином (НвНСО2). В крови тканевых капилляров одновременно с поступлением СО2 внутрь эритроцитов и образованием в них угольной кислоты происходит отдача О2 оксигемоглобином. Восстановленный гемоглобин легко связывает водородные ионы, образующиеся при диссоциации угольной кислоты. Таким образом, восстановленный гемоглобин венозной крови способствует связыванию СО2, а оксигемоглобин, образующийся в легочных капиллярах, облегчает его отдачу. В состоянии покоя с дыханием из организма человека удаляется 230-250 мл СО2 в 1 минуту. Так дыхание участвует в регуляции кислотно-щелочного состояния во внутренней среде организма.
Обмен газов между кровью и тканями осуществляется также путем диффузии. Между кровью в капиллярах и межтканевой жидкостью существует градиент напряжения О2, который составляет 30-80 мм рт. ст., а напряжение СО2 в интерстициальной жидкости на 20-40 мм рт. ст. выше, чем в крови. Кроме того, на обмен О2 и СО2 в тканях влияют площадь обменной поверхности, количество эритроцитов в крови, скорость кровотока, коэффициенты диффузии газов в тех средах, через которые осуществляется их перенос.
Артериальная кровь отдает тканям не весь кислород. Разность между об.% О2 в притекающей к тканям артериальной крови (около 20 об.%) и оттекающей от них венозной кровью (примерно 13 об.%) называется артериовенозной разностью по кислороду (7 об.%). Эта величина служит важной характеристикой дыхательной функции крови, показывая, какое количество О2 доставляют тканям каждые 100 мл крови. Для того, чтобы установить, какая часть приносимого кровью кислорода переходит в ткани, вычисляют коэффициент утилизации (использования) кислорода. Его определяют путем деления величины артериовенозной разности на содержание О2 в артериальной крови и умножения на 100. В покое для всего организма коэффициент утилизации О2 равен примерно 30-40%. При этом в миокарде, сером веществе мозга, печени и корковом слое почек он составляет 40-60%. При тяжелых физических нагрузках коэффициент утилизации кислорода работающими скелетными мышцами и миокардом достигает 80-90%. В снабжении мышц О2 при тяжелой работе имеет определенное значение внутримышечный пигмент миоглобин, который связывает дополнительно 1,0-1,5 л О2. Связь О2 с миоглобином более прочная, чем с гемоглобином. Оксимиоглобин отдает О2 только при выраженной гипоксемии.
Регуляция дыхания
Регуляция внешнего дыхания представляет собой физиологический процесс управления легочной вентиляцией для обеспечения оптимального газового состава внутренней среды организма в постоянно меняющихся условиях его жизнедеятельности.
Основную роль в регуляции дыхания играют рефлекторные реакции. Эти реакции возникают в результате возбуждения специфических рецепторов, заложенных в легочной ткани, сосудистых рефлексогенных зонах и скелетных мышцах. Центральный аппарат регуляции дыхания представляют нервные образования спинного, продолговатого мозга и выше лежащих сегментов ЦНС.
Теория гуморальной регуляция дыхания, созданная Д. Холденом и Д. Пристли около 50 лет тому назад, в последние годы не находит экспериментального подтверждения, большинством специалистов считается ошибочной и упоминается сейчас только в историческом плане. Это обусловлено открытием специфических рецепторов (механо- и хеморецепторов), а также других рефлекторных влияний на дыхательный центр. Поэтому все изменения внешнего дыхания в настоящее время объясняются только рефлекторными механизмами.
Дыхательный ритм и управление деятельностью дыхательных мышц генерируется работой дыхательного центра, представляющего собой совокупность взаимосвязанных нейронов ретикулярной формации продолговатого мозга и вышележащих отделов ЦНС, обеспечивающих приспособление дыхания к различным условиям внешней среды.
Современные представления о работе дыхательного центра сводятся к тому, что часть дыхательных нейронов, объединенных в так называемую латеральную зону, является эфферентной частью дыхательного центра и обеспечивает преимущественно фазу вдоха (инспираторные нейроны). Другая группа нейронов, составляющая медиальную зону, является афферентной частью дыхательного центра и обеспечивает фазу выдоха (экспираторные нейроны). Предназначение этой зоны заключается в контроле периодичности дыхательной ритмики, организуемой латеральной зоной.
В регуляции дыхания на основе механизма обратных связей принимают участие несколько групп механорецепторов легких. Рецепторы растяжения легких находятся в гладких мышцах трахеи и бронхов. Адекватным раздражителем этих рецепторов является растяжение стенок воздухоносных путей. Ирритантные рецепторы расположены в эпителиальном слое верхних дыхательных путей и раздражаются при изменении объема легких, а также при пневмотораксе, коллапсе и действии на слизистую трахеи и бронхов механических или химических раздражителей. При раздражении этих рецепторов у человека возникают кашлевой рефлекс, першение и жжение, учащение дыхания и бронхоспазм. Джи - рецепторы расположены в стенках альвеол в местах их контакта с капиллярами, поэтому их еще называют юкстакапиллярные рецепторы легких. Эти рецепторы формируют частое поверхностное дыхание при патологии легких (воспаление, отек, повреждения легочной ткани), а также раздражаются при действии некоторых биологически активных веществ (никотин, гистамин и др.).
Проприорецепторы дыхательных мышц (межреберные мышцы, мышцы живота) обеспечивают усиление вентиляции легких при повышении сопротивления дыханию.
Поддержание постоянства газового состава внутренней среды организма регулируется с помощью центральных и периферических хеморецепторов. Центральные хеморецепторы расположены в структурах продолговатого мозга, и они чувствительны к изменению рН межклеточной жидкости мозга. Эти рецепторы стимулируются ионами водорода, концентрация которых зависит от рСО 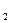 в крови. При снижении рН интерстициальной жидкости мозга (концентрация водородных ионов растет) дыхание становится более глубоким и частым. Напротив, при увеличении рН угнетается активность дыхательного центра и снижается вентиляция легких. Периферические (артериальные) хеморецепторы расположены в дуге аорты и месте деления общей сонной артерии (каротидный синус). Эти рецепторы вызывают рефлекторное увеличение легочной вентиляции в ответ на снижение рО
в крови. При снижении рН интерстициальной жидкости мозга (концентрация водородных ионов растет) дыхание становится более глубоким и частым. Напротив, при увеличении рН угнетается активность дыхательного центра и снижается вентиляция легких. Периферические (артериальные) хеморецепторы расположены в дуге аорты и месте деления общей сонной артерии (каротидный синус). Эти рецепторы вызывают рефлекторное увеличение легочной вентиляции в ответ на снижение рО 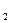 в крови (гипоксемия).
в крови (гипоксемия).
Афферентные влияния с работающих мышц осуществляются благодаря раздражению проприорецепторов, что приводит к усилению дыхания рефлекторным путем. Повышение активности дыхательного центра в этом случае является результатом распространения возбуждения по различным отделам ЦНС.
Существенное воздействие на регуляцию дыхания оказывают и условнорефлекторные влияния. В частности, эмоциональные нагрузки, предстартовые состояния, гипнотические внушения, влияния индифферентных раздражителей, сочетавшихся ранее с избытком СО 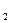 , самообучение управлению дыханием подтверждают сказанное. Легочная вентиляция зависит также от особенностей гемодинамики (уровень АД, величина МОК), температуры внешней среды и других факторов.
, самообучение управлению дыханием подтверждают сказанное. Легочная вентиляция зависит также от особенностей гемодинамики (уровень АД, величина МОК), температуры внешней среды и других факторов.
Дата добавления: 2016-09-06; просмотров: 2463;











