Перший закон термодинаміки для різних термодинамічних процесів
Розглянемо перший початок термодинаміки для ізопроцесів.
Якщо термодинамічний процес відбувається при постійній температурі T=const (ізотермічний процес) внутрішня енергія газу не змінюється. Тоді кількість теплоти, що передається газу витрачається на виконання роботи проти зовнішніх сил.
∆U =0, Q = А, 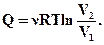 (2.47)
(2.47)
Якщо термодинамічний процес відбувається під постійним тиском P=const
(ізобарний процес)
Q = ∆U+ А.(2.48)
Цей вираз можна представити у такому вигляді:
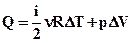 ,але
,але 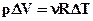 , тоді
, тоді
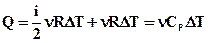
з останнього виразу слідує, що при ізобарному процесі
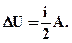
При ізобарному розширенні Q > 0 - тепло поглинається газом, і газ здійснює позитивну роботу. При ізобарному стисканні Q < 0- тепло віддається зовнішнім тілам. В цьому випадку A< 0. Температура газу при ізобарному стисканні зменшується, T2 < T1; внутрішня енергія убуває, ΔU < 0.
 Якщо термодинамічний процес відбувається при постійному об'ємі V=const (ізохорний процес), тоді:
Якщо термодинамічний процес відбувається при постійному об'ємі V=const (ізохорний процес), тоді:
А =0, Q = ∆U,(2.49)
Кількість теплоти Q, отримана газом в процесі ізотермічного розширення, перетворюється на роботу над зовнішніми тілами. При ізотермічному стисканні робота зовнішніх сил, проведена над газом, перетворюється на тепло, яке передається навколишнім тілам.
Дата добавления: 2020-10-25; просмотров: 554;











