Общие способы получения диазинов. Свойства
Для формирования пиридазинового гетероцикла используют гидразин и соответствующую четырехуглеродную молекулу, например, малеиновый ангидрид, малеиновый альдегид или малеиновую кислоту:
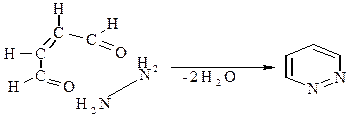
“Сборку” пиримидинового гетероцикла можно осуществлять по одной из следующих схем:
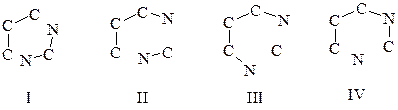
Наиболее удобным и чаще применяемым является I-й путь, предполагающий использование соединений, содержащих атомы азота в положениях 1,3 (мочевины, амидины, тиомочевина и др.), а также b-диальдегидов, b-кетоэфиров, малоновый эфир и др. В препаративном отношении этот метод также выгоден:
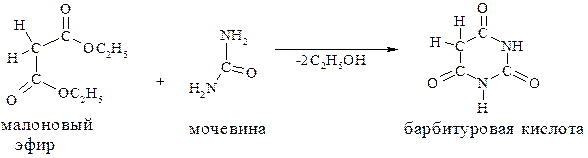
Из многочисленных путей синтеза пиразинов рассмотрим димеризацию a-ациламиносоединений, в частности конденсацию двух молекул a-аминокетона:
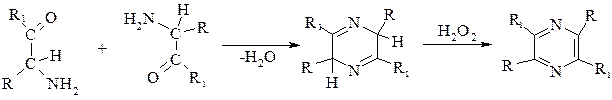
Пиридазин, пиримидин пиразин – бесцветные вещества, растворимые в воде. Оксо-, гидрокси- и аминопроизводные образуют прочные межмолекулярные водородные связи, что приводит к повышению температур плавления. Как ароматические соединения они стабилизированы благодаря циклической делокализации 6p-электронов. Значение энергий делокализации этих гетероциклов ниже, чем у бензола (153,2 кДж/моль): пиримидин – 109,2 кДж/моль; пиразин – 138,6 кДж/моль; пиридазин – 92,4 кДж/моль.
Основность. Наличие двух гетероатомов пиридинового типа обусловливает их основные свойства, которые выражены слабее, чем у пиридина. Это объясняется электроно-акцепторным влиянием второго гетероатома азота. Они образуют соли преимущественно по одному гетероатому азота, а протонирование второго гетероатома возможно только в концентрированных растворах кислот:
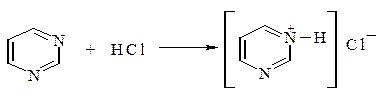
Реакции с электрофилами. Атаке электрофила в первую очередь подвергается один из гетероатомов азота: при действии сильных алкилирующих реагентов образуются соответствующие соли N-алкилония:
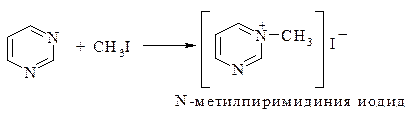
Электрофильное замещение при наличии в ядре гетероцикла активирующих групп, например, у пиримидина предпочтительно проходит по положению С-5.
Реакции нитрования, сульфирования, галогенирования и ацилирования для незамещенных диазинов до сих пор не описаны.
Взаимодействие с нуклеофилами. Реакцию аминирования удобно проводить с замещенными диазинами. В большинстве случаев нуклеофильного замещения входящая группа замещает не водород, а, как правило, имеющийся заместитель в ядре, например, галоген:
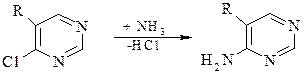
Гидрированиедиазинов протекает гораздо легче, чем пиридина. Пиримидин переходит в гексагидропиримидин, а пиразин – в пиперазин. Пиридазин гидрируется с одновременной дециклизацией и образованием 1,4-диамина:
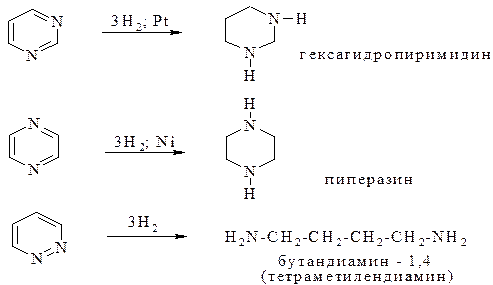
Дата добавления: 2020-10-01; просмотров: 556;











