Соединения с изолированными ядрами
Бифенил (фенилбензол, дифенил) является простейшей системой данного типа соединений:
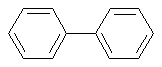
Молекула бифенила характеризуется свободным вращением ядер вокруг центральной связи; бензольные кольца копланарны. В основном состоянии молекулы бифенила между ядрами существует слабое сопряжение и каждый из них сохраняет свою индивидуальность. В принципе бифенил во многих случаях можно рассматривать как монозамещенный бензол, но с некоторыми оговорками. Так, в рассмотренных выше монозамещенных бензолах заместитель участвует в делокализации положительного заряда в σ-комплексе при SE реакции по орто- или пара-положениям.
В бифениле орто-положения атакуемого бензольного ядра в значительной степени экранированы атомами водорода в орто-положениях второго ядра, рассматриваемого в качестве заместителя. Поэтому реакция электрофильного замещения будет протекать преимущественно по пара-положениям, что представлено на схеме:
Дифенилметан. В данной молекуле оба бензольных ядра соединены метиленовой группой, поэтому они в значительной степени автономны и каждое из них ведет себя как монозамещенный бензол. В отличие от бифенила в дифенилметане бензольные ядра изолированы и между ними сопряжение отсутствует. Получить дифенилметан можно по реакции Фриделя – Крафтса из бензилхлорида и бензола:
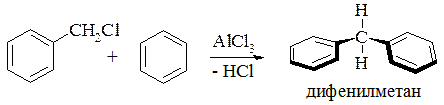
Химические свойства дифенилметана очень напоминают толуол: в SE реакциях замещение может идти по обоим ядрам с образованием ди- и тетразамещенных производных:
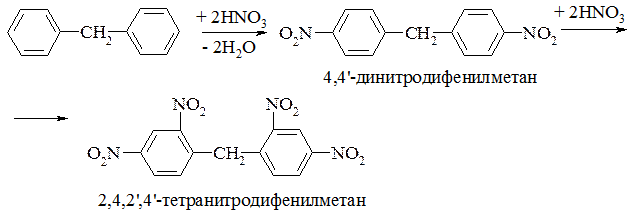
Атомы водорода метиленовой группы подвижны и могут замещаться:
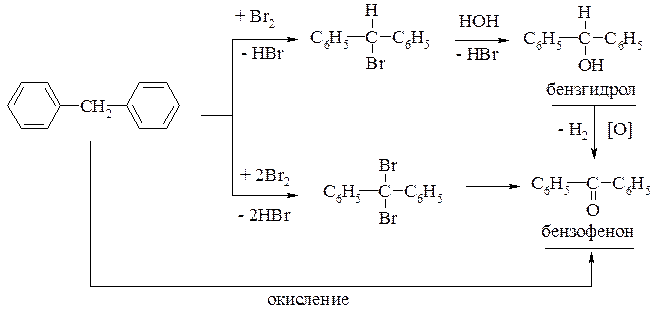
 Трифенилметан
Трифенилметан
Для получения трифенилметана используют хлороформ и бензол в условиях реакции Фриделя-Крафтса.
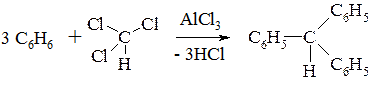
Для трифенилметана характерны SE реакции по ароматическим ядрам. Однако с точки зрения практической значимости наиболее важными являются превращения с участием центрального (метанового) углеродного атома. Это связано с образованием стабильных частиц – карбаниона, радикала и карбокатиона.
Центральный углеродный атом находится в sp3-гибридном состоянии, однако атом водорода может быть замещен, например, на атом натрия, что свидетельствует о С–Н кислотных свойствах:
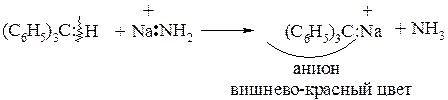
Трифенилметан, легко окисляясь, переходит в трифенилкарбинол:
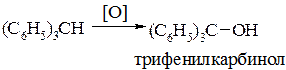
Трифенилкарбинол представляет собой третичный спирт, который в присутствии сильных минеральных кислот может образовать катион:
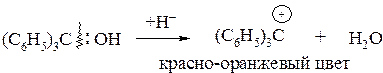
Если на трифенилхлорметан подействовать металлом (Zn, Na, Ag и т.д.), то образуется свободный радикал:
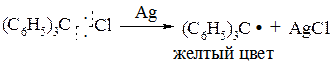
Существование стабильных частиц объясняется присутствием трех бензольных ядер.
 В тритильном карбанионе (трифенилметанид-ионе) отрицательный заряд делокализован между тремя бензольными ядрами. Сами же бензольные ядра в одной плоскости разместиться не могут из-за отталкиванивающего влияния о-атомов водорода. Эти ядра отклонены (вывернуты) от плоскости на 30 - 40°, напоминая воздушный винт самолета.
В тритильном карбанионе (трифенилметанид-ионе) отрицательный заряд делокализован между тремя бензольными ядрами. Сами же бензольные ядра в одной плоскости разместиться не могут из-за отталкиванивающего влияния о-атомов водорода. Эти ядра отклонены (вывернуты) от плоскости на 30 - 40°, напоминая воздушный винт самолета.
В тритильном карбкатионеположительный заряд на центральном атоме углерода значительно делокализован и частично компенсируется р-электронами трех бензольных ядер.
Причиной относительно высокой стабильности тритильного радикала является делокализация неспаренного электрона по π-электронной системе ароматических ядер.

Многочисленные производные трифенилметана находят широкое применение в качестве красителей. В трифенилметановых красителях, преимущественно в пара-положениях, находятся сильные ауксохромы, чаще всего – N(CH3)2 или NH2 и OH (см. также разд. 19.4.3.)
При получении таких красителей вначале образуются бесцветные лейкооснования. Последние, окисляясь, переходят в карбинольные основания, которые далее превращаются в краситель.
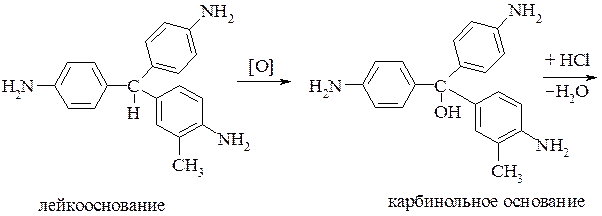
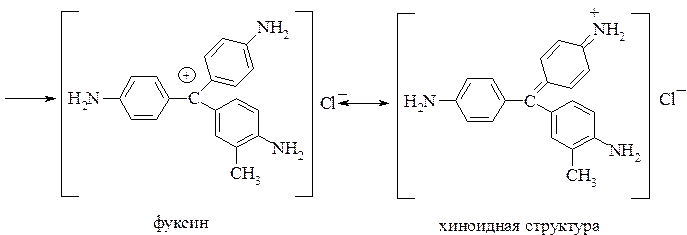
Дата добавления: 2020-10-01; просмотров: 758;











