Свойства веществ зависят от строения молекул, т.е. от того, в каком порядке атомы взаимосвязаны между собой.
Данное положение теории явилось ключом к объяснению явления изомерии: два или более вещества, характеризующиеся одинаковым качественным и количественным составом (и относительной молекулярной массой), но отличающиеся порядком взаимосвязи атомов в молекуле, т.е. строением, и, следовательно, физическими и химическими свойствами, называются изомерами.
Например, формуле С4Н10 отвечают два вещества, структуры которых можно представить:
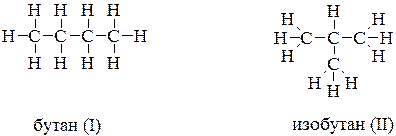
В одном случае атомы углерода образуют неразветвленную цепь (I), а во втором — разветвленную цепь (II). Вещества (I) и (II) имеют различное строение (различную последовательность взаимосвязи атомов) и поэтому их свойства тоже будут отличаться друг от друга, следовательно, они являются изомерами (бутан, изобутан).
Явление изомерии — одна из причин многообразия органических веществ.
3. Изучая продукты химического превращения вещества, можно определить его строение и выразить это конкретной структурной формулой.
При изложении последующих разделов органической химии данное положение теории будет проиллюстрировано на конкретных примерах.
4. В молекулах существует взаимное влияние атомов, как связанных, так и непосредственно между собой не связанных.
Это положение утверждает, что реакционная способность атомов (или атомных групп), входящих в состав молекулы, меняется в зависимости от того, с какими атомами они связаны в данной молекуле. Это изменение обусловлено прежде всего взаимным влиянием связанных непосредственно друг с другом атомов.
Сравнивая между собой, например,моно-, ди- и трихлор- уксусные кислоты, можно заметить, что константа диссоциации возрастает при переходе от уксусной кислоты к трихлоруксусной, причем кислотные свойства последней сопоставимы с таковыми сильных минеральных кислот.
Увеличение константы диссоциации при введении галогена в молекулу кислоты объясняется тем, что хлор как более электроотрицательный элемент оттягивает к себе электроны от соседнего углеродного атома, вследствие чего последний приобретает некоторый положительный заряд. В свою очередь, этот атом углерода притягивает электроны от соседнего атома углерода. Таким образом, сдвиг электронов в сторону хлора происходит по всей цепи атомов, и в конечном итоге атом водорода в карбоксильной группе легче отщепляется в виде иона, чем водород в карбоксильной группе уксусной кислоты. Этот сдвиг электронов усиливается по мере увеличения числа атомов галогена и поэтому трихлоруксусная кислота в данном ряду является самой сильной кислотой.
В дальнейшем положение о взаимном влиянии атомов было блестяще подтверждено и развито учеником А. М. Бутлерова, выдающимся химиком-органиком В. В. Марковниковым.
Создание теории строения сыграло важнейшую роль в развитии органической химии: из науки преимущественно аналитической она превращается в синтетическую. Теория строения создала предпосылки для объяснения и прогнозирования различных видов изомерии органических молекул, а также направлений и механизмов протекания химических реакций.
Дата добавления: 2020-10-01; просмотров: 628;











