ИММОБИЛИЗОВАННЫЕ ФЕРМЕНТЫ
Иммобилизованными ферментами называются ферменты, искусственно связанные с нерастворимым в воде носителем, но сохраняющие свои каталитические свойства. При этом нерастворимый носитель представляет собой частицу (гранулу, нить, пространственную конструкцию с развитой поверхностью) размер которой на много порядков больше размера самой крупной молекулы фермента. Такую частицу можно видеть невооруженным глазом, держать в руках, загружать в различные устройства. Таким образом ферментативный катализ из гомогенного процесса, протекающего во всем объеме реакционной среды, превращается в гетерогенный, протекающий на поверхности такого носителя.
Еще в 1916 г. Дж. Нельсон и Е. Гриффин показали, что фермент сахараза, сорбированная на угле, сохраняла свою каталитическую активность, но лишь в 1953 г. Н. Грубхофер и Д. Шлейт впервые осуществили ковалентные связывания амилазы, пепсина, РНКазы и карбоксипептидазы с нерастворимым носителем без потери активности иммобилизуемого фермента.
В 1971 г. на первой конференции по инженерной энзимологии был узаконен термин «иммобилизованные ферменты». Однако в понятие «иммобилизация» в настоящее время вкладывают более широкий смысл, чем связывание на нерастворимом носителе, а именно - полное или частичное ограничение свободы движения белковых молекул или клеток.
Иммобилизованные ферменты имеют ряд преимуществ в сравнении со свободными молекулами. Прежде всего, такие ферменты, представляя собой гетерогенные катализаторы, которые легко отделяются от реакционной среды и могут использоваться многократно без потери активности, обеспечивая таким образом непрерывность каталитического процесса при сохранении асептических условий. Кроме того, иммобилизация ведет к изменению свойств фермента: субстратной специфичности, устойчивости, зависимости активности от параметров среды. Иммобилизованные ферменты долговечны и в тысячи и десятки тысяч раз стабильнее свободных энзимов. Так, происходящая при температуре 65 °С термоинактивация лактатдегидрогеназы, иммобилизованной в 60 %-м полиакриламидном геле, замедлена в 3600 раз по сравнению с нативным ферментом. Все перечисленное обеспечивает высокую экономичность, эффектив-ность и конкурентоспособность технологий, использующих иммобилизованные ферменты.
1. Носители для иммобилизованных ферментов.Считается, что идеальные материалы, используемые для иммобилизации ферментов, должны обладать следующими основными свойствами: нерастворимостью в воде; высокой химической и биологической стойкостью; значительной гидрофильностью (смачиваемостью); достаточной проницаемостью, как для ферментов, так и для коферментов, субстратов и продуктов реакции; способностью носителя легко активироваться (переходить в реакционно-способную форму). Кроме того материал носителя должен быть нетоксичным для человека и микроорганизмов-продуцентов, а так же не влиять на физико-химические свойства реакционной среды (значение рН, концентрацию определенных ионов), которые могут повлиять на активность фермента.
Естественно, ни один из используемых в настоящее время в качестве носителя материал не отвечает полностью перечисленным требованиям. Тем не менее, существует широкий набор носителей, пригодных для иммобилизации определенных энзимов в конкретных условиях.
В зависимости от природы носители делятся на органические и неоргани-ческие материалы.
Органические полимерные носители.Иммобилизация многих ферментов осуществляется на полимерных носителях органической природы. Существующие органические полимерные носители можно разделить на два класса: природные и синтетические полимерные носители. В свою очередь, каждый из классов органических полимерных носителей подразделяется на группы в зависимости от их строения. Среди природных полимеров выделяют белковые, полисахаридные и липидные носители, а среди синтетических- полиметиленовые, полиамидные и полиэфирные.
К преимуществам природных носителей следует отнести их доступность, полифункциональность и гидрофильность, а к недостаткам - биодеградируемость и достаточно высокую стоимость.
Из полисахаридов для иммобилизации наиболее часто используют целлюлозу, декстран, агарозу (агар) и их производные. Для придания химической устойчивости линейные цепи целлюлозы и декстрана поперечно сшивают эпихлоргидрином. В полученные сетчатые структуры довольно легко вводят различные ионогенные группировки. Химической модификацией крахмала сшивающими агентами (формальдегид, глиоксаль, глутаровый альдегид) синтезирован новый носитель - губчатый крахмал, обладающий повышенной устойчивостью к гликозидазам.
Из природных аминосахаридов в качестве носителей для иммобилизации применяют хитин, который в значительных количествах накапливается в виде отходов в процессе промышленной переработки крабов и креветок. Хитин химически стоек и имеет хорошо выраженную пористую структуру.
Среди белков практическое применение в качестве носителей нашли структурные протеины, такие, как кератин, фиброин, коллаген и продукт переработки коллагена - желатина. Эти белки широко распространены в природе, поэтому доступны в значительных количествах, дешевы и имеют большое число функциональных групп для связывания фермента. Белки способны к биодеградации, что очень важно при конструировании иммобилизованных ферментов для медицинских целей. К недостаткам белков как носителей в этом случае следует отнести их высокую иммуногенность.
Синтетические полимерные носители.Благодаря разнообразию и доступности материалы этой группы широко используются как носители для иммобилизации. К ним относятся полимеры на основе стирола, акриловой кислоты, поливинилового спирта; полиамидные и полиуретановые полимеры. Большинство синтетических полимерных носителей обладают механической прочностью, а при образовании обеспечивают возможность варьирования в широких пределах величины пор, введения различных функциональных групп. Некоторые синтетические полимеры могут быть произведены в различных физических формах (трубы, волокна, гранулы). Все эти свойства полезны для разных способов иммобилизации ферментов.
Носители неорганической природы.В качестве носителей наиболее часто применяют материалы из стекла, глины, керамики, графитовой сажи, силикагеля, а также силохромы, оксиды металлов. Их можно подвергать химической модификации, для чего носители покрывают пленкой оксидов алюминия, титана, гафния, циркония или обрабатывают органическими полимерами. Основное преимущество неорганических носителей - легкость регенерации, механическая и химическая прочность. Подобно синтетическим полимерам неорганическим носителям можно придать любую форму и получать их с любой степенью пористости.
Таким образом, к настоящему времени создано огромное число разнообразных носителей для иммобилизации ферментов. Однако для каждого индивидуального фермента, используемого в конкретном технологическом процессе, необходимо подбирать оптимальные варианты, как носителя, так и условий и способов иммобилизации.
2.Методы иммобилизации ферментов.Существуют два принципиально различных метода иммобилизации ферментов: без возникновения ковалентных связей между ферментом и носителем (физические методы иммобилизации) и с образованием ковалентной связи между ними (химические методы иммобилизации). Каждый из этих методов осуществляется разными способами.
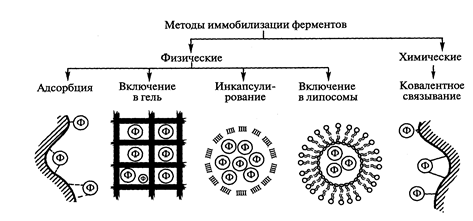
Рис.3. Методы иммобилизации ферментов (ф-молекула фермента)
Физические методы иммобилизации ферментовреализуются либо посредством адсорбции фермента на нерастворимом носителе, либо путем включения их в поры поперечносшитого геля, в полупроницаемые структуры или различные двухфазные системы.
Адсорбция ферментов на нерастворимых носителях.При адсорбционной иммобилизации белковая молекула удерживается на поверхности носителя за счет электростатических, гидрофобных, дисперсионных взаимодействий и водородных связей. Адсорбция была первым методом иммобилизации ферментов (Дж. Нель-сон, Э.Гриффин, 1916), но и сейчас не потеряла своего значения и стала наиболее широко распространенным способом получения иммобилизованных ферментов в промышленности. В литературе описано получение адсорбционным способом более 70 иммобилизованных ферментов с использованием главным образом таких носителей, как кремнезем, активированный уголь, графитовая сажа, различные глины, пористое стекло, полисахариды, синтетические полимеры, оксиды алюминия, титана и других металлов. Последние применяются наиболее часто. Эффективность адсорбции молекулы белка на носителе определяется удельной поверхностью (плотностью центров сорбции) и пористостью носителя. Процесс адсорбции ферментов на нерастворимых носителях отличается крайней простотой и достигается при контакте водного раствора фермента с носителем (статистическим способом, при перемешивании, динамическим способом с использованием колонок). С этой целью раствор фермента смешивают со свежим осадком, например, гидроксида титана, и высушивают в мягких условиях. Активность фермента при таком варианте иммобилизации сохраняется практически на 100 %, а удельная концентрация белка достигает 64 мг на 1 г носителя.
К недостаткам адсорбционного метода следует отнести невысокую прочность связывания фермента с носителем. При изменении условий иммобилизации могут происходить десорбция фермента, его потеря и загрязнение продуктов реакции. Существенно повысить прочность связывания фермента с носителем может предварительная его модификация (обработка ионами металлов, полифункциональными агентами - полимерами, белками, гидрофобными соединениями, монослоем липида и пр.). Иногда, наоборот, модификации подвергается молекула исходного фермента, однако зачастую это ведет к снижению его активности.
Иммобилизация ферментов путем включения в гель.Способ иммобилизации ферментов путем включения в трехмерную структуру полимерного геля широко распространен благодаря своей простоте и уникальности. Метод применим для иммобилизации не только индивидуальных ферментов, но и мультиэнзимных комплексов и даже интактных клеток. Иммобилизацию ферментов вгеле осуществляют двумя способами. В первом случае фермент вводят в водный раствор мономера, а затем проводят полимеризацию, в результате которой возникает пространственная структура полимерного геля с включенными в его ячейки молекулами фермента. Во втором случае фермент вносят в раствор уже готового полимера, который впоследствии переводят в гелеобразное состояние. Для первого варианта используют гели полиакриламида, поли-винилового спирта, поливинилпирролидона, силикагеля, для второго - гели крахмала, агар-агара, каррагинана, агарозы, фосфата кальция.
Иммобилизация ферментов в гелях обеспечивает равномерное распределение энзима в объеме носителя. Большинство гелевых матриц обладает высокой механической, химической, тепловой и биологической стойкостью и обеспечивает возможность многократного использования фермента, включенного в его структуру. Однако метод непригоден для иммобилизации ферментов, действующих на водонерастворимые субстраты. Многие субстраты с большим размером молекул так же могут не проникнуть в поры такого геля.
Иммобилизация ферментов в полупроницаемые структуры.Сущность этого способа иммобилизации заключается в отделении водного раствора фермента от водного раствора субстрата с помощью полупроницаемой мембраны, пропускающей низкомолекулярные молекулы субстратов и кофакторов, но задерживающей большие молекулы фермента. Разработано несколько модификаций этого метода, из которых интерес представляет микрокапсулирование и включение ферментов в липосомы.
Первый способ предложен Т.Чангом в 1964 г. и состоит в том, что водный раствор фермента включается внутрь замкнутой микрокапсулы, стенки которой образованы полупроницаемым полимером. Один из механизмов возникновения мембраны на поверхности водных микрокапсул фермента заключается вреакции межфазной поликонденсации двух соединений, одно из которых растворено в водной, а другое - в органической фазе. Примером может служить образование на поверхности раздела фаз микрокапсулы, получаемой путем поликонденсации гексаметилендиамина-1,6 (водная фаза) и галогенангидрида себациновой кислоты (органическая фаза):
-HCl
H2N-(CH2)6-NH2 + СlOС-(СН2)8-СОС1→ HN-(CH2)6-NH - СО-(СН2)8-СО-
Размер получаемых капсул составляет десятки или сотни микрометров, а толщина мембраны - сотые доли микрометра.
Достоинства метода микрокапсулирования - простота, универсальность, возможность многократного использования нативного фермента (фермент может быть отделен от непрореагировавшего субстрата и продуктов реакции процедурой простого фильтрования). Особенно существенно, что методом микрокапсулирования могут быть иммобилизованы не только индивидуальные ферменты, но и мультиэнзимные комплексы, целые клетки и отдельные фрагменты клеток. К недостаткам метода следует отнести невозможность инкапсулированных ферментов осуществлять превращения высокомолекулярных субстратов.
Близким к инкапсулированию методом иммобилизации можно считать включение водных растворов ферментов в липосомы, представляющие собой сферические или ламеллярные системы двойных липидных бислоев. Впервые данный способ был применен для иммобилизации ферментов Дж. Вайсманом и Дж. Сессом в 1970 г. Для получения липосом из растворов липида (чаще всего лецитина) упаривают органический растворитель. Оставшуюся тонкую пленку липидов диспергируют в водном растворе, содержащем фермент. В процессе диспергирования происходит самосборка бислойных липидных структур липосомы, содержащих включенный раствор фермента.
Ферменты, иммобилизованные путем включения в структуру липосом, используют преимущественно в медицинских и научных целях, ибо значительная часть ферментов в клетке локализована в составе липидного матрикса биологических мембран, поэтому изучение липосом имеет большое значение для понимания закономерностей процессов жизнедеятельности в клетке.
Другие приемы иммобилизации ферментов, основанные на физических методах, менее распространены по сравнению с рассмотренными выше.
Химические методы иммобилизации ферментов.Иммобилизация ферментов путем образования новых ковалентных связей между ферментом и носителем - наиболее массовый способ получения промышленных биокатализаторов.
В отличие от физических методов этот способ иммобилизации обеспечивает прочную и необратимую связь фермента с носителем и часто сопровождается стабилизацией молекулы энзима. Однако расположение фермента относительно носителя на расстоянии одной ковалентной связи создает стерические трудности в осуществлении каталитического процесса. Фермент отделяют от носителя с помощью специальной вставки (сшивка, спейсер), в роли которой чаще всего выступают бифункциональные и полифункциональные агенты (бромциан, гидразин, сульфурилхлорид, глутаровый диальдегид и др.). Например, для выведения галактозилтрансферазы из микроокружения носителя между ним и ферментом вставляют последовательность —СН2—NH—(СН2)5—СО—. В этом случае структура иммобилизованного фермента включает носитель, вставку и фермент, соединенные между собой ковалентными связями.
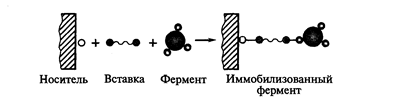
Рис.4. Схема иммобилизации фермента химическим методом
Принципиально важно, чтобы в иммобилизации фермента участвовали функциональные группы, не существенные для его каталитической функции (функциональные группы активного центра). Так, гликопротеины обычно присоединяют к носителю через углеводную, а не через белковую часть молекулы фермента. Если это условие не соблюдается, то химическая иммобилизация может привести к полной потере ферментативной активности.
Число методических приемов, разработанных для осуществления ковалентной иммобилизации ферментов, исключительно велико. Все методы химической иммобилизации классифицируют в зависимости от природы реакционной группы носителя, вступающей во взаимодействие с молекулой фермента. Ниже представлен ряд примеров, иллюстрирующих некоторые способы химической иммобилизации ферментов.
Иммобилизация ферментов на носителях, обладающих гидроксо-группами.Наиболее распространенным методом образования ковалентной связи между ферментом и полисахаридным носителем или синтетическим диольным
соединением является бромциановый метод, который был предложен Р.Аксеном,
Дж. Поратом и С.Эрнбаком в 1967 г. При обработке носителя бромцианом возникают реакционноспособные цианаты и имидокарбонаты, которые при взаимодействии с нуклеофильными аминогруппами фермента образуют производные изомочевины и уретанов:
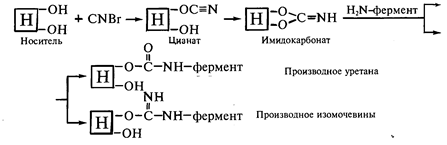
Иммобилизация ферментов носителях, обладающих аминогруппами. Первичные аминогруппы носителя, связанные с ароматическим кольцом, предварительно превращают в соли диазония, которые затем подвергают разнообразным реакциям сочетания. В реакции сочетания вступают фенольные, имидазольные, аминные, гуанидиновые, тиольные группы белков. Так, в щелочной среде фенольные радикалы тирозина образуют прочные азо-соединения, в составе которых белок связан с носителями:
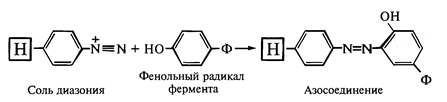
Существенно, что п-аминофенильные функции могут быть легко введены вразнообразные носители.
Иммобилизация на носителях, обладающих активированными производными карбоксильной группы.Наиболее часто для соединения аминогрупп белка с ацильными группировками носителя используют ангидриды, галогенангидриды, активированные эфиры и другие производные карбоновых кислот. Например,
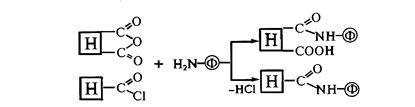
Реакционная способность производных карбоновых кислот в реакциях ацилирования аминогрупп фермента уменьшается от галогенангидридов до эфиров.
Иммобилизация на носителях, обладающих сульфгидрилъными группа-ми.Сульфгидрильные группы носителя и фермента легко окисляются с образова-нием дисульфидных связей под действием кислорода воздуха:

Дата добавления: 2020-10-01; просмотров: 877;











