Коферменты – производные пиридоксина
Ряд различных реакций катализируется ферментами, коферментами которых являются производные пиридоксина (витамина В6).
Пиридоксин имеет следующее строение:
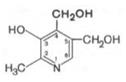
Рис. 1.4.16. Структура пиридоксина
Витамин В6 может давать различные производные, и они, а не сам витамин В6, входят в состав различных ферментов. Производными пиридоксина, играющими роль коферментов, являются пиридоксальфосфат и пиридоксаминфосфат, строение которых представлено ниже:

Рис. 1.4.17. Структура пиридоксальфосфата и пиридоксаминфосфата
Большинство ферментативных реакций, коферментами которых являются пиридоксальфосфат и пиридоксаминфосфат, связано с различными превращениями аминокислот. Однако было показано, что пиридоксальфосфат входит в состав фермента, который никакого отношения к превращениям аминокислот не имеет, а именно α-глюканфосфорилазы. Этот фермент катализирует перенос глюкозильных групп между различными полиглюкозидами (например, крахмалом или гликогеном) или неорганическим фосфатом. Роль пиридоксальфосфата в молекуле фосфорилазы заключается не в том, что он является ее коферментом, а в том, что альдегидная группа пиридоксальфосфата, связываясь с аминогруппами фермента, поддерживает третичную структуру молекулы фосфорилазы.
Одной из важных групп ферментов, у которых в качестве коферментов выступают пиридоксаль и его производные, являются аминотрансферазы, то есть ферменты, которые переносят аминогруппы от одного соединения на другое.
Реакция ферментативного переаминирования была открыта А. Е. Браунштейном с сотрудниками. Реакции переаминирования играют важную роль в обмене веществ. Наиболее важными реакциями переаминирования являются следующие три. Перваяиз них такова:
| глютаминовая кислота | щавелевоуксусная кислота | α-кето- глутарат | аспарагиновая кислота | |||
| CООH ô CH2 ô CH2 ô СН─ NН2 ô СОOН | + | CООH
ô
СН2
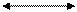 ô
С═ O
ô
СООН ô
С═ O
ô
СООН
| CООH ô CH2 ô CH2 ô С═ O ô СОOН | + | CООH ô CH2 ô СН─ NН2 ô СООН |
Вторая важная реакция переаминирования, катализируемая аминотрансферазой, это взаимодействие между глютаминовой и пировиноградной кислотами:
| глютаминовая кислота | пировиноградная кислота | α-кето- глутарат | α-аланин | |||
| CООH ô CH2 ô CH2 ô СН─ NН2 ô СОOН | + | 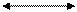 СН3
ô
С═ O
ô
СООН СН3
ô
С═ O
ô
СООН
| CООH ô CH2 ô CH2 ô С═ O ô СОOН | + | CH3 ô СН─ NН2 ô СООН |
В результате этой реакции из глютаминовой кислоты образуется α-кетоглютаровая кислота, а из пировиноградной кислоты α-аланин.
И наконец, третья реакция ферментативного переаминирования – это реакция между аспарагиновой кислотой и пировиноградной кислотой. В результате этой реакции образуется из аспарагиновой кислоты соответствующая ей кетокислота – щавелевоуксусная, а из пировиноградной кислоты – соответствующая ей аминокислота – α-аланин.
| аспарагиновая кислота | пировиноградная кислота | щавелевоуксусная кислота | α-аланин | |||
| CООH ô CH2 ô СН─ NН2 ô СОOН | + | СН3
ô
С═ O
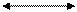 ô
СООН ô
СООН
| CООH ô СН2 ô С═ O ô СООН | + | CH3 ô СН─ NН2 ô СООН |
В последние годы, благодаря применению более чувствительных методов определения различных соединений, например метода хроматографии, удалось показать, что в живой клетке кроме трех указанных выше реакций протекают самые разнообразные реакции ферментативного переаминирования. Например, показано, что важную роль в обмене играют фосфопиридоксалевые ферменты, которые названы декарбоксилазами аминокислот. Эти ферменты катализируют отщепление от аминокислот углекислоты. Типичным представителем декарбоксилаз аминокислот является глютаматдекарбоксилаза, которая катализирует расщепление глютаминовой кислоты на СО2 и γ-аминомасляную кислоту. К числу декарбоксилаз аминокислот принадлежат также декарбоксилазы аспарагиновой кислоты или аспартатдекарбоксилазы. Под действием этих ферментов может происходить образование либо α-аланина, либо β-аланина, в зависимости от того, из какой карбоксильной группы аспарагиновой кислоты выделяется СО2.
Дата добавления: 2020-10-01; просмотров: 749;











