Детекторы для определения химического состава среды
 В настоящее время разработаны электроды для определения рН, окислительно-восстановительного потенциала (Eh), парциального давления растворенного кислорода и СО2, которые можно подвергать неоднократной стерилизации паром на месте установки. Чаще других применяют рН-электроды, отличающиеся высокой надежностью; обычно в качестве рН-электрода применяют стеклянный мембранный электрод.
В настоящее время разработаны электроды для определения рН, окислительно-восстановительного потенциала (Eh), парциального давления растворенного кислорода и СО2, которые можно подвергать неоднократной стерилизации паром на месте установки. Чаще других применяют рН-электроды, отличающиеся высокой надежностью; обычно в качестве рН-электрода применяют стеклянный мембранный электрод.
На рис. 2 изображено устройство рН-электрода, предназначенного для контроля процесса стерилизации в автоклаве. Электроды, стерилизуемые на месте установки, должны быть заключены в чехол, защищающий их от повышения давления. Окислительно-восстановительный потенциал среды можно измерять платиновым электродом в сочетании с электродом сравнения. Имеются и комбинированные зонды для определения рН и окислительно-восстановительного потенциала. Неоднократно показано, что рН влияет на кинетику биохимических превращений, поэтому необходимость измерения рН очевидна. Напротив, интерпретация результатов определения окислительно-восстановительных потенциалов и выяснение взаимосвязи между окислительно-восстановительным потенциалом и активностью клеток могут вызывать затруднения.
РИС. 2. Комбинированный электрод типа Ingold 465 для определения рН, выдерживающий стерилизацию паром в автоклаве. (С любезного разрешения Ingold Electrodes Inc.)
Одной из перспективных областей применения электродов для измерения окислительно-восстановительных потенциалов является определение низких концентраций кислорода (<1 млн-1) в анаэробных микробиологических процессах (—450 мВ<Eh<—150 мВ), когда скорость образования продукта может быть очень чувствительной к изменению Eh.
Для определения концентрации растворенного кислорода применяют гальванические (потенциометрические) или полярографические (амперометрические или электрод Кларка) зонды. По сути дела, эти электроды измеряют не концентрацию растворенного кислорода, а его парциальное давление (или активность). И в первом, и во втором зонде собственно электрод обычно отделен от среды мембраной (рис. 3), а на поверхности катода осуществляется восстановление кислорода
Катод:
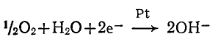 (1)
(1)
Реакция на аноде в гальваническом электроде:
Анод (гальванический электрод):
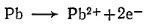 (2)
(2)
Катод и анод образуют гальванический элемент, напряжение которого зависит от количества кислорода, достигающего поверхности электрода. В кислородном электроде полярографического типа на катоде также происходит реакция (1), а на аноде осуществляется другой процесс
Анод (полярографический):
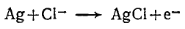 (3)
(3)
 Между катодом и анодом устанавливают постоянное напряжение и измеряют силу тока, которая зависит от притока кислорода к катоду. Недостатком как первого, так и второго электрода является дрейф сигнала (силы тока или напряжения), обусловленный накоплением гидроксильных ионов или ионов металла или истощением Cl-.
Между катодом и анодом устанавливают постоянное напряжение и измеряют силу тока, которая зависит от притока кислорода к катоду. Недостатком как первого, так и второго электрода является дрейф сигнала (силы тока или напряжения), обусловленный накоплением гидроксильных ионов или ионов металла или истощением Cl-.
РИС. 3. Устройство и основные элементы электрохимического зонда для определения парциального давления растворенного кислорода. (Воспроизведено с разрешения из работы: Wang N. S., Stephanopoulos G., Computer Application to Fermentation Processes, ORG Critical Reviews in Biotechnology, vol. 2, p. 1. © CRC Press, Inc., 1974.)
Дрейфу способствует также загрязнение наружной поверхности мембраны.
В стационарном состоянии приток кислорода к катоду зависит от ряда процессов переноса, включая перенос кислорода из жидкой фазы к наружной поверхности мембраны, диффузию через мембрану и, наконец, диффузию через раствор электролита к поверхности катода, где реакция происходит практически мгновенно. Если общая скорость переноса, а, следовательно, и концентрация кислорода вблизи катода лимитируется первой стадией, то сигнал электрода будет зависеть от свойств жидкой фазы (например, от ее вязкости) и локальных гидродинамических условий вблизи электрода. По этой причине, в частности, рекомендовалось, чтобы скорость движения жидкости вблизи полярографического электрода была не менее 0,55 м/с. Чувствительность сигнала электрода к переносу через наружный граничный слой можно снизить за счет применения менее проницаемой мембраны. Однако в этом случае увеличивается запаздывание отклика электрода на изменение парциального давления кислорода, которое в случае мембранных электродов и без того довольно велико (10—100 с). В то же время, как показано в приведенном ниже примере, такие электроды можно применять и для изучения процессов массопереноса в биореакторах в переходном состоянии, если при анализе данных учитывать диффузию через мембрану электрода.
Для определения специфических компонентов жидкой фазы разработан ряд биодетекторов (биосенсоров). Принцип действия биосенсоров заключается в определении с помощью того или иного аналитического устройства конкретного продукта реакции, катализируемой иммобилизованными ферментом или клетками. Широко изучаются также ферментные терморезисторы, в которых с помощью калориметра определяется количество теплоты, выделяющейся в процессе катализируемой ферментом реакции. В табл. 1 перечислены некоторые определявшиеся этим методом соединения и соответствующие ферменты.
Иммобилизованные ферменты можно применять и в биосенсорах других типов, например в таких, в которых продукты реакции (водород) изменяют электронную проводимость полупроводниковых устройств (кремниевых кристаллов, на которые нанесен слой SiO2 и пленка Pd).
Сферу применения биосенсоров можно существенно расширить за счет использования различных биохимических превращений, в том числе многостадийных и разветвленных реакций, в результате которых образуется детектируемое вещество. Во многих случаях с помощью иммобилизованных клеток анализируемое соединение можно превратить в более подходящее для непосредственного определения соединение. В основу разработки и применения биосенсоров с иммобилизованными клетками была положена дыхательная активность интактных иммобилизованных клеток (определение с помощью кислородного электрода), а также образование или поглощение интактными клетками электроактивных метаболитов (определение с помощью топливного электрода, рН- или СО2-электродов).
Таблица 1. Примеры применения ферментных терморезисторов в аналитической химииа

В табл. 2 приведены свойства ряда биосенсоров на основе иммобилизованных клеток; подробнее подобные аналитические устройства.
Таблица 2. Микробиологические детекторы для определения компонентов жидкой фазы

Газовый анализ
Концентрация СО2 в отходящих газах биореактора, содержащего культуру клеток, связана с дыхательной или иной ферментативной активностью клеток. Неудивительно, что этот параметр широко и успешно применяется для контроля и регулирования биореакторов. Концентрацию СО2 в отходящих газах биореактора чаще всего определяют с помощью инфракрасного спектрофотометра. Для предотвращения повреждений стекол ячейки анализируемый газ до поступления в спектрофотометр необходимо высушить. Концентрацию СО2 в потоке газа можно также определять по теплопроводности, методом газовой хроматографии или масс-спектрометрии.
Парциальное давление кислорода в газовом потоке обычно измеряют с помощью парамагнитного анализатора. Приборы этого типа также требуют предварительного высушивания и тщательного регулирования скорости газового потока; только в этом случае обеспечиваются минимальный дрейф и достаточная надежность результатов. Парамагнитные анализаторы, кроме того, очень чувствительны даже к небольшим колебаниям общего атмосферного давления, поэтому необходим одновременный контроль барометрического давления, чтобы внести, соответствующие поправки в результаты анализа на кислород. В силу дрейфа показаний парамагнитных анализаторов их применение в микробиологических процессах часто требует повторной калибровки в ходе процесса.
С помощью газовой хроматографии можно определять несколько компонентов отходящих газов: О2, СО2, СН4 (образующегося, например, в анаэробных процессах) и Н2 (выделяемого, например, культурами Hydrogenomonas). Этим методом можно также определять парциальное давление летучих компонентов газовой фазы — этанола, ацетальдегида и карбоновых кислот. Таким образом, газовая хроматография дает ценную информацию о ходе микробиологического процесса в целом, а также о концентрациях перечисленных выше веществ в жидкой фазе. Применению газовой хроматографии для контроля; процессов в нестационарном состоянии препятствует периодический характер измерений, поскольку интервал между двумя последовательными измерениями составляет примерно 15 мин.
 Для контроля состава газового потока в последнее время все чаще применяют масс-спектрометрический метод. Появление сравнительно недорогих серийных масс-спектрометров позволило расширить область применения этих приборов в исследовательских работах, а выпуск надежных, устойчивых к внешним воздействиям промышленных масс-спектрометров обусловил целесообразность их использования в промышленности. Масс-спектрометры выгодно отличаются малым временем отклика (менее 1 мин), высокой чувствительностью (предел обнаружения около 10-5 М), способностью определять несколько компонентов одновременно, линейной зависимостью отклика от концентрации в достаточно широком диапазоне и очень малым дрейфом калибровки. Ввиду высокой стоимости масс-спектрометров целесообразно обслуживать одним прибором несколько биореакторов с помощью управляемого ЭВМ переключающего устройства, которое последовательно вводит в масс-спектрометр потоки из различных реакторов (рис. 4). Как показано на рис. 4, с помощью этой же ЭВМ можно управлять и процессом (здесь показаны три реактора, но практически один масс-спектрометр может обслуживать до 30 реакторов).
Для контроля состава газового потока в последнее время все чаще применяют масс-спектрометрический метод. Появление сравнительно недорогих серийных масс-спектрометров позволило расширить область применения этих приборов в исследовательских работах, а выпуск надежных, устойчивых к внешним воздействиям промышленных масс-спектрометров обусловил целесообразность их использования в промышленности. Масс-спектрометры выгодно отличаются малым временем отклика (менее 1 мин), высокой чувствительностью (предел обнаружения около 10-5 М), способностью определять несколько компонентов одновременно, линейной зависимостью отклика от концентрации в достаточно широком диапазоне и очень малым дрейфом калибровки. Ввиду высокой стоимости масс-спектрометров целесообразно обслуживать одним прибором несколько биореакторов с помощью управляемого ЭВМ переключающего устройства, которое последовательно вводит в масс-спектрометр потоки из различных реакторов (рис. 4). Как показано на рис. 4, с помощью этой же ЭВМ можно управлять и процессом (здесь показаны три реактора, но практически один масс-спектрометр может обслуживать до 30 реакторов).
РИС. 4. Схема управляемой ЭВМ системы отбора проб при использовании масс-спектрометра для контроля процессов в нескольких реакторах. (Воспроизведено с разрешения из работы: Buckland R. С., Fastert Я., Analysis of Fermentation Exhaust Gas Using a Mass Spectrometer, in Computer Applications in Fermentation Technology, p. 119, Society of Chemical Industry, London, 1982.)
Часто в анализах принимают, что поступающий в систему воздух имеет стандартный состав (20,91% O2, 0,03% СО2), однако иногда в целях повышения надежности и достоверности результатов измерений целесообразно определять состав и поступающего в реактор воздуха, включив, как это показано на рис. 4, его поток в распределяющее устройство. Конечно, такое комплексное и многостороннее использование аналитических приборов с помощью распределяющих устройств выгодно не только в случае масс-спектрометров.
Дата добавления: 2020-10-01; просмотров: 687;











