Определение содержания сахара в растениях методом титрования по Бертрану
Реактивы. 1. 300 г (СН3СОО)2Рь растирают с 50 г свинцового глета РЬО в 100 мл дистиллированной воды. В закрытой стеклом фарфоровой чашке реактив выдерживают на кипящей водяной бане до тех пор, пока желтая масса не приобретет белый или розовый цвет. После этого добавляют 950 мл горячей дистиллированной воды, вместе с которой смесь переносят в бутыль, которую закрывают пробкой и в теплом месте оставляют до осветления раствора. Затем содержимое фильтруют и хранят в закупоренной склянке .
2. 165 г Na2SО4 ∙ 10Н2О растворяют в литровой колбе и доводят объем раствора дистиллированной водой до метки. 3. 20-процентный раствор соляной кислоты. 4. Раствор сульфата меди. 5. Щелочной раствор сегнетовой соли. 6. 10-процентный раствор хлорида бария. 7. 50 г Fe2(SО4)3 растворяют в дистиллированной воде, добавляют 108,7 мл серной кислоты (плотность 1,84) и доводят объем раствора в мерной литровой колбе до метки (если при добавлении к 20 мл реактива 1—2 капель 0,1 н. раствора перманганата калия он окрасится в красный цвет, реактив пригоден к употреблению). 8. 0,1 н. раствор перманганата калия.
В составе плодов и овощей находятся простые (глюкоза, фруктоза) и сложные (сахароза) сахара. Определение сахаров очень важно для характеристики качества продукции.
Обнаружение сахаров титрованием по Бертрану основано на свойстве глюкозы в щелочном растворе восстанавливать окисные соединения меди в закисные. При взаимодействии раствора глюкозы с фелинговой жидкостью образуется осадок оксида меди (I), количество которого соответствует количеству сахара в растворе. Осадок растворяется в сульфате железа (III) в присутствии серной-кислоты. При этом оксидные соединения железа окисляют медь и восстанавливаются в закисные, которые окисляются перманганатом калия.
По израсходованному на титрование (окисление железа) раствору перманганата калия устанавливают содержание сахара в растворе. В связи с тем что между количеством сахара с массой осадка оксида меди (I) прямой пропорциональной зависимости нет, расчет количества сахара ведут по таблице 31.
Сахароза не имеет альдегидных и кетонных групп и не способна восстанавливать медь в фелинговой жидкости. Поэтому предварительно гидролизом (действием соляной кислотой) переводят ее в глюкозу и фруктозу.
Ход анализа. 1. Возьмите навеску свежеизмельченного иследуемого материала (25—50 г).
2. Перенесите навеску через воронку в мерную колбу емкостью 250 мл, ополаскивая дистиллированной водой несколько раз стакан (в котором брали навеску) и воронку, пока в мерной колбе не будет 150 мл жидкости.
3. Содержимое колбы взболтайте и нагрейте на водяной 6aне (при 80° С) в течение 30 мин.
4. После охлаждения добавьте 5-10 мл нейтрального свинцового уксуса (СН3СОО)2РЬ. (Это необходимо для осаждения белковых и красящих веществ.)
5. Доведите объем жидкости в колбе до метки дистиллированной водой, закройте пробкой и взболтайте.
6. После отстаивания жидкость отфильтруйте в сухой стакан или колбу.
7. Фильтрат (50 мл) перенесите пипеткой в мерную колбу 200 мл.
8. В эту же колбу прибавьте 10 мл сульфата натрия до удаления избытка ацетата свинца, доведите объем жидкости в колбе до метки дистиллированной водой, взболтайте и дайте отстояться.
9. Отстоявшуюся жидкость фильтруйте через двойной сухой фильтр в колбу или стакан. В этом фильтрате определяют монет сахара (п.20).
10. Фильтрат (50 мл) перелейте в колбу на 100 мл, поставь ее на водяную баню при 80—82°С, во вторую колбу (контрольную) влейте 50 мл воды, опустите термометр и тоже поставьте водяную баню. Обе колбы нагревайте до 60°С.
11. В колбу с испытуемым раствором прибавьте 5,5 мл 20-процентного раствора соляной кислоты (для процесса гидролиза сахарозы).
12. Обе колбы снова опустите в водяную баню на 8 мин при 68—70°С.
13. Колбу с испытуемым раствором охладите и жидкость в ней нейтрализуйте насыщенным раствором соды Na2C03 индикатору метиловому красному или метиловому оранжевого до перехода окраски раствора в золотистую или чуть желтоватую. Затем доведите дистиллированной водой до метки. Раствор служит для определения общего количества сахара.
14. 50 мл раствора поместите в коническую колбу емкостью 150—200 мл и туда же прилейте смесь из 20 мл раствора сульфата меди и 20 мл щелочного раствора сегнетовой соли.
15. Колбу нагрейте до кипения и кипятите 3 мин.
16. Снимите колбу с огня и дайте 1—2 мин отстояться осадку оксида меди (I).
17. Жидкость фильтруйте через стеклянную вату, не перенося осадка на фильтр. Осадок многократно промывайте декантацией и ту его часть, которая попала на фильтр, отмойте горячей дистиллированной водой, а потом холодной. Окончание отмывания устанавливайте пробой промывных вод на сульфат-ион 10-процентным раствором хлорида бария (муть должна отсутствовать).
18. Отмытый декантацией осадок растворите в колбе, приливая постепенно небольшими порциями раствор сульфата железа (III), подкисленного серной кислотой. Этот осадок вначале чернеет, а затем растворяется и приобретает зелено-голубоватую окраску.
29. Удалив промывные воды из колбы, в нее снова вставьте тот же фильтр и жидкость с растворенным осадком профильтруйте. При этом растворится та часть осадка, которая попала на фильтр при отмывании его декантацией. Колбу промойте теплой дистиллированной водой 2 раза и промывные воды слейте на фильтр.
20. Полученный фильтрат немедленно титруйте 0,1 н. раствором перманганата калия до появления розового окрашивания.
Вычисление результата. Предположим, что 1 мл 0,1 н. раствора перманганата калия соответствует 6,36 мг меди. Пользуясь таблицей 31, найдите (по количеству меди) содержание в исследуемом растворе общего сахара (в мг). Необходимо выразить их в процентах к анализируемому веществу. Для этого надо узнать, какое количество соответствует взятому для анализа раствора.
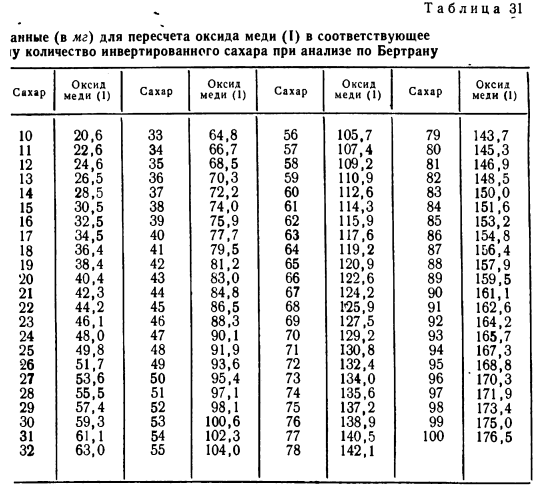
При гидролизе дисахаров соляной кислотой раствор надо дополнительно разбавить в 2 раза (50 мл до 100 мл). Если взять 20 мл такого раствора, то это отвечает 0,5 г или 500 мг исходного исследуемого вещества. Например, на титрование пошло 10 мл 0,1 н. перманганата калия, что соответствует 63,6 мг меди (10 • 6,36), которые в свою очередь отвечают (табл. 31) т мг сахара:
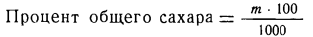
Дата добавления: 2024-11-30; просмотров: 575;











