Химические свойства
Кислота средней силы:
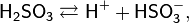
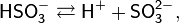
Существует лишь в разбавленных водных растворах (в свободном состоянии не выделена):
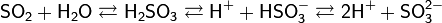
Растворы H2SO3 всегда имеют резкий специфический запах (похожий на запах зажигающейся спички), обусловленный наличием химически не связанного водой SO2.
Двухосновная кислота, образует два ряда солей: кислые — гидросульфиты (в недостатке щёлочи):
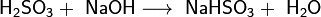
и средние — сульфиты (в избытке щёлочи):
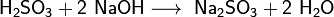
Как и сернистый газ, сернистая кислота и её соли являются сильными восстановителями:
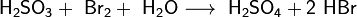
При взаимодействии с ещё более сильными восстановителями может играть роль окислителя:
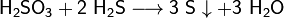
Качественная реакция на сульфит-ионы — обесцвечивание раствора перманганата калия:
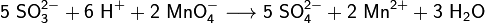
слабая двухосновная кислота, отвечающая степени окисления серы +4
Применение
Сернистая кислота и её соли применяют как восстановители, для беления шерсти, шелка и других материалов, которые не выдерживают отбеливания с помощью сильных окислителей (хлора). Сернистую кислоту применяют при консервировании плодов и овощей. Гидросульфит кальция (сульфитный щелок, Са(HSO3)2) используют для переработки древесины в так называемую сульфитную целлюлозу (раствор гидросульфита кальция растворяет лигнин — вещество, связывающее волокна целлюлозы, в результате чего волокна отделяются друг от друга; обработанную таким образом древесину используют для получения бумаги).
Се́рная кислота́ H2SO4 — сильная двухосновная кислота, отвечающая высшей степени окисления серы (+6). При обычных условиях концентрированная серная кислота — тяжёлая маслянистая жидкость без цвета и запаха, с кислым «медным» вкусом. В технике серной кислотой называют её смеси как с водой, так и с серным ангидридом SO3. Если молярное отношение SO3 : H2O < 1, то это водный раствор серной кислоты, если > 1 — раствор SO3 в серной кислоте (олеум).
Дата добавления: 2016-06-22; просмотров: 1661;











