Термодинамическая система
Основные понятия и определения термодинамики
Энергия
Энергия – количественная мера различных видов материального движения в процессах взаимного превращения движения из одних форм в другие. Существует бесконечное количество видов материального движения и соответственно количество видов энергий: тепловая, электрическая, химическая, магнитная, кинетическая и т.д. Энергия переходит из одного вида в другую при взаимодействии тел. От понятия «вид энергии» следует отличать понятие «форма передачи энергии».
ТДС обладает некоторым полным запасом энергии.
Внутренняя энергия системы «U» [Дж] – это часть полного запаса энергии, которая не зависит от положения системы, как единого целого в поле внешних сил и от ее движения как единого целого. Её можно представить как сумму кинетической энергии молекул, энергии электронов, внутриядерной энергии, энергии взаимодействия между ядром молекулы и электронами, потенциальной энергии или энергии положения молекул в каком либо внешнем поле сил, энергии электромагнитного излучения. Поскольку абсолютное значение внутренней энергии методами термодинамики определить невозможно, то при анализе оценивается её изменение в результате происходящих процессов. Внутренняя энергия есть параметр или функция состояния системы. Ее величина не зависит от того, каким путем система попала в данное состояние и может быть определена из уравнения состояния.
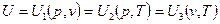
Форм передачи энергии существует только две:
1. Работа. При данном способе передачи происходит макроскопическое перемещение в некотором направлении макроскопического количества частиц – носителей энергии. Это макроскопическая форма передачи энергии. Количество энергии, переданной в этом случае, называют работой процесса.
2. Теплообмен. При данном способе передача энергии осуществляется за счет хаотического, ненаправленного движения микрочастиц. Это микрофизическая форма передачи энергии. Количество энергии переданное таким образом называют теплотой процесса (или количеством теплоты, или теплотой).
Термодинамическая система
Объектом исследования в термодинамике является термодинамическая система (ТДС).
Термодинамическая система (ТДС) – совокупность взаимодействующих макроскопических тел произвольной физической или химической природы. Частным случаем ТДС является рабочее тело тепловой машины (рабочее тело – среда, используемая в машине для преобразования энергии).
Окружающая среда (ОС) – все тела не вошедшие в данную ТДС.
Контрольная поверхность – граница раздела между ТДС и ОС. Это поверхность, через которую осуществляется взаимодействие ТДС с ОС, например – обмен веществом, энергией, работой и т.п. Конкретный вид взаимодействия называют родом взаимодействия. Количество способов взаимодействия называют количеством т/д степеней свободы.
Свойства ТДС зависят от свойств контрольной поверхности, иначе говоря – от особенностей взаимодействия между ТДС и ОС через неё. Традиционно различают следующие виды систем:
По наличию массообмена различают открытую и закрытую ТДС.
Открытая ТДС – это ТДС, которая обменивается с ОС веществом. Частным случаем открытой системы является проточная система, на одних участках контрольной поверхности которой вещество входит, а на других уходит из системы, как это происходит, например, в прямоточном воздушно – реактивном двигателе.
Закрытая (замкнутая) ТДС – система, контрольная поверхность которой не проницаема для вещества. Частным случаем открытой системы является проточная система, на одних участках контрольной поверхности которой вещество входит, а на других выходит.
По особенностям обмена энергией различают изолированную и неизолированную ТДС
Изолированная ТДС – это ТДС, которая не обменивающуюся с ОС ни веществом, ни энергией. Изоляция может быть частичной.
Теплоизолированная (адиабатная) ТДС – это система, которая не обменивается с ОС теплотой, но может обмениваться работой.
Механически изолированная ТДС – это система, которая может обмениваться с ОС теплотой, но не обменивается работой механической деформации.
Термодеформационная система ТДС – это система, которая обменивается с ОС теплотой и работой.
По виду протекающих в ТДС реакций различают простые и сложные ТДС.
Простой называют ТДС постоянного химического состава.
Сложной называют ТДС, где могут протекать химические реакции и осуществляться фазовые переходы.
Дата добавления: 2020-03-21; просмотров: 1275;











