Гипотезы строения стекла
СТРОЕНИЕ И СТРУКТУРА СТЁКОЛ
2.1. Структура стёкол
Свойства вещества зависят от его состава и строения. Строение стекла определяется двумя факторами:
1. Геометрией расположения атомов относительно друг друга.
2. Природой химических связей между атомами.
Основные теоретические направления изучения строения стекла: кристаллохимическое и валентно-химическое. Рассматривается строение стёкол на электронном, атомном, молекулярном уровнях.
Гипотезы строения стекла
До появления экспериментальных методов изучения структуры стёкол учёными выдвигались различные предположения об особенностях их строения. Первые гипотезы строения стекла появились в начале XIX века. На базе этих гипотез возникла современная наука. Самыми мощными орудиями познания учёных того времени были интуиция и законы логики. Экспериментальная проверка гипотез тогда была невозможна, а такие важнейшие разделы науки как термодинамика, статистическая и молекулярная физика ещё не существовали или только зарождались. XX-й век по существу пытался ответить на те же вопросы, которые возникли в начале XIX века. При этом возникали схожие модели, формулировались подобные же гипотезы.
Первой научной гипотезой строения стекла была модель, предложенная в 1835 году немецким учёным М.Л.Франкенгеймом (1801-1869). Франкенгейм считал, что стекло состоит из очень маленьких кристалликов различного размера и, возможно, состава. Кристаллики расположены хаотично и имеют субмикроскопические размеры, намного большие, чем размеры атомов или молекул. При нагревании самые маленькие кристаллики плавятся и растворяют большие кристаллы. Образующийся расплав является смазкой для больших кристаллов.
Смеси, состоящие из различных частиц, не достигают точки плавления внезапно. Когда плавятся некоторые составляющие смеси, тогда становятся подвижными отдельные зёрна слитка. Эта подвижность увеличивается с ростом температуры за счёт того, что всё больше зёрен растворяется в уже жидкой составляющей, пока вся масса не станет жидкой.
Энергия сцепления частиц в кристаллах, стёклах и жидкостях примерно одинакова. В жидкостях частицы подвижны, так как их силовые поля обладают шаровой симметрией. Одинаковое воздействие на частицы с разных сторон не препятствует их взаимному смещению. Если симметрия сил взаимодействия нарушается, то относительное движение частиц вещества затрудняется. Ассимметрия сил когезии вызывает малую сдвиговую податливость всех твёрдых тел.
Гипотеза объясняет постепенный переход от твёрдого состояния к жидкому, кристаллизацию стекла и образование стекла при охлаждении жидкости. Гипотеза Франкенгейма примерно на 90 лет опередила аналогичные представления в современной науке.
Гипотеза Д. И. Менделеева (1834-1907).
Стёкла представляют собой некристаллические кремнезёмистые сплавы оксидов, образовавшиеся в результате переохлаждения соответствующих расплавов. Стёкла – это весьма сложные в структурном отношении тела, свойства которых зависят от природы входящих в их состав оксидов и от количественного соотношения между ними. При обсуждении вопроса о химической природе силикатов, Д.И.Менделеев указывал на полимерность стёкол. Кремнезёмистые молекулы способны соединяться друг с другом в более сложные (полимерные) образования. Этим явлением Д.И.Менделеев объяснял возможность получения стёкол разнообразного состава, содержащих кремнезёмистую составляющую из большего или меньшего числа молекул SiO2 (кремнезёмистый каркас силикатных стёкол) и замещаемую составляющую переменного химического состава. Предположил возможное полимерное строение стёкол, Д.И.Менделеев предвосхитил этим современные гипотезы.
Таким образом, в структуре стекла следует различать две составные части: неизменную и изменяемую. Неизменная часть стекла – это каркас кремнезёмистого сплава, изменение которого должно вызывать изменение свойств соединения в целом. Изменяемая часть содержит элементы, замещение которых не вызывает существенных изменений свойств стекла.
Оксиды в стекле соединяются с образование неопределённых по составу химических соединений. В этом стекло подобно сплавам металлов переменного состава. Д.И.Менделеев: «стекло не есть определённое химическое соединение, а является сплавом оксидов, подобным металлическим сплавам переменного состава».
Кристаллитная гипотеза Лебедева (1893-1969).
Структуру стекла следует рассматривать как скопление микроструктурных образований, аналогичных по кристаллохимическим характеристикам силикатам и кремнезёму. Их количественное соотношение определяется диаграммой состояния системы. Чаще всего в стёклах должна наблюдаться микроэвтектоидная структура. Например, в стекле состава Na2O·3SiO2 при кристаллизации выделяется сначала b-кварц, а затем – дисиликат натрия Na2O·2SiO2. Микрокристаллитные образования в стекле, из которых могут возникать кристаллы, получили название кристаллитов. Кристаллиты – это локальные деформированные структурные микрообразования. В центре кристаллиты имеют наиболее упорядоченное кристаллическое строение, соответствующее обычному кристаллу. По мере перехода от ядра к периферии в структуре кристаллита накапливается всё больше дефектов – структура оказывается аморфной.
В отличие от микрокристаллов, возникающими в стекле при кристаллизации, кристаллиты не имеют поверхностей раздела с аморфной составляющей стекла, которая в качестве прослойки находится между кристаллитами. По приближённым подсчётам Лебедева, концентрация кристаллитов достигает 10 – 15% от объёма стекла. Размер кристаллитов составляет 20 – 30 нм.
Современные рентгеноструктурные исследования подтверждают гипотезу Лебедева. Однако размеры обнаруженных упорядочений в стекле примерно на порядок меньше предсказанных (не более 1,5-2,0 нм). Идея микронеоднородного строения стёкол, заложенная в кристаллитной гипотезе Лебедева, оказалась исключительно плодотворной и предвосхитила современные представления о стекле.
Гипотеза Захариасена.
На основе анализа зависимостей свойств стёкол от состава и данных рентгеноструктурных исследований сделано предположение о непрерывной неправильной сетке стекла.
Структурная сетка стекла выполнена из тех же координационных полиэдров, что и кристаллическая решётка. Для кристаллических модификаций кремнезёма характерна строгая взаимная ориентация кислородных полиэдров в пространстве. Для силикатного стекла угол между кремнекислородными тетраэдрами, соединенными общей вершиной, варьируется в широком диапазоне. Захариасен сделал вывод, что структурная сетка стекла – совершенно беспорядочно расположенные тетраэдры SiO44-. Равновероятным допускается любое взаимное расположение соседних тетраэдров (рис.2.1).
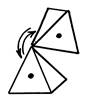
Рис. 2.1 Взаимная ориентация кремнекислородных
тетраэдров в силикатном стекле
По мнению Захариасена, угол в структурной цепочке Si – O – Si может быть совершенно случайный. Гипотеза полностью отрицала возможность какого-либо упорядочения в стекле. Как показали исследования, гипотеза Захариасена оказалась ошибочной. Любой выбранный в структуре стекла тетраэдр вследствие направленности ковалентных связей всегда предопределяет ориентацию соседних тетраэдров. Спектр взаимной ориентации тетраэдров в стекле охватывает действительно относительно широкий диапазон углов. Однако наиболее вероятными оказываются углы, характерные для кристаллических состояний диоксида кремния. Условия стеклообразования, сформулированные Захариасеном, противоречат экспериментальным данным.
Гипотеза Таммана (1861-1938).
Стекло – переохлажденная жидкость. В настоящее время это утверждение Таммана является общепризнанным. Возможность перехода в стеклообразное состояние определяется температурной зависимостью соотношения скоростей образования центров кристаллизации и роста кристаллов на образованных центрах. Чем выше скорость охлаждения, тем больше вероятность получения вещества в стеклообразном состоянии. Тамман впервые ввёл представления об интервале размягчения и граничных температурах Тg и Тf. Он считал, что в интервале размягчения молекулы стекла приобретают характер движения, свойственный жидкому состоянию. Понятие молекул Тамман использовал для органических соединений, для силикатных стёкол структурными составляющими являются не молекулы, а кремнекислородные тетраэдры.
В интервале размягчения в стекле не образуется жидкой фазы, система является однофазной. Постепенное размягчение стекла и его переход в жидкое состояние при высоких температурах сопровождаются непрерывным изменением свойств стекла. В кристаллах такой переход имеет скачкообразный характер.
Гипотеза А.А.Аппена.
Развиты представления
1) о степени связности кремнекислородного каркаса;
2) о координационном состоянии ионов металлов в стекле;
3) о влиянии состава стекла на координационное состояние ионов и свойства стекла.
Повышение основности, т.е. увеличение концентрации кислорода в составе стекла при постоянном содержании оксида кремния вызывает понижение координационных чисел Al, Ti, Co, Pb, Zn. У бора координационное число возратает от 3 до 4, все другие металлические катионы понижают свою координацию.
Основность ↑, к.ч. Al, Ti, Co, Pb, Zn ↓ , к.ч. В↑.
Если в стекле одновременно присутствуют катионы алюминя и бора, при введении оксидов Ме2О или МеО в первую очередь меняют свою координацию ионы алюминия, переходя из шестерной в четверную координацию по кислороду.
Небольшие катионы фосфора, кремния, бора, алюминия и других элементов, несущие высокий заряд, образуют прочные координационные полиэдры с кислородом. Такие полиэдры сохраняют свою индивидуальность (определённость, обособленность) в стёклах различного состава. Это позволило А.А.Аппену создать систему расчётных формул для оценки свойств стёкол исходя из представлений о парциальных свойствах компонентов, входящих в состав стекла.
Дата добавления: 2018-11-26; просмотров: 1547;











