Химические свойства алканов
В молекулах предельных углеводородов все атомы углерода находятся в состоянии sp3- гибридизации атомных орбиталей. Каждый атом углерода затрачивает на соединение с любым соседним атомом углерода не более одной валентности, причем все свободные (не затраченные на соединение с атомами углерода) его валентности насыщены водородом. Поэтому они не вступают в реакции присоединения. При обычных условиях алканы химически инертны, они не взаимодействуют с концентрированными серной и азотной кислотами, щелочами, перманганатом калия. Русский химик М.И. Коновалов назвал алканы «химическими мертвецами». Устойчивость объясняется прочностью связей и их неполярностью.
Предельные углеводороды не склонны к реакциях разрыва связи (реакция присоединения), для них свойственно замещение.
1. Галогенирование алканов. Под воздействием кванта света начинается радикальное замещение (хлорирование) алкана. Общая схема:
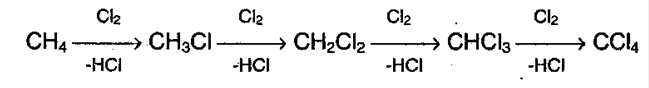
Реакция идет по цепному механизму, в которой различают:
а) Инициирование цепи:
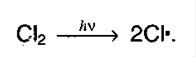
б) Рост цепи:
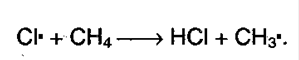
в) Обрыв цепи:
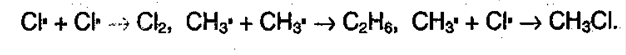
Суммарно можно представить в виде:
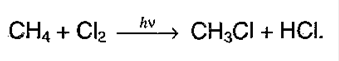
2. Нитрование(реакция М.И.Коновалова)алканов. Реакция протекает при 140 °С при действии 12-14% азотной кислоты:
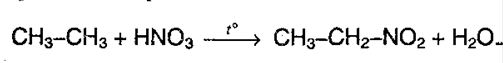
Легче всего реакция протекает с третитичным атомом углерода, чем с первичным и вторичным.
3. Изомеризация алканов. При конкретных условиях алканы нормального строения могут превращаться в разветвленные:
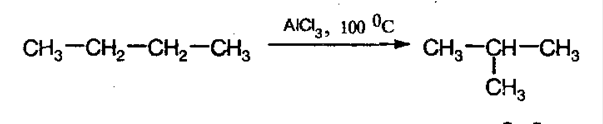
4. Крекинг алканов. При действии высоких температур и катализаторов высшие алканы могут рвать свои связи, образуя алкены и алканы более низшие:
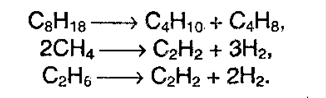
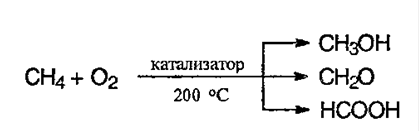
5. Окисление алканов. В различных условиях и при разных катализаторах окисление алкана может привести к образованию спирта, альдегида (кетона) и уксусной кислоты. В условиях полного окисления реакция протекает до конца – до образования воды и углекислого газа:
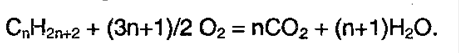
Дата добавления: 2021-10-28; просмотров: 716;











