Нервно-мышечный аппарат
Понятие о биологических основах
Клетка – основная структурная единица всех живых организмов, элементарная живая целостная система (рис.1). Она имеет протоплазму, окруженную мембраной. В клетке есть ядро, в котором содержится наследственная информация – ДНК. В протоплазме имеются структурные образования, органеллы или органоиды:
Рибосомы – в них при помощи РНК производится строительство белка – анаболические процессы.
Митохондрии – энергетические станции клетки, в них при помощи кислорода происходит превращение жиров или глюкозы в углекислый газ, воду и энергию, заключенную в молекулу АТФ.
Эндоплазматическая сеть (саркоплазматический ретикулум) является органеллой, состоящей из мембран и ферметативных систем, прикреплённых к ней.
Комплекс Гольджи – система мембран, образующих совокупность мешочков и пузырьков, служит для синтеза и выделения веществ из клетки.
Лизосомы – пищеварительный Аппарат клетки, органеллы в форме пузырьков содержащие ферменты, которые разрушают белки до простейших составляющих – аминокислот.
Специализированные органеллы – структурные компоненты клетки присущие определённым видам клеток, к примеру в мышечных волокнах – миофибриллы [6,с.15].
Таким образом, необходимо учитывать пищеварительный аппарат клетки – лизосомы, правильно дозируя нагрузку.
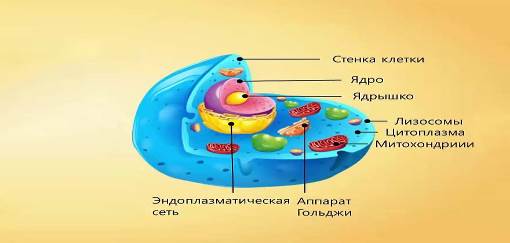
Рисунок 1 - Строение клетки
Нервно-мышечный аппарат
Человек выполняя любые действия, в том числе физические упражнения тратит энергию при помощи нервно-мышечного аппарата.
Нервно-мышечный аппарат (рис. 2) – является совокупностью двигательных единиц. Каждая двигательная единица включает мотонейрон, аксон и совокупность мышечных волокон. Количество двигательных единиц у человека остаются неизменными. Количество мышечных волокон, если и поддаётся изменению, то не более, чем на 5 процентов. В самом мышечном волокне происходит рост количества многих органелл: миофибрилл, митохондрий, саркоплазматического ретикулум, глобул гликогена, миоглобина, рибосом, ДНК и др. Так же, подлежит изменению количество капилляров обслуживающих мышечное волокно.
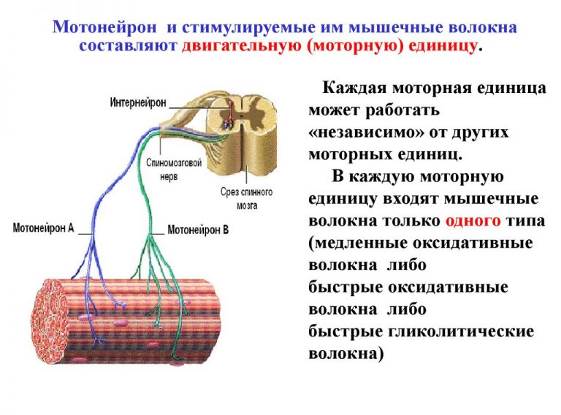
Рисунок 2 - Двигательная (моторная) единица
Миофибрилла – специализированная органелла мышечного волокна (рис.3) Состоит из саркомеров, саркомер включает нити актина и миозина, между которыми образуются мостики при затрате энергии заключённой в АТФ. Поворот мостиков – сокращение миофибрилл – сокращение мышечного волокна – сокращение мышцы. Мостики образуются при наличии в саркоплазме ионов кальция и молекул АТФ. Увеличение количества миофибрилл в мышечном волокне приводит к увеличению его силы, скорости сокращения и размера. При росте миофибрилл происходит разрастание других обслуживающих их органелл, например саркоплазматического ретикулума.
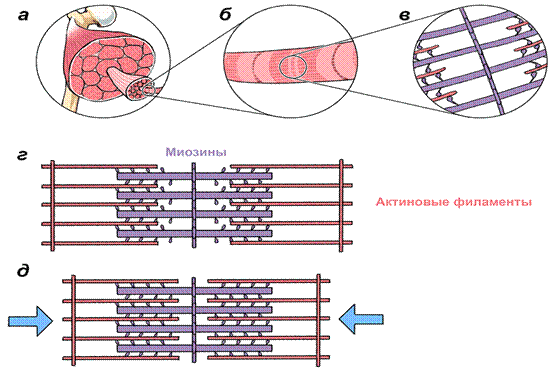
Рисунок 3 - Саркомер
Саркоплазматический ретикулум – это сеть внутренних мембран, которая образует пузырьки, канальцы, цистерны. В мышечном волокне СПР образует цистерны в которых скапливаются ионы кальция. (Предполагается, что к мембранам СПР прикреплены ферменты гликолиза, что при прекращении доступа кислорода приводит к значительному разбуханию каналов. Это явление связано с накоплением ионов водорода (Н+), которые вызывают частичные разрушения белковых структур). Для механизма мышечного сокращения большое значение имеет скорость откачивания кальция из саркоплазмы, так как это обеспечивает процесс расслабления мышцы. В мембраны СПР встроены натрий-калиевые и кольцевые насосы, поэтому есть предположение, что увеличение поверхности мембран СПР по отношению к массе миофибрилл должно вести к росту скорости расслабления МВ. Поэтому увеличение скорости расслабления мышцы должно говорить об относительном приросте мембран [39,с.42].
Поддержание максимального темпа обеспечивается запасами в МВ АТФ, КрФ, массой миофибриллярных митохондрий, массой саркоплазматических митохондрий, массой гликолитических ферментов и буферной ёмкостью содержимого мышечного волокна и крови. Все эти факторы влияют на процесс энергообеспечения мышечного сокращения, но способность поддерживать максимальный темп должна зависеть в основном от митохондрий СПР. Увеличивая количество окислительных МВ – продолжительность упражнения с максимальной мощностью растёт. Так как поддержание концентрации КрФ в ходе гликолиза ведет к закислению МВ, торможению распада АТФ из-за «борьбы» ионов водорода с ионами кальция на головках миозина. Поэтому процесс поддержания КрФ при преобладании в мышце аэробных процессов по мере выполнения упражнения идёт всё более эффективнее. Важно то, что митохондрии активно поглощают ионы водорода, следовательно при выполнении кратковременных предельных упражнений от 10 до 30 секунд их роль является – буферирование закисления клетки [39,c.45].
Митохондрии располагаются везде, где необходима в большом количестве энергия АТФ. В мышечных волокнах энергия требуется для сокращения миофибрилл, поэтому вокруг них образуются миофибриллярные митохондрии.
Биохимия клетки (рис.4).
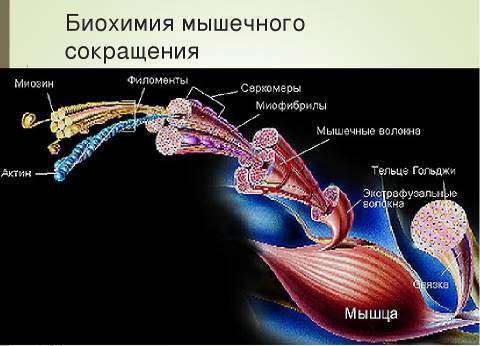
Рисунок 4 - Биохимия мышечного сокращения
Хорошо известно, что мышечная активность есть результат преобразования химической энергии, содержащейся в АТФ, в механическую энергию сокращения миофибрилл. Освобождение энергии происходит благодаря ферменту АТФ – азе, который имеется в тех местах клетки, где требуется энергия. В следствии освобождения энергии образуются молекулы АДФ, Ф, Н+. Ресинтез АТФ происходит за счёт запаса КрФ. КрФ отдавший энергию распадается на креатин и фосфат. Креатин и фосфат распространяются по цитоплазме и активируют активность ферментов, которая связана с синтезом АТФ. Есть два основных пути образования АТФ: анаэробный и аэробный.
Анаэробный путь – гликолиз, связан с ферментативными системами, расположенными на мембране СПР и в саркоплазме. При появлении рядом с этими ферментами креатина и фосфата происходит цепь химических реакций, при которых гликоген или глюкоза распадается до пирувата с образованием молекул АТФ. Молекулы АТФ сразу отдают энергию для ресинтеза КрФ, а АДФ и Ф опять используются в гликолизе для образования новой молекулы АТФ. Пируват имеет две возможности для преобразования:
1) при помощи фермента лактат- дегирогеназы мышечного типа пируват превращается в лактат. Этот метаболический путь – гликоген – пируват – лактат – называется анаэробным гликолизом и сопровождается образованием и накоплением ионов водорода [39,c.48].
2) подойти к митохондриям, превратиться в ацетил – коэнзим – А, подвергнуться окислительному фосфорилированию до образования углекислого газа, воды и молекул АТФ. Этот метаболический путь – гликоген – пируват – митохондрия – углекислый газ и вода – называют аэробным гликолизом.
Аэробный путь – окислительное фосфорилирование, связан с митохондриальной системой. При появлении рядом с митохондриями криатина и фосфата при помощи митохондриальной КФК – азы выполняется ресинтез КрФ за счёт АТФ, образовавшейся в митохондрии. АДФ и Ф поступают обратно в митохондрию чтобы образовать новую молекулу АТФ. Для синтеза АТФ есть два метаболических пути:
1) Аэробный гликолиз;
2) Окисление липидов.
Аэробные процессы связаны с поглощением ионов водорода, а в медленных мышечных волокнах (МВ сердца и диафрагмы) преобладает фермент лактат – дегидрогеназа сердечного типа, который более интенсивно превращает лактат в перуват. Поэтому при функционировании медленных МВ идёт быстрое устранение лактатов и ионов водорода [39,c.48].
Увеличение в мышечном волокне лактата и ионов водорода приводит к ингибированию окисления жиров, а интенсивное окисление жиров приводит к накоплению в клетке цитрата, а он угнетает ферменты гликолиза.
Таким образом, аэробный и анаэробный пути включают в работу разные мышечные волокна.
Физиология мышечной деятельности (рис.5).
Мышца включает определённую совокупность мышечных волокон. МВ различаются между собой. Их классифицируют по АТФ-азной активности, по активности ферментов гликолиза или окислительного фосфорилирования. Следовательно, мышцы разделяют на быстрые и медленные (ГМВ, ОМВ).
Биохимия и физиология мышечной активности могут быть описаны следующим образом:
- сначала производим усилие с малым внешним сопротивлением, тогда рекрутируются низкопороговые двигательные единицы мышечного волокна. Они имеют высокие окислительные возможности, источником являются жирные кислоты. Но первые 10-20 секунд энергообеспечение происходит за счёт запасов АТФ и КрФ в активных мышечных волокнах. Постепенно происходит рекрутирование новых мышечных волокон. Усиливается активизация ЦНС, что приводит к вовлечению новых двигательных единиц мышечных волокон. Постепенное увеличение внешней нагрузки (мощности) сопровождается пропорциональным изменением некоторых показателей: возрастает ЧСС, потребление кислорода, лёгочная вентиляция, не изменяется концентрация молочной кислоты и ионов водорода [39,с.52].
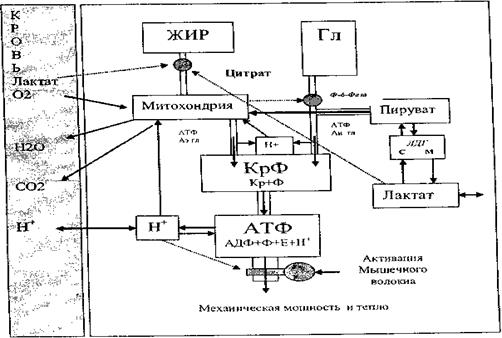
Рисунок 5 - Энергообеспечение клетки
- при достижении определённой мощности наступает момент, когда в работу включаются все ММВ и начинают рекрутироваться промежуточные мышечные волокна (ПМВ). В ПМВ активизируется гликолиз, пируват преобразовывается в молочную кислоту, которая выходит в кровь, проникает в ММВ. ММВ при попадании лактата перестают окислять жиры и субстратом окисления становится в большей мере гликоген. Значит, признаком рекрутирования всех ММВ есть увеличение в крови концентрации лактата и усиление лёгочной вентиляции. Лёгочная вентиляция усиливается из-за накопления в ПМВ ионов водорода, которые при выходе в кровь вызывают образование избыточного углекислого газа. Повышение концентрации углекислого газа в крови приводит к активации дыхания. Имеет место, явление которое принято называть аэробным порогом (АэП), что свидетельствует о рекрутировании всех ММВ.
- дальнейшее увеличение мощности требует рекрутирования более высокопороговых двигательных единиц мышечного волокна, что усиливает процессы анаэробного гликолиза, в кровь выходит больше лактата и ионов водорода. При попадании продуктов распада в ММВ митохондрии переваривают их, однако мощность метохондриальной системы имеет предел. Поэтому сначала наступает равновесие, а затем равновесие нарушается и лактат, Н+, СО2 – вызывают резкую интенсификацию физиологических функций.
Дыхание один из наиболее чувствительных процессов, реагирует очень активно. Меняется субстрат окисления в ММВ на углеводы, что обеспечивает максимальную скорость образования энергии в митохондриях ММВ. Следовательно, потребление кислорода или мощность на анаэробном пороге (АнП) характеризует максимальный потенциал (мощность) ММВ.
- дальнейший рост внешней мощности вовлекает более высокопороговые двигательные единицы, которые иннервируют гликолитические мышечные волокна. Динамическое равновесие нарушается, продукция Н+, лактата начинает превышать скорость их устранения, что влечёт за собой увеличение лёгочной вентиляции, ЧСС и потребления кислорода. После АнП потребление кислорода в основном связано с работой дыхательных мышц и миокарда. При достижении предельных величин лёгочной вентиляции и ЧСС, или при локальном утомлении мышц потреблении е кислорода стабилизируется, а за тем начинает уменьшаться. В этот момент фиксируют МПК [39,с.53].
МПК есть сумма величин потребления кислорода окислительными мышечными волокнами (ММВ), дыхательными мышцами и миокардом.
Следовательно, энергоснабжение при упражнениях более 60 секунд в большей части идёт за счёт запасов гликогена в мышцах и в печени.
По длительности поддержания мощности АнП можно судить о запасах гликогена в мышцах.
Увеличение мощности АнП (рост митохондриальной массы ММВ) приводит к адаптационным процессам – увеличение количества капилляров и их плотности. Это даёт основание предполагать, что увеличение мощности АнП одновременно говорит о росте массы ММВ, а также степени капелиризации ММВ.
Таким образом, выстраивать тренировочный процесс необходимо с учётом энергообеспечения клетки.
Сердце и кровообращение
Деятельность сердца и сосудов обеспечивает кровообращение - непрерывное движение крови в организме. В своем движении кровь проходит по большому и малому кругам кровообращения. Большой круг начинается от левого желудочка сердца, включая аорту, отходящие от нее артерии, артериолы, капилляры, вены и заканчивается полыми венами, впадающими в правое предсердие. Малый круг кровообращения начинается от правого желудочка, далее - легочная артерия, легочные артериолы, капилляры вены, легочная вена, впадающая в левое предсердие.
Функцией сердца является ритмическое нагнетание в артерии крови. Сокращение мышечных волокон стенок предсердий и желудочков называют систолой, а расслабление - диастолой.
Количество крови, выбрасываемое левым желудочком сердцем в минуту, называется минутным объемом кровотока (МОК). В покое он составляет 45 л/мин. Разделив МОК на частоту сердечных сокращений в минуту, можно получить ударный объем кровотока или сердца (УОС). В покое он составляет 60-70 мл крови.
Частота и сила сокращений зависят от нервной, гуморальной регуляции биомеханических условий работы желудочков.
При вертикальном положении имеется механический фактор тяжести крови, затрудняющий работу сердца, приток венозной крови к правому предсердию. В нижних конечностях скапливается 300-800 мл крови.
При мышечной работе минутный объем кровотока растет за счет увеличения ЧСС и УОС. Заметим, что УОС достигает максимума при ЧСС 120-150 уд/мин, а максимум ЧСС бывают при 180-200 и более уд/мин. МОК достигает 18-25 л/мин у нетренированных лиц при достижении максимальной ЧСС. В этот момент сердце доставляет организму максимум кислорода: 4,288 л/мин.
Если бы мышцы нетренированного человека могли бы полностью использовать весь приходящий кислород, то этот человек мог бы стать мастером спорта по бегу на длинные дистанции (бегуны мирового класса потребляют кислород на уровне анаэробного порога 4,0-4,5 л/мин). Однако в мышцах мало митохондрий, поэтому максимальное потребление кислорода у нетренированного мужчины составляет 3-3,05 л/мин (45-50 мл/кг/мин), у нетренированной женщины 2-2,2 л/мин (40-45 мл/кг/мин. На уровне анаэробного порога потребления кислорода составляет в среднем 60-70% МПК, что в 2 раза меньше, чем у мастеров спорта [12,c/49].
Кровеносные сосуды
Сердце при сокращении (систоле) выталкивает кровь в аорту и легочную артерию, растягивая их и создавая давление крови (Р). Движению крови препятствует сосудистое (периферическое) сопротивление. Максимальное давление называется систолическим артериальным давлением (САД), минимальное - диастолическим (ДАД). В условиях покоя в норме САД = 120, ДАД = 80 рт. ст. Между растяжимостью артерий и давлением обратная зависимость. Чем растяжимее артерии, тем больше крови может быть нагнетено без увеличения артериального давления (АД). При атеросклерозе стенки аорты менее эластичны, поэтому надо сильнее нагнетать кровь (тот же объем, что и у здорового человека), чтобы она дальше шла по сосудам. Сопротивление кровотоку зависит от вязкости крови и от просветов сосудов. Увеличение напряжения мышц вызовет перекрытие сосудов - увеличение сосудистого сопротивления. Накопление в крови мышц продуктов анаэробных процессов приводит к рабочей гиперемии - расширению кровеносных сосудов, т.е. уменьшению АД.
Нервный контроль и гуморальный наиболее важны в управлении функциями сосудистой системы. Симпатические нервные волокна иннервируют гладкие мышцы в стенках артериальных и венозных сосудов, особенно мелких. Кровоток через капилляры определяется местными факторами. Сосудосуживающий эффект связан с выделением из окончаний адренергических симпатических волокон норадреналина, который вызывает эффект сокращения гладкомышечных сосудистых клеток, имеющих альфа-рецепторы на мембране (почки, печень, желудочно-кишечный тракт, легкие, кожа). Сосудорасширительный эффект вызывает действие норадреналина и адреналина на гладкомышечные клетки, имеющие бета-рецепторы.
Таким образом, сердечно-сосудистая система так же выполняет кислород-транспортную функцию [12,с..49].
Эндокринная система
Эндокринная система состоит из желез внутренней секреции: гипофиза, щитовидной, околощитовидных, поджелудочной, надпочечников, половых. Эти железы выделяют гормоны - регуляторы обмена веществ, роста, полового созревания организма.
Регуляция выделения гормонов осуществляется нервно-гуморальным путем. Изменение состояния физиологических процессов достигается посылкой нервных импульсов из ЦНС к некоторым железам (гипофизу). Выделяемые передней долей гипофиза гормоны регулируют деятельность других желез - щитовидной, половых, надпочечников.
Принято различать симпатоадреналовую, гипофизарно адренокортикальную, гипофизарно-половую системы.
Симпатоадреналовая система ответственна за мобилизацию энергетических ресурсов. Адреналин и норадреналин образуются в мозговом веществе надпочечников и вместе с норадреналином, выделяющимся из нервных окончаний симпатической нервной системы, действуют через систему «аденилатциклаза-циклиеский аденозин монофосфат (цАМФ)». Для необходимого накопления цАМФ в клетке требуется ингибировать цАМФ-фосфодиэстеразу - фермент, катализирующий расщепление цАМФ. Ингибирование осуществляется глюкокортикоидами (инсулин противодействует этому эффекту).
Система «аденилатциклаза - цАМФ» действует следующим образом. Гормон током крови подходит к клетке, на наружной поверхности клеточной мембраны которой имеются рецепторы. Взаимодействие гормон-рецептор приводит к конформации рецептора, т.е. к активации каталитического компонента аденил атциклазного комплекса. Далее из АТФ начинает образовываться цАМФ, который участвует в регуляции метаболизма, клеточной дифференциации, синтезе белков, мышечном сокращении.
Гипофизарно-адренокортикальная система включает нервные структуры, кровоснабжение и надпочечники. В состоянии стресса усиливается выход кортиколиберина из гипоталамуса в кровоток. Это вызывает усиление секреции адренокортикотропного гормона (АКТГ), который током крови переносится в надпочечники.
Механизм действия глюкокортикоидов на синтез ферментов может быть представлен следующим образом:
кортизол, кортикостерон, кортикотропин, кортиколиберин проходят через клеточную мембрану (процесс диффузии);
в клетке гормон (Г) соединяется со специфическим белком-рецептором (Р), образуется комплекс (Г-Р);
комплекс Г-Р перемещается в ядро клетки (через 15 минут) и связывается с хроматином (ДНК);
стимулируется активность структурного гена, усиливается транскрипция информационной РНК (иРНК);
образование и-РНК стимулирует синтез других видов РНК. Непосредственное действие глюкокортикоидов на аппарат трансляции состоит из двух этапов:
1) освобождение рибосом из эндоплазматической сети и усиление агрегации рибосом (наступает через 60 минут);
2) трансляции информации, т.е. синтез ферментов (в печени, в железах внутренней секреции, скелетных мышцах).
После выполнения своей роли в ядре клетки Г отщепляется от рецептора (время полураспада комплекса около 13 мин), выходит из клетки в неизменном виде.
На мембранах органов-мишеней имеются спецрецепторы, благодаря которым осуществляется транспорт гормонов в клетку. Клетки печени имеют особенно много таких рецепторов, поэтому глюкокортикоиды в них интенсивно накапливаются и метаболизируются. Время полужизни большинства гормонов составляет 20-200 мин [39,с.57].
Гипофизарно-щитовидная система имеет гуморальные и нервные взаимосвязи. Предполагается ее синхронное функционирование с гипофизарно-адренокортикальной системой. Гормоны щитовидной железы (тироксин, трийодтиронин, тиротропонин) положительно сказываются на процессах восстановления после выполнения физических упражнений.
Гипофизарно-половая система включает гипофиз, кору надпочечников, половые железы. Взаимосвязь между ними осуществляется нервным и гуморальным путем. Мужские половые гормоны - андрогены (стероидные гормоны), женские - эстрогены. У мужчин биосинтез андрогенов осуществляется в основном в клетках лейдига семенников, В женском организме стероиды образуются в надпочечниках и яичниках, а также коже. Суточная продукция у мужчин составляет 4-7 мг, у женщин в 10-30 раз меньше. Органы-мишени андрогенов - предстательная железа, семенные пузырьки, семенники, придатки, скелетные мышцы, миокард. Этапы действия тестостерона на клетки органов-мишеней следующие:
тестостерон превращается в более активное соединение 5-альфадегидротестостерон;
образуется комплекс Г-Р;
комплекс активизируется в форму, проникающую в ядро;
происходит взаимодействие с акцепторными участками хроматина ядра (ДНК);
усиливается матричная активность ДНК и синтез различных видов РНК;
активизируется биогенез рибосом и полисом и синтез белков, в том числе андрогенозависимых ферментов;
увеличивается синтез ДНК и активизируется клеточное деление.
Важно заметить, что для тестостерона участие в синтезе белка необратимо, гормон полностью метаболизируется [39,с.57].
Гормоны, попадающие в кровь, подвергаются элиминации, причем при росте мощности интенсивность метаболизма, в частности глюкокортикоидов, возрастает. Основой повышения тренированности эндокринной системы являются структурные приспособительные перестройки в железах. Известно, что тренировка приводит к росту массы надпочечников, гипофиза, щитовидной железы, половых желез (через 125 дней детренировки все возвращается к норме). Отмечено, что увеличение массы надпочечников сочетается с повышением содержания ДНК, т.е. интенсифицируется митоз - растет количество клеток. Изменение массы железы связано с 2 процессами - синтеза и деградации. Синтез железы прямо пропорционально зависит от ее массы и обратно пропорционально - от концентрации гормонов в железе. Скорость деградации увеличивается с ростом массы железы и механической мощности, уменьшается - с повышением концентрации анаболических гормонов в крови.
Таким образом, эндокринная система выполняет регулирующую функцию.
Иммунная система
Человек имеет механизмы надзора - иммунную систему. Эта система защищает человека от болезнетворных микроорганизмов и от раковых клеток, распознает и избирательно уничтожает вторгшиеся в организм чужеродные агенты. Различают клеточный и гуморальный виды ответа.
Клеточный иммунный ответ особенно эффективен против грибов, паразитов, внутриклеточных вирусных инфекций, раковых клеток и чужеродных тканей. Гуморальный иммунный ответ проявляется преимущественно в период внеклеточной фазы бактериальных и вирусных инфекций.
Иммунная система (рис. 6) - совокупность всех лимфоидных органов и скоплений лимфоидных клеток: вилочковая железа, селезенка, лимфатические узлы, пейперовы бляшки, стволовые клетки костного мозга.
Взаимодействие организма с чужеродными размножающимися антигенами академик Р.В. Петров (1987) представил 4 процессами:
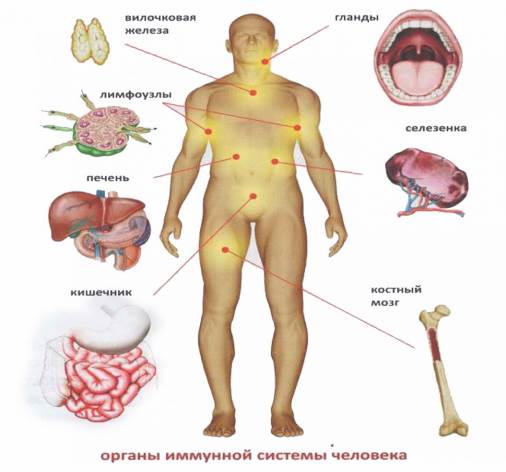
Рисунок 6 - Органы иммунной системы
Размножение приникших чужеродных клеток. Изменение числа антигенов зависти от темпа их размножения за данный отрезок времени минус то их число, которое нейтрализуется за это время существовавшими ранее или появившимися антителами.
Иммунная система организма реагирует на антигенное вторжение накоплением иммунокомпетентных клеток. Запускающим реакции субстратом является комплекс антигена с рецептором распознающего Т-лимфоцита. Количество плазмоклеток зависит от числа активированных В-лимфоцитов и от темпа их пролиферации минус их убыль за счет старения.
Количество антител в данном отрезке времени зависит от скорости их производства минус то количество, которое связывается антигеном, и то количество, которое выводится за счет естественного их катаболизма.
Функционирование иммунной системы организма зависит от нормальной работы других систем и органов. Вирус поражает какую-нибудь систему не обязательно непосредственно лимфоидную. Это может быть, печень, легкие, железы внутренней секреции и др. В любом случае поражение может достигать такой глубины, которая отразится на обеспечении работы иммунной системы.
Простейшая модель иммунологической реакции организма на вирус является одновременно простейшей моделью инфекционного заболевания. Самый придирчивый критик не сможет найти, как пишет Р. Петров (1987), здесь неучтенного процесса, если иметь в виду базовые процессы.
Простейшая математическая модель иммунной системы была разработана академиком Г.И. Марчуком (1985). Она позволяет имитировать основные закономерности протекания защитной реакции организма, в модели не различаются клеточные и гуморальные компоненты иммунитета. Предполагаются, что такие компоненты имеются.
Модель включает элементы: пул антигенов, пул антител, пул плазмоклеток, орган-мишень [14.с.47].
Имитационное моделирование реакции иммунной системы введением разного исходного уровня антигенов показало, что модель демонстрирует хроническую, субклиническую, острую и летальную форму болезни.
Хроническая форма болезни имеет место в том случае, когда в организм постоянно поступает в небольших дозах инфекция. В этом случае устанавливается динамическое равновесие между синтезом патогенных микробов и их элиминацией, благодаря адекватному производству антител. Субклиническая, острая или летальная форма заболевания может быть вызвана двумя способами: однократным введением возрастающей дозы антигенов, уменьшением массы органа-мишени.
Кроветворная стволовая клетка костного мозга является предшественником различных форм иммунологического реагирования (Т- и В-систем). По мере старения количество стволовых клеток уменьшается. В возрасте 65-76 лет иммунная активность антител составляет 20-30% от максимального уровня.
Таким образом, иммунная система выполняет защитную функцию.
Пищеварение
К органам пищеварения относятся: полость рта, глотка, пищевод, желудок, тонкая и толстая кишка.
Пищеварение (рис.7) - физиологический процесс, благодаря которому пища, поступившая в пищеварительный тракт, подвергается физическим и химическим изменениям, а образующиеся питательные вещества всасываются в кровь и лимфу.
Физические изменения пищи связаны с ее механической обработкой, перемешиванием, растиранием. Химические изменения состоят из последовательных этапов гидролитического расщепления пищи с помощью ферментов и соляной кислоты желудка [47,с.29].
В полости рта происходит размельчение, смачивание слюной и формирование пищевого комка. Вкусовые рецепторы рта возбуждают определенные отделы ЦНС, в результате рефлекторно активизируется секреция слюнных, желудочных и поджелудочных желез, осуществляется двигательный акт глотания и продвижения пищи по пищеводу.
В слюне содержатся ферменты (птиалин, мальтоза) гидролитического расщепления углеводов. В желудке действие ферментов слюны прекращается (кислая среда).
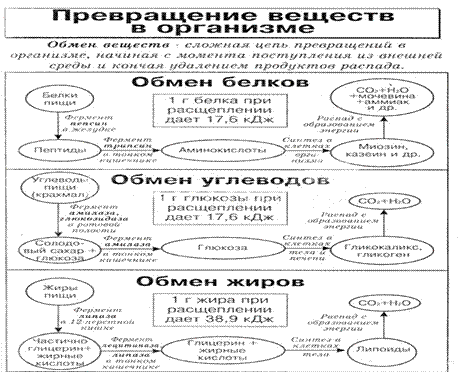
Рисунок 7 - переваривание веществ.
В желудке пища находится в течение нескольких часов и постепенно переходит в кишечник. Желудочный сок выделяется железами и содержит соляную кислоту (рН-0,9 - 1,5), протеазы-пепсины, желатиназы, химозины (расщепляют белки), липазы (расщепляют эмульгированные жиры). На мясо выделяется больше соляной кислоты, на хлеб больше выделяется ферментов, жиры вызывают угнетение желез желудка в течение нескольких часов, затем наблюдается возбуждение симпатической нервной системы. Возбуждение симпатической нервной системы и появление в крови адреналина оказывает тормозящее влияние на секрецию желудочных желез.
Быстрота перехода пищи из желудка в кишку зависит от объема, состава и консистенции пищи. Пища находится в желудке 6-8 часов. Углеводистая пища эвакуируется быстрее, чем белковая; жирная пища задерживается на 8-10 часов. Жидкости начинают проходить кишку почти тотчас после их поступления в желудок. Содержимое желудка уходит в кишку, когда его консистенция становится жидкой или полужидкой.
В двенадцатиперстной кишке пища подвергается действию поджелудочного сока, желчи, выделений брунеровых и либеркюновых желез. В отсутствие пищеварения среда кишки имеет слабо щелочную реакцию (рН - 7,2-8,0), это связано с наличием бикарбонатов.
Поджелудочный сок богат ферментами, действующими на белки (трипсин, химотрипсин и др.), углеводы (амилаза, мальтаза, лактаза и др.), жиры (липаза) и нуклеиновые кислоты (нуклеазы). Секреция поджелудочного сока начинается через 2-3 мин после приема пищи и продолжается 6-14 часов.
Желчь является продуктом секретной работы печеночных клеток. Она активизирует деятельность ферментов - липазы.
А.М. Уголев установил, что пористая поверхность тонкой кишки, адсорбируя ферменты, способствует усилению энзиматических процессов. Пристеночное пищеварение сопровождается процессом всасывания элементарных единиц пищи (мембранное пищеварение) [4,с98].
В толстых кишках находится богатая бактерийная флора, вызывающая сбраживание углеводов и гниение белков. В результате микробного брожения происходит расщепление растительной клетчатки, освобождение содержимого растительных клеток и их усвоение с помощью кишечного сока. В толстых кишках происходит сгущение поступающего содержимого (вода всасывается в толстом кишечнике), образуется кал.
Всасывание представляет собой сложный физиологический процесс прохождения веществ через эпителиальную мембрану кишечной стенки (тонкой или толстой кишки) и поступления их в кровь или лимфу.
Углеводы активно (с затратой энергии АТФ) всасываются в кровь в основном в виде глюкозы или галактозы [47,с.32].
Всасывание аминокислот происходит главным образом в тонком кишечнике и является активным, требующим энергии АТФ процессом. Далее они попадают портальную систему, следовательно, в печень. Аминокислоты быстро (5 мин) попадают из крови в печень и во все другие органы.
После приема жирной пищи тонкий кишечник содержит анионы жирных кислот и смесь моно-, ди- и триглицеридов, хорошо эмульгированных солями желчных кислот и мылами. Основная часть этой смеси всасывается через стенку тонкого кишечника. Глицерин водорастворим и вместе с жирными кислотами с короткой цепью уходит в кровь. Жирные кислоты с длинной цепью проникают в лимфатическую систему.
Таким образом, пищеварительная система главный поставщик энергии.
Жировая ткань
Жировая ткань является самостоятельным в отношении гистоэмбриогенеза образованием. Она выполняет три основные функции:
- синтез триглицеринов из сывороточных липидов и глюкозы;
- сохранение их в жировых депо;
- освобождение их из жировых депо.
Жировая клетка - адипоцит (рис.8), может увеличиваться в размере по мере накопления липидов, протоплазма клетки отжимается на периферию вместе с ядром, которое постепенно уплощается. В межклеточном пространстве располагаются кровеносные капилляры, подходящие к каждой жировой клетке. Здесь же проходят ретикулярные волокна, выполняющие опорную механическую роль. Нервные волокна, иннервирующие жировые клетки, в основном принадлежат симпатической нервной системе. Нервные стволы поступают в жировую ткань вместе с сосудами, далее они постепенно разволокняются и нервные волокна охватывают каждую жировую клетку.

Рисунок 8 - Адипоцит
В жировой ткани происходят как процессы превращения углеводов в жиры, так и переход жиров в углеводы [47,с.29].
Биосинтез жирных кислот происходит в основном в цитоплазме адипоцитов. Сырьем для биосинтеза является ацетилкоэнзим - А, который образуется из избыточной глюкозы или аминокислот.
Липолиз усиливается под действием катехоламинов, которые захватываются клетками активизированной жировой ткани. При стрессовых ситуациях увеличивается скорость высвобождения жирных кислот и глицерина из жировой ткани.
Таким образом, жировая ткань – это самый большой запас энергии.
Дата добавления: 2021-09-25; просмотров: 1192;











