ПЕРЕРАБОТКА УГЛЕВОДОРОДНЫХ ГАЗОВ
Все углеводородные газы (УГ) по их происхождению можно разделить на две большие группы - первичные и вторичные.
Первичные УГ - это газы, добываемые непосредственно из земных недр. По условиям залегания они могут быть разделены на природные и попутные нефтяные УГ. К природным УГ относят легкие по составу газы (от метана до бутана) собственно газовых месторождений (ГМ), а также газы газоконденсатных месторождений (ГКМ), которые выносят на поверхность в сконденсированном виде в небольших количествах (от 5 до 400 г/м) более тяжелые углеводороды (конденсаты).
Попутные УГ - это газы, добываемые вместе с нефтью на нефтяных месторождениях.
Вторичные УГ - это легкие углеводороды, образовавшиеся за счет термокаталитических превращений при переработке нефти. Они обычно включают углеводороды от метана до пентана и могут быть насыщенными (предельными) и ненасыщенными (непредельными).
Насыщенные вторичные УГ - это газы, содержащие только насыщенные углеводороды, образующиеся при первичной дистилляции нефти (как результат десорбции остатков растворенного в нефти попутного газа) и в каталитических процессах, протекающих в атмосфере избытка водорода (гидрокрекинг, гидроочистка, изомеризация, каталитический риформинг).
Ненасыщенные вторичные УГ - это газы, содержащие олефиновые углеводороды, которые образуются в деструктивных процессах с недостатком водорода, таких, как каталитический крекинг, термический крекинг, коксование, пиролиз.
В данной главе рассматривается переработка первичных углеводородных газов. Переработка вторичных УГ и газоконденсатов рассмотрена в других главах.
2.1. Физико-химические основы процессов ректификации, экстракции, абсорбции и адсорбции
Физико-химические основы процессов ректификации
Разделение много компонентной жидкости на фракции или индивидуальные вещества осуществимо при ее нагревании и отводе от нее образовавшихся паров.
Возможно образование паров с поверхности (испарение) и во всем объеме жидкости (кипение). Кипение происходит тогда, когда наблюдается равенство внешнего (например, атмосферного) давления и давления паров жидкости при заданной температуре. Чем ниже внешнее давление, тем при более низкой температуре начинает закипать жидкость.
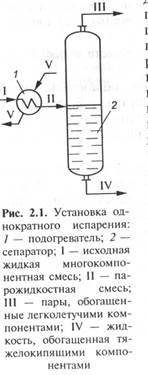
Если многокомпонентную жидкость нагреть до кипения, то образовавшиеся пары будут находиться с ней в равновесии. Подадим теперь эту парожидкостную смесь в пустотелый цилиндр (сепаратор), имеющий два выходных штуцера - верхний и нижний. Смесь будет делиться в сепараторе на две фазы - паровую и жидкую. Паровая фаза будет уходить из сепаратора через верхний штуцер, а жидкая - через нижний. При этом паровая фаза будет обогащена легкокипящими (низкокипящими), а жидкая - тяжелокипящими (высококипящими) компонентами. Такой процесс называется однократным испарением. Его можно осуществить непрерывным способом. Схема процесса однократного испарения изображена на рис. 2.1.
Для лучшего понимания процессов испарения многокомпонентных жидких смесей проанализируем диаграмму температура - состав двухкомпонентной жидкости, состоящей из веществ А и В. Ее состав будет определяться мольными долями хА и хВ веществ А и В. Общее давление в системе будем поддерживать постоянным (изобарическим). Если известны зависимость давления пара от состава жидкой фазы при нескольких температурах и температуры кипения каждой из двух чистых жидкостей, то можно построить диаграмму, выражающую зависимость температуры кипения от состава жидкой фазы, так называемую рыбку. Такая диаграмма изображена на рис. 2.2.
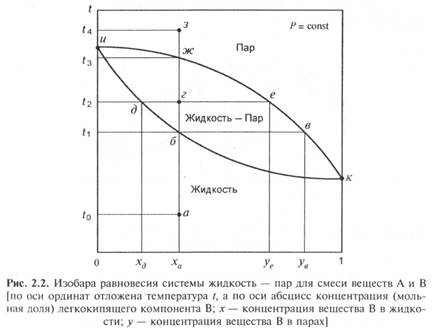
Нижняя кривая является кривой начала кипения жидкости.
Под ней находится некипящая жидкость, а над ней - область совместного существования жидкости и насыщенного (влажного) пара (парожидкостная смесь). Над верхней кривой находится область перегретого пара. Сама верхняя кривая - это кривая начала конденсации (росы) паровой фазы.
Выберем на рис. 2.2 в области некипящей жидкости некоторую точку, а при температуре t0 и составе xa. В этой точке концентрация вещества В составит xa, а вещества А соответственно (1 - xa). Начнем нагревать жидкость, т. е. двигаться вверх от точки, а к точке б. При достижении точки б система будет уже состоять из жидкости и пара. Состав пара теперь определяется координатой точки в. Очевидно, что концентрация легкокипящего компонента В в парах ув будет больше, чем в жидкости xa (точка У. находится правее точки х). Если мы будем нагревать нашу парожидкостную смесь, не отводя из нее пары, то достигнем точки г. Дальнейший нагрев переведет последнюю каплю жидкости в пар в точке ж. Нагревая пар, мы достигнем, например, точки з. В этой точке пар будет перегретым при температуре t4.
Если при движении от точки б к точке ж мы остановимся в точке г и захотим узнать состав жидкой и паровой фаз, то нужно провести через точку г горизонтальную линию. В точке д мы будем иметь состав жидкой фазы xд, а в точке е - состав пара уе.
 Мы рассматривали поведение раствора, состоящего из двух идеальных жидкостей А и В. Это такие жидкости, которые дают растворы, подчиняющиеся правилу аддитивности. Например, если взять по 1 л жидкости А и жидкости В и их смешать, то мы получим 2 л раствора. Это говорит о том, что между молекулами А и В нет никакого взаимодействия.
Мы рассматривали поведение раствора, состоящего из двух идеальных жидкостей А и В. Это такие жидкости, которые дают растворы, подчиняющиеся правилу аддитивности. Например, если взять по 1 л жидкости А и жидкости В и их смешать, то мы получим 2 л раствора. Это говорит о том, что между молекулами А и В нет никакого взаимодействия.
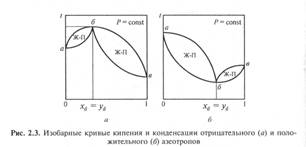
В реальности могут встречаться растворы, проявляющие различные отклонения от законов идеальных растворов. Например, имеются растворы, дающие азеотропы. Это когда кривые равновесий сливаются в одну точку, в которой состав паровой и жидкой фаз одинаков.
Диаграммы температура-состав, имеющие точки азеотропа, представлены на рис. 2.3.
Мы рассмотрели принцип действия установки однократного испарения. Если пары, выходящие из сепаратора, сконденсировать, то мы получим две жидкости. Одна из них (конденсат паров, или дистиллят) будет обогащена низкокипящим компонентом, а другая (кубовая жидкость) - высококипящим. Однако в этом случае нельзя достичь высокой четкости разделения смеси. В дистилляте будет содержаться некоторое количество высококипящих, а в кубе - низкокипящих компонентов.
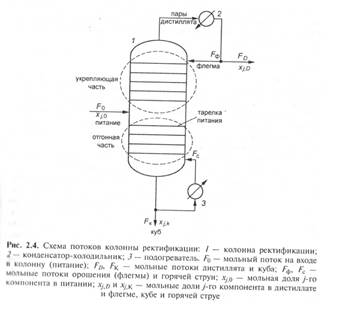 Возможно, организовать многократное испарение и конденсацию многокомпонентного раствора (ректификацию). Для этого вместо сепаратора, в котором только однократно происходит контакт жидкой и паровой фаз, устанавливают вертикальный цилиндр, снабженный так называемыми тарелками. Тарелки, закрывающие все сечение цилиндра, имеют переливные патрубки для жидкости, которая образует на ней слой определенной высоты (рис. 2.4). Отверстия в тарелке служат для прохода паров, поднимающихся снизу вверх по колонне и проходящих через слой жидкости на тарелке.
Возможно, организовать многократное испарение и конденсацию многокомпонентного раствора (ректификацию). Для этого вместо сепаратора, в котором только однократно происходит контакт жидкой и паровой фаз, устанавливают вертикальный цилиндр, снабженный так называемыми тарелками. Тарелки, закрывающие все сечение цилиндра, имеют переливные патрубки для жидкости, которая образует на ней слой определенной высоты (рис. 2.4). Отверстия в тарелке служат для прохода паров, поднимающихся снизу вверх по колонне и проходящих через слой жидкости на тарелке.
Организация жидких и паровых потоков в колонне происходит следующим образом. Парожидкостная смесь после нагревателя попадает на определенную тарелку, называемую тарелкой питания. Тарелка питания находится приблизительно в середине колонны ректификации. Пары начинают подниматься в верхнюю часть колонны или укрепляющую ее часть, жидкость же стекает вниз - в отгонную часть. Чтобы в укрепляющей части колонны создать парам встречный поток жидкости, после самой верхней тарелки устанавливают конденсатор. Пары, уходящие с верхней тарелки, попадают в конденсатор и выходят из него в виде жидкости. Поток этой жидкости делится на две части. Одна из них возвращается на верхнюю тарелку в виде орошения, называемого также флегмой. Другая часть отводится для дальнейшей переработки или как товарный продукт.
Чтобы в отгонной части колонны создать жидкости встречный поток пара, внизу колонны устанавливается подогревающее устройство (кипятильник). В кипятильнике часть жидкости, стекающей с нижней тарелки, испаряется и возвращается вниз колонны в виде паров.
Конструктивно конденсатор и кипятильник могут быть выполнены в различных вариантах.
Кроме тарельчатых, в промышленности, и особенно в лабораторной практике, используют насадочные колонны. В этом случае колонна вместо тарелок имеет слой насадки определенной высоты. Насадка, чаще всего выполненная из керамики или металла, должна иметь высокую удельную поверхность (развитую поверхность), на которой стекающий вниз слой жидкости контактирует с поднимающимися вверх парами.
В нефтезаводской практике распространены преимущественно тарельчатые колонны. Их использование в процессах переработки нефти объясняется значительно большей производительностью по сравнению с насадочными. Тарельчатые колонны малых диаметров дороже насадочных. Однако по мере увеличения диаметра стоимость последних растет намного быстрее первых. Для оценки можно считать, что стоимость тарельчатых колонн растет пропорционально диаметру колонны в первой, а насадочных - во второй степени.
Длительный опыт промышленной эксплуатации насадочных колонн показал целесообразность их использования при диаметрах не более 0,8 м, тогда как в нефтепереработке колонны диаметром меньше 1м встречаются крайне редко. Это и определило преимущественное распространение тарельчатых колонн в нефтяной промышленности.
В нефтезаводской практике большей частью применяются колпачковые, ситчатые, клапанные и другие виды устройств для создания максимальной поверхности контакта паровой и жидкой фаз на тарелке в колонне ректификации. Увеличение поверхности контакта фаз увеличивает скорость массообмена между паром и жидкостью, способствуя установлению равновесия между фазами.
Если при заданных давлении и температуре успевает устаноl3иться равновесие между фазами, то такую тарелку называют теоретической. На практике, несмотря на тарелки различной конструкции, равновесие на них не успевает установиться.
Число реальных тарелок при прочих равных условиях всегда превышает число теоретических. Отношение числа теоретических тарелок к числу практических тарелок называется коэффициентом полезного действия тарелки (КПД). КПД реальных тарелок всегда меньше единицы и меняется в широких пределах от 0,4 до 0,8.
Ректификацию высококипящих фракций нефти осуществляют в колоннах, работающих под разрежением, т. е. при давлении ниже атмосферного. Это делают для того, чтобы понизить температуру кипения всех компонентов и тем самым уменьшить протекание побочных химических процессов, например, уплотнения разделяемых в колонне веществ.
Такого же эффекта можно добиться, вводя в колонну газы или пары веществ, которые не конденсируются при рабочих давлении и температуре процесса ректификации. Чаще всего используют пары воды.
После конденсатора газы легко отделяются от дистиллята, т. е. жидкой фазы, в газожидкостном сепараторе. Если использовались пары воды, то после конденсатора смесь двух несмешивающихся жидкостей (водной и углеводородной) разделяют путем отстоя.
Кроме простых колонн, в которых смесь делится на дистиллят и куб (см. рис. 2.4), в практике нефтеперегонки используют сложные колонны. В них осуществляется дополнительно отбор фракций с промежуточных тарелок (сбоку колонны), т. е. происходит деление исходной смеси более чем две фракции.
Физико-химические основы процессов абсорбции, экстракции и адсорбции
Абсорбцией называют процесс поглощения газов жидкими поглотителями (абсорбентами), в которых газы растворяются. Обратный процесс выделения растворенных газов из растворителя носит название десорбции. В абсорбционных процессах участвуют газовая и жидкая фазы. При абсорбции происходит переход вещества из газовой фазы в жидкую, а при десорбции, наоборот - из жидкой в газовую.
На практике абсорбции подвергают чаще всего газовые смеси, необходимые компоненты которых могут поглощаться растворителем в заметных количествах. Непоглощаемая часть газовой смеси называется инертным газом.
Жидкая фаза состоит из поглотителя и абсорбированного (поглощенного) компонента газовой фазы. Если между молекулами поглотителя и· абсорбированного компонента газовой фазы не происходит химического взаимодействия, то это - физическая абсорбция. При наличии химических реакций между молекулами поглотителя и абсорбированного компонента процесс называется хемосорбцией.
Существуют различные способы осуществления контакта газовой и жидкой фаз. Как и при ректификации жидких смесей, абсорбция осуществляется чаще всего в цилиндрических аппаратах (абсорберах), имеющих слой насадки или определенное количество тарелок. В абсорберах поглотитель движется сверху вниз, а газовая смесь противотоком снизу вверх. Из нижней части абсорбера выводится поглотитель с абсорбированными в нем компонентами газовой смеси. Из верхней части абсорбера отводится остаточная газовая смесь, из которой удалены абсорбированные компоненты.
В абсорберах с насадкой осуществляется непрерывный контакт между жидким поглотителем и газовой фазой. В тарельчатых абсорберах такой контакт происходит на тарелках, т. е. ступенчато.
При физической абсорбции полное извлечение компонентов из газовой фазы практически невозможно.
При хемосорбции абсорбируемый из газа компонент связывается с жидкой фазой в виде нелетучего химического соединения. Если химическая реакция необратима, то возможно полное извлечение компонента из газа.
Повышение давления и снижение температуры активизируют процесс абсорбции. Десорбция, наоборот, осуществляется при пониженном давлении и повышенной температуре. Конструктивно десорберы аналогичны абсорберам.
Промышленное проведение абсорбции может сочетаться или с сочетаться с десорбцией. Если десорбцию не производят, то абсорбент используется однократно. Сочетание абсорбции с десорбцией позволяет многократно использовать абсорбент и выделять абсорбированный компонент в концентрированном виде практически любой чистоты.
Выходящий из абсорбера раствор поглотителя с абсорбированным (растворенным) в нем компонентом газа направляют на десорбцию. Здесь происходит разделение на газовую (бывший поглощенный компонент) и жидкую (абсорбент) фазы. Регенерированный поглотитель вновь возвращается на абсорбцию. При такой схеме (круговой процесс) абсорбент практически не расходуется, если не считать его небольших потерь. Поглотители, в которых абсорбция сопровождается необратимой химической реакцией, регенерируются только химическими, а не физическими способами.
Абсорбция, десорбция и ректификация являются процессами одной и той же диффузионной природы. Различие заключается в том, что в случае ректификации, взаимодействующие жидкий и паровой потоки обмениваются компонентами, тогда как явления абсорбции и десорбции имеют одностороннюю направленность. Это связано с тем, что абсорбент можно считать практически нелетучим по сравнению с компонентами газовой фазы.
На нефтегазовых заводах абсорбция и десорбция углеводородных газовых смесей проводятся, главным образом, в тарельчатых колоннах, расчет и анализ работы которых ведется на базе метода теоретической тарелки.
Экстракцией называется процесс извлечения из сырья, находящегося в твердом или жидком (для нефтепереработки) состоянии, отдельных его компонентов путем обработки, избирательно действующим растворителем (экстрагентом).
При экстракции образуются две несмешивающиеся фазы: сырье-растворитель. Это могут быть твердое тело - жидкость или жидкость-жидкость. Эти фазы должны легко отделяться одна от другой при отстаивании. Скорость перехода компонентов из сырья в растворитель зависит от поверхности контакта фаз так же, как и в процессах ректификации и абсорбции.
Очевидно, что вначале сырье и растворитель должны быть хорошо и быстро перемешаны, а потом разделены при их отстаивании. Образовавшиеся две несмешивающиеся фазы носят название экстрактной и рафинатной. В составе экстрактной фазы будут находиться, главным образом, растворитель и хорошо растворимые в нем компоненты сырья. Рафинат будет содержать оставшуюся часть сырья и растворенную в ней небольшую часть растворителя. Например, если отгонкой из разделенных путем отстаивания фаз удалить растворитель, то получим экстракт и рафинат. Экстракт будет в основном состоять из компонентов сырья, извлеченных из него путем экстракции.
Экстрагент должен обладать следующими свойствами при экстракции из жидкой фазы:
• не растворяться совсем или минимально растворяться в сырье;
• образующиеся экстрактная и рафинатная фазы должны значительно отличаться по плотности;
• проявлять высокую избирательность и растворяющую способность по отношению к извлекаемому веществу;
• заметно отличаться по температуре кипения от извлекаемого вещества, что облегчает их разделение (например, путем ректификации);
• быть химически устойчивым или инертным веществом. Экстракцию можно организовать так, что смешивание сырья и растворителя и затем их разделение - отстаивание будет осуществлено в непрерывном режиме многократно, например, в полочных колонных аппаратах.
Процесс растворения зависит от химического строения молекул растворителя и растворяемого вещества. Надежных теоретических представлений о природе растворимости нет. На качественном уровне можно только отметить, что вещества, значительно отличающиеся по полярности, плохо растворяются одни в других. Наоборот, равнополярные вещества взаимно хорошо растворяются.
На рис. 2.5 показана схема противоточной экстракции с четырьмя ступенями перемешивания экстрагента и сырья. В нашем случае экстрагент имеет большую плотность, чем сырье, и поэтому он подается сверху колонны. Противотоком снизу поднимается сырье.
В случае, когда растворитель имеет меньшую плотность, чем сырье, места их ввода меняются: сырье подается сверху, а экстрагент - снизу.
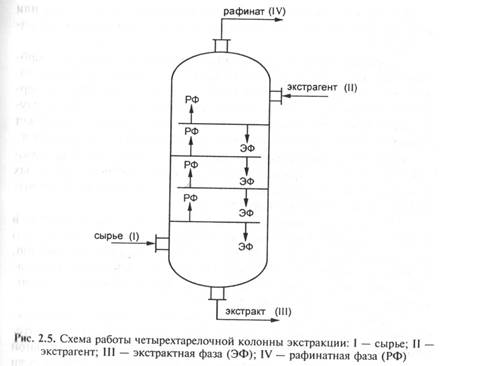
Применение колонных аппаратов целесообразно в тех случаях, когда при рабочей температуре процесса потоки имеют невысокую вязкость, что позволяет при помощи встроенных в колонну контактных устройств осуществить надежное перемешивание фаз. При этом разность плотностей рафинатной и экстрактной фаз такая, что в свободном пространстве между контактными устройствами (полками, тарелками и др.) происходит хорошее разделение фаз, что предотвращает их взаимный унос. В противном случае вместо колонных экстракторов применяются экстракторы другого устройства. Чаще всего смешение потоков происходит в специальных горизонтально расположенных смесителях (например, аппаратах с мешалками). Разделение фаз осуществляется в отдельных отстойниках. Смеситель и отстойник образуют одну ступень экстракции.
Адсорбцией называют процесс поглощения газов, паров или жидкостей поверхностью твердого тела, которое называется адсорбентом.
Адсорбция имеет определенные преимущества перед абсорбционным методом разделения смесей. В отходящем после абсорбции, например, газовом потоке, обязательно будет содержаться некоторое количество извлекаемого компонента. В случае адсорбции его конечная концентрация практически может равняться нулю. На этом основан принцип работы противогаза.
Адсорбцию целесообразно применять для разделения газовых смесей, концентрация извлекаемых компонентов в которых невысока, или в случаях, когда необходимо достичь полного выделения веществ из газового потока.
При высоких концентрациях извлекаемых компонентов в потоке адсорбент будет быстро насыщаться, что потребует его частой регенерации. В таких случаях лучше сочетать адсорбцию, например, с абсорбцией. Сначала абсорбцией из потока извлекается основная масса вещества, а затем осуществляется его окончательное извлечение путем адсорбции.
В качестве адсорбентов, применяемых в нефтепереработке, используют активированные угли, силикагель, алюмогель, синтетические цеолиты. Все эти вещества обладают большой удельной поверхностью, которая определяется отношением поверхности (м2) к единице массы адсорбента (г), т. е. имеет размерность м2/г. Другой характеристикой адсорбентов является их активность (удельная сорбционная емкость). Это количество адсорбированного вещества (г), отнесенное к единице массы (кг) или объема адсорбента (л). Размерность активности - г/кг или г/л. Часто активность выражают также в процентах от веса адсорбента.
Различают статическую и динамическую активности. Статическая активность определяется в момент равновесия при данной температуре. Экспериментально она определяется в периодических условиях и говорит о максимальном количестве вещества, адсорбированного единицей массы адсорбента.
На рис. 2.6 представлена типичная зависимость от времени количества адсорбируемого вещества, отнесенного к единице массы адсорбента.
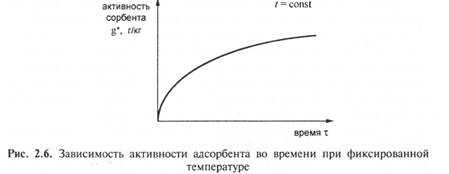
Динамическая активность характеризуется количеством вещества, поглощенного адсорбентом до появления следов адсорбируемого вещества на выходе из аппарата.
Рассмотрим некоторые характеристики важнейших адсорбентов.
Активированные угли получают следующим образом. Вначале вещества растительного (дерево, торф, уголь, скорлупа орехов) и животного (кости) происхождения, а также синтетические смолы, углеродные волокна нагревают без доступа воздуха с целью получения твердого углеродистого или минерального остатка. Затем с целью увеличения удельной поверхности и ее модификации эти твердые вещества обрабатывают при высоких температурах (несколько сотен градусов Цельсия) парам и воды, углекислым газом или воздухом (так называемое активирование).
Полученные таким образом активированные угли имеют различную удельную поверхность, плотность, зернение и активность. Величина удельной активности может колебаться от 600 до 1700 м2 на 1 г угля. Активированные угли применяются в виде зерен различных размеров (от 1 до 7 мм) или в виде порошка. Зерна имеют форму цилиндриков или таблеток при формовании порошков или неправильную форму, если они получаются дроблением.
Активные угли имеют три основных разновидности пор: микро- и макропоры, а также средние между ними - переходные поры (мезопоры). Размеры микропор соизмеримы с размерами адсорбируемых молекул. Удельная размерность микропор выражается сотнями, переходных - десятками, а макропор единицами квадратных метров на грамм. Очевидно, что для адсорбции основное значение имеет микропористая структура активных углей. Основная задача мезопор и макропор - это транспортирование адсорбируемого вещества вглубь частиц адсорбента.
Активированные угли гидрофобны, поэтому они особенно пригодны для адсорбции неполярныx органических соединений.
Силикагель получают обезвоживанием геля кремниевой кислоты SiО2 x nH2О, который образуется при взаимодействии кислот с раствором силиката натрия. Гель после промывки сушат и получают высокопористую твердую массу. В ней равномерно распределены близкие по размерам поры. Силикагель термостоек, но обладает невысокой механической прочностью.
Алюмогель - активный оксид алюминия Al2O3, содержащий небольшое (около 1% мас.) количество оксидов кремния, железа, титана и др. Он обладает высокой активностью к парам воды, превосходя в этом отношении силикагель. Кроме того, алюмогель имеет высокую механическую прочность, вытесняя в процессах осушки газов силикагель.
Широкое распространение как адсорбенты и подложки для различных катализаторов получили цеолиты - алюмосиликатные пористые кристаллы. Цеолиты встречаются в природе, но для технических целей их специально синтезируют. Наиболее часто используют цеолиты типов А и Х. Цеолиты получаются в виде очень мелких кристаллов. В гидратированном виде - это сплошные твердые тела. После сушки образуются пористые кристаллы. Пористая структура собственно кристаллов цеолитов неизменна для каждого типа. В состав цеолитов входят ионы кремния, алюминия, кислорода, а также способные к ионному обмену катионы щелочных и щелочноземельных металлов. Поры типов А и Х представляют собой сферические полости, которые соединяются друг с другом узкими отверстиями, называемыми окнами. Диаметр окон зависит от природы ионообменного катиона и составляет несколько ангстрем (~4-9 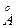 ). Проникать в полости через окна могут только те молекулы, размеры которых меньше размеров окон. На этом основана резко выраженная избирательность адсорбционных свойств цеолитов, которые называются также молекулярными ситами.
). Проникать в полости через окна могут только те молекулы, размеры которых меньше размеров окон. На этом основана резко выраженная избирательность адсорбционных свойств цеолитов, которые называются также молекулярными ситами.
Цеолиты особенно энергично адсорбируют электрически несимметричные молекулы (например, воды, углекислого газа и др.). Хорошо сорбируются цеолитами органические вещества, имеющие кратные связи, - ацетилен, этилен.
В технике цеолиты типов А и Х применяют в виде гранул, таблеток, шариков, состоящих из кристаллических порошков цеолитов и добавок связующих веществ, обычно глин. После термической обработки при температуре 550-6000С формованные цеолиты при обретают необходимую механическую прочность. Такие цеолиты применяются для тонкой (тщательной) очистки газов и жидкостей, а также для выделения из смесей газов и жидкостей отдельных компонентов.
В промышленности используются адсорбционные аппараты с неподвижным и движущимся слоем адсорбента периодического и непрерывного действия. Адсорберы с неподвижным (стационарным) слоем являются аппаратами периодического действия. Процесс проводится до достижения определенной степени насыщения, чаще всего до появления следов адсорбируемого вещества на выходе из аппарата. Затем в этом же аппарате осуществляется десорбция. Пара аппаратов, работая попеременно на адсорбцию и десорбцию, позволяет осуществлять практически непрерывный процесс. В адсорберах с движущимся слоем перемещение адсорбента происходит под действием силы тяжести или силы трения восходящего газового потока. В первом случае адсорбент непрерывно движется сверху вниз, во втором - пылевидный адсорбент находится во взвешенном (псевдоожиженном) состоянии. В адсорбере с движущимся слоем осуществляется не только непрерывная адсорбция, но и десорбция. Эти установки получили название гиперсорберов.
Дата добавления: 2016-06-05; просмотров: 4276;











