Поражение почек при васкулитах, ассоциированных с ANCA
К ANCA-ассоциированным ПСВ, при которых выявляют малоиммунный сегментарный пролиферативный ГН с некрозами и полулуниями, относятся два типа васкулитов: грануломатозный полиангиит, ГПА (ранее – гранулематоз Вегенера) и микроскопический полиангиит (МПА), поражающие мелкие сосуды. ГПА и МПА одинаково часто встречаются у мужчин и женщин, средний возраст пациентов составляет 50-60 лет. Еще существует локальный почечный васкулит, когда выявляется характерное поражение почек с положительными результатами серологического исследования на ANCA, но без системных проявлений. Некоторые считают его вариантом МПА [9, 14].
Этиология и патогенез связывают с инфекциями, главным образом, дыхательных путей. Известна более высокая частота обострений ГПА у носителей золотистого стафилококка. Имеются сообщения о профилактической роли своевременной антибактериальной терапии в развитии заболеваний. Ключевую роль в патогенезе ГПА и МПА отводят ANCA, однако следует заметить, что низкие титры ANCA иногда обнаруживаются при других системных заболеваниях соединительной ткани и системных инфекциях. При эозинофильном гранулематозе с полиангиитом (ЭГПА, ранее -синдром Чарджа-Штросса) ANCA выявляются в 45%. Высокие титры ANCA определяются у пациентов с васкулитами, вызванными лекарствами (например, антитиреоидными).
ANCA – это антитела, реагирующие с антигенами нейтрофилов. Различают 2 разновидности ANCA: цитоплазматические c-ANCA и перинкулеарные р-ANCA. C-ANCA направлены против протеиназы 3 и чаще присутствуют у пациентов ГПА, хотя их не считают специфичными для данного заболевания. Перинуклеарные антитела в 90% направлены против миелопероксидазы, их выявляют чаще при МПА. ANCA-отрицательными являются УП, болезнь Такаясу и гигантоклеточный артериит.
Морфология. Характерно выявление фокального и сегментарного некротизирующего ЭКГН. При ИФ исследовании иммуноглобулины или фракции комплемента отсутствуют (малоиммунный ЭКГН). Обнаружение гранулем в почечной и других тканях является характерным признаком ГПА [14].
Клиническая картина. Возможно появление кожной сыпи, признаков поражения ЖКТ, ЦНС. Общие симптомы включают лихорадку, потерю в весе, миалгии, артралгии и др. симптомы. Самыми характерными являются признаки поражения верхних дыхательных путей. Могут иметь место язвенно-некротические риниты, синуситы, средний отит. У детей чаще, чем у взрослых, выявляются надгортанный, трахеальный или эндобронхиальный стенозы. В отличие от ГПА, поражение верхних дыхательных путей у пациентов с МПА встречается редко и не приводит к деструкции тканей. Прогноз определяет, наряду с поражением почек, легочный капиллярит. Самым опасным осложнением является легочное кровотечение. Рентгенологически выявляются массивные инфильтраты, признаки геморрагического альвеолита. При ГПА также поражаются легкие, но изменения выяляются чаще только рентгенологически. Грануломатозное поражение глазницы у пациентов с ГПА может привести к выраженному экзофтальму. Поражение почек развивается часто (ГПА – 80-90%, МПА – 90-100%). Проявления могут быть разными, от изолированного мочевого синдрома до БПГН. Самая частая причина БПГН – системные васкулиты [9, 13]. Изолированный мочевой синдром проявляется чаще микрогематурией в сочетании с умеренной протеинурией. АГ выявляется у 50% пациентов с ГПА с поражением почек, реже – при МПА.
Диагноз. Для гранулематозного полиангиита характерно наличие классической триады: поражение верхних дыхательных путей, легких и почек. Обнаружение ANCA (чаще c-ANCA) и биопсия почки подтверждают диагноз ГПА. Однако пациенты нередко лечатся у ЛОР-врачей или других специалистов, где упускаются изменения в почках на ранних стадиях. При любом подозрении васкулитов необходимо следить за уровнем креатинина крови. При обращении к нефрологу, как правило, уже имеют место признаки прогрессирующего почечного заболевания (БПГН). Поэтому очень важно сотрудничество ревматологов с нефрологами. Нередко именно почечное поражение определяет тяжесть заболевания и нефрологу в данной ситуации принадлежит главная роль в ведении пациента. Диагноз МПА подтверждает поражение почек и легких с выявлением р-ANCA (у 80%) и малоиммунного фокального сегментарного некротического ГН, как правило, с полулуниями в клубочках. Общие изменения в крови и моче неспецифичны (повышение СОЭ, СРБ, эритроцитурия и протеинурия). Необходимо проведение скрининга на все ГН и другие заболевания, протекающие с развитием почечно-легочного синдрома, в том числе исследование анти-ГБМ, серологических маркеров СКВ, опухолей у пациентов с ANCA-ассоциированным ПСВ. Встречаются сочетания ANCA с анти-ГБМ антителами. У пациентов с МПА, в отличие от УП, маркеры ВГВ отсутствуют.
Лечение. Прогноз зависит от своевременности и адекватности ИСТ. Благодаря прогрессу ИСТ на современном этапе, выживаемость при ГВ и других ПСВ повысилась. Необходимо придерживаться международно принятых принципов лечения, включающих индукционную, поддерживающую терапию и лечение обострений ANCA-ассоциированных васкулитов (KDIGO 2012) [8].
Индукционная терапия. Для лечения малоиммунного фокального сегментарного некротизирующего ГН рекомендуются ЦФ и ГКС. У пациентов с менее тяжелыми формами заболеваний и наличием противопоказаний к циклофосфамиду, проводится лечение ритуксимабом и ГКС. В особых случаях:
· при быстром нарастании креатинина в крови
· при необходимости диализной терапии
· при легочном кровотечении
рекомендуется дополнительное проведение плазмаообмена (ПО). ПО также показан у пациентов с перекрестным синдромом – сочетанием ANCA-ассоциированного васулита и анти-ГБМ ГН.
У пациентов, зависимых от диализа, в течение 3 месяцев и при наличии внепочечных проявлений ГПА, рекомендуется отменить терапию ЦФ. После достижения полной ремиссии продолжается поддерживающая терапия в течение минимум 18 месяцев. У пациентов на диализе и не имеющих внепочечные проявления заболевания, поддерживающая терапия не проводится.
В качестве поддерживающей терапии рекомендуется азатиоприн в дозе 1-2 мг/кг/сут, при непереносимости к нему – ММФ в дозе до 1 г в два приема. У пациентов с поражением верхних дыхательных путей в качестве дополнительного препарата предложено применять триметоприма-сульфаметоксазол. При непереносимости АЗА и ММФ применяют метотрексат (в начале 0.3 мг/кг/нед, максимально 25 мг/нед), но только при СКФ >60 мл/мин.
При обострениях: применяют индукциионную терапию в полном объеме. В настоящее время первым выбором в лечении рецидива ANCA-нефритов является ритуксимаб.
Рефрактерные формы заболевания. При ANCA-ассоциированном ГН, резистентном к индукционной терапии ЦФ и ГКС, рекомендуется добавить ритуксимаб или применять в/в иммуноглобулин, либо провести ПО. Режимы иммуносупрессии зависят от активности органных поражений, но не от титров ANCA. Трансплантация почки рекомендуется не ранее чем через 12 месяцев после достижения полной ремиссии внепочечных проявлений. Отличием МПА являются более частые показания к проведению повторных курсов ПО и в/в введения иммуноглобулинов из-за характерного для этого заболевания тяжелого легочного васкулита. При БПГН, который может быть основным проявлением васкулита, жизненно важное значение имеет быстрое начало пульс-терапии МП и ЦФ. В настоящее время даже при агрессивной ИСТ 5-летняя выживаемость составляет 65%.
Следующий клинический случай является примером когда диагноз и терапия стали возможным только после консультации нефролога.
Пациентка Щ., 31 год. В начале лета появился шум в ушах, снижение слуха, головокружение. Диагностирован катаральный отит, обострение хронического ринита, неврит слухового нерва. Через неделю присоединились боли в нижнечелюстном суставе. Через месяц выявлены СОЭ 45 мм/час, креатинин сыворотки крови 93 мкмоль/л, была госпитализирована в ЦКБ, где выявлены СОЭ 52 мм/ч, креатинин 98 мкмоль/л, протеинурия 1,5 г/л. При КТ ОБП: лимфаденопатия, МРТ головы – мастоидит справа. Исследование на АНЦА антитела были положительными. Через 2 недели в ЛОР-клинике диагностирован кохлеоневрит, в связи с чем назначается гормональная терапия (в/в преднизолон в течение 5 дней). На этом фоне – СОЭ 40 мм/час, креатинин 72 мкмоль/л, восстановление слуха. Из раннего анамнеза: сезонный аллергический ринит. 1-я беременность – замерший плод, 2-я беременность 2 года назад,, ребенок здоров. Отеков и повышения артериального давления не отмечено. Предварительный диагноз: АНЦА-ассоциированный васкулит, рАНЦА повторно положительно.
Биопсия почки проведена через 2 недели: Светооптическое исследование выполнено на парафиновых срезах с использованием окрасок: PAS-реакция, трихром по Массону, импрегнация солями серебра по Джонсу, гематоксилин-эозин.
В материале нефробиопсии представлены корковый и мозговой слои ткани почки (рис.6.3); 17 клубочков, тотально склерозированных – 2. В 12 клубочках имеются полулуния, 11 клеточных и 1 фиброзное циркулярное (в тотально склерозированном клубочке). Некроз капиллярных петель в 6 клубочках с клеточными полулуниями. Стаз нейтрофилов в просвете капиллярных петель.
4 клубочка не изменены, не увеличены, с одноконтурной равномерной капиллярной стенкой, без гиперклеточности, сегментарного склероза, депозитов и полулуний.
Очаговый тубулонекроз с исчезновением щеточной каймы, расширением просветов канальцев, слущиванием клеток тубулярного эпителия в просвет канальцев. Очаговая инфильтрация мононуклеарами и небольшим количеством нейтрофильных лейкоцитов. Небольшой отек интимы артерий. Легкий очаговый интерстициальный фиброз и атрофия канальцев.
Иммуногистохимическое исследование: со всеми реагентами отрицательный результат.
ЗАКЛЮЧЕНИЕ: Экстракапиллярный некротизирующий гломерулонефрит (полулуния в 70,6%, некроз капиллярных петель в 35%, тотальный склероз в 11,8% клубочков). Очаговый тубулонекроз. Очаговый интерстициальный фиброз и атрофия канальцев.
Примечание: гистологическая картина может соответствовать АНЦА-ассоциированному или анти-ГБМ ЭКГН.
А
В
С
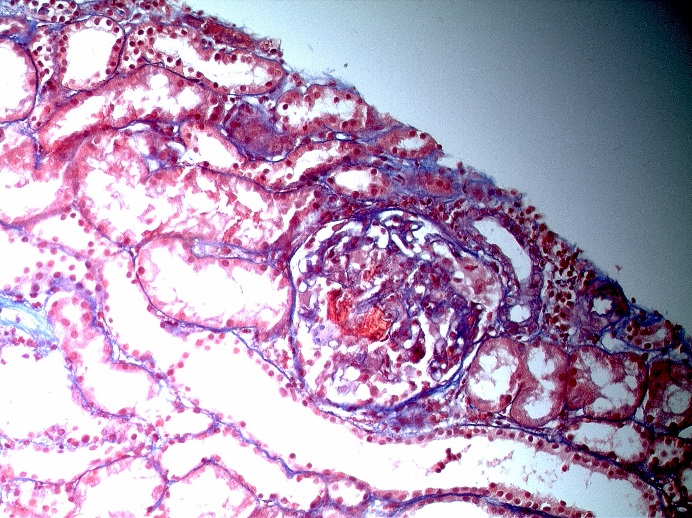
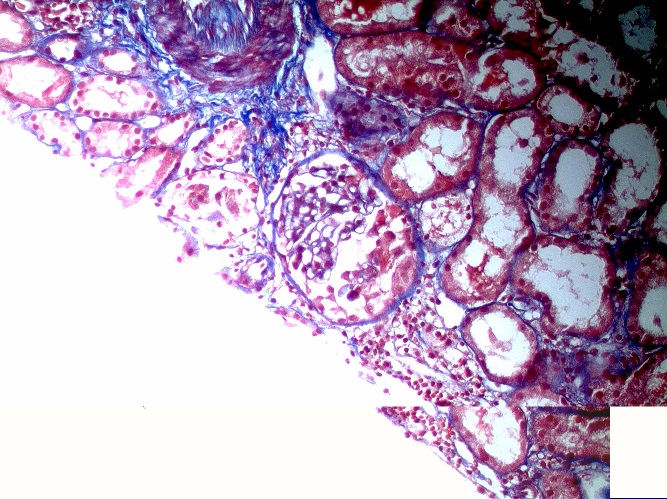
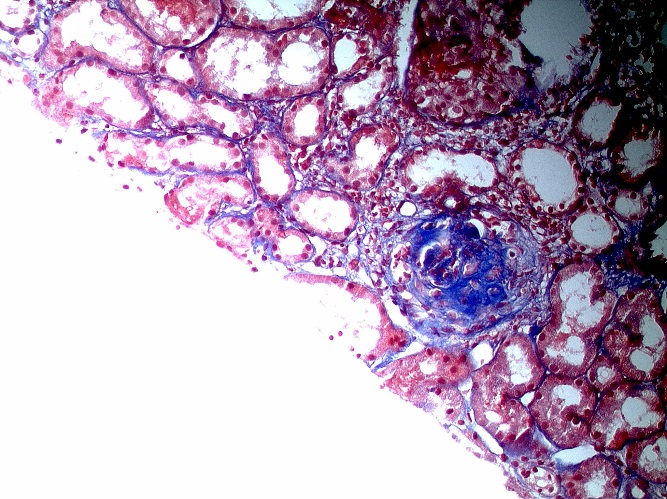
Рисунок 6.3. Трихром по Массону, х200. (Микрофотография – А.Е.Наушабаева, Алматы, 2013 г). А – Некроз петель капилляров клубочков. В – Начало формирования клеточного полулуния. С – Гломерулосклероз в исходе ЭКГН.
Лечение: ЦФ пульсы №6 в течение 6 месяцев, метипреднизолон пульсы №3, в виде таблеток. На этом фоне нарастание креатинина прекратилось, но колебания в пределах 200-170 мкмоль/л, протеинурия снизилась до 1 г/с. Далее продолжено лечение ритуксимабом, сразу после первой инъекции креатинин снизился до 100 мкмоль/л , протеинурия в пределах 0,09 мкмоль/л.
Эозинофильный гранулематоз с полиангиитом (ЭГП) или ранее синдром Чарджа-Штроссапроявляется аллергическим ринитом, астмой и эозинофилией. Поражаются преимущественно сосуды мелкого и среднего калибра. Одинаково часто болеют лица как мужского, так и женского пола, в возрасте 30-50 лет. Причина неизвестна. В начале заболевания отмечается лихорадка, потеря в весе, могут быть миалгии, полиартралгии, кожная сыпь, мононевриты и другие симптомы. Изменения в моче и нарушения функции почек умеренные. В крови характерно наличие эозинофилии, которая снижается на фоне терапии ГКС. Возможно повышение уровня IgE. Повышаются СОЭ, СРБ в крови, ANCA положительны у 45% пациентов. Биопсия тканей свидетельствует о наличии эозинофильного грануломатозного воспаления, иногда может иметь место фокальный сегментарный некротизирующий ГН с эозинофильными инфильтратами и гранулемами в интерстиции.
Лечение. Преднизолон назначается в дозе 1 мг/кг/сут в течение 6-12 мес. При наступлении полной ремиссии ПЗ отменяют и проводится контроль числа эозинофилов в крови, показателей острой фазы воспаления (СОЭ, СРБ). Рецидивы отмечаются у около 25% пациентов при неэффективности терапии ГКС, при этом дополнительно назначается ЦФ.
Дата добавления: 2017-10-04; просмотров: 2573;











