Виды межмолекулярных взаимодействий на границе раздела фаз
Основой адгезионных взаимодействий являются межмолекулярные связи между адгезивом и субстратом, начиная от самых слабых-дисперсионных (физических) до сиьных-химических (ионных, ковалентных, координационных).
Виды связей дифференцируют условно на первичные и вторичные (таблица 2.1). Физические взаимодействия составляют кулоновские, Ван-дер-ваальсовые и силы водородного взаимодействия. Промежуточное состояние между физическими и химическими взаимодействиями занимают комплексные соединения, в которых реализуются донорно-акцепторные и водородные взаимодействия.
Таблица 2.1 – Виды связи и уровень их энергии
| № | Вид связи | Энергия связи, кДж/моль |
| Первичные: | ||
| 1.1 | ионные | 600-1100 |
| 1.2 | ковалентные | 60-700 |
| 1.3 | металлические | 110-350 |
| 1.4 | химические | |
| 1.5 | кислотно-основные | 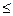 1000 1000
|
| 1.6 | кислотно-основные льюисовского типа | 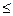 80-100 80-100
|
| Вторичные: | ||
| 2.1 | водородное | 4-7 ккал/моль, может достигать значений 20-30 ккал/моль |
| 2.2 | с участием атомов фтора | 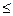 40 40
|
| 2.3 | в отсутствие атомов фтора | 10 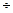 25 25
|
| 2.4 | Ван-дер-ваальсовые | 1-30 кДж/моль. |
| 2.5 | диполь-дипольные взаимодействия | 4-20 |
| 2.6 | индуцированные диполь-дипольные | до 2,0 |
| 2.7 | Дисперсионные (лондоновские) взаимодействия | 0,08-40 |
| 2.8 | Кислота-донор, основание-акцептор атома водорода | |
| 2.9 | Кислота-акцептор, основание-донор электронной шары |
Ван-дер-ваальсовые силы – одна из разновидностей сил притяжения, действующих между атомами и молекулами. Важность этих сил следует из двух уникальных их свойств. Во-первых, эти силы универсальны. Такой механизм притяжения действует между всеми атомами и молекулами. Он ответствен за такие явления, как сцепление атомов инертных газов в твердом и жидком состояниях и физическая адсорбция молекул на поверхности твердых тел, когда отсутствуют химические связи. Во-вторых, эти силы сохраняют значительную величину при сравнительно больших расстояниях между молекулами и отличаются аддитивностью для большого числа молекул. Ван-дер-ваальсовы силы влияют на различные свойства газов. Кроме того, они приводят к возникновению притяжения между двумя твердыми объектами, разделенными малым зазором, что существенно для сцепления и устойчивости коллоидов. Если молекулы находятся на некотором расстоянии друг от друга, теоретические выражения для этих сил особенно просты и к настоящему времени подтверждены экспериментально как для изолированных молекул, так и для двух твердых объектов, разделенных малым зазором.
Межмолекулярные физические взаимодействие – взаимодействие молекул между собой, не приводящее к разрыву или образованию новых химических связей. В их основе, как и в основе химической связи, лежат электрические взаимодействия (6). Ван-дер-ваальсовы силы заметно уступают химическому связыванию. Силы Ван-дер-Ваальса включают все виды межмолекулярного притяжения и отталкивания. Они получили название в честь Я.Д. Ван-дер-Ваальса, который первым принял во внимание межмолекулярные взаимодействия для объяснения свойств реальных газов и жидкостей. Эти силы определяют отличие реальных газов от идеальных, существование жидкостей и молекулярных кристаллов. От них зависят многие структурные, спектральные и другие свойства веществ.
Основу ван-дер-ваальсовых сил составляют кулоновские силы взаимодействия между электронами и ядрами одной молекулы, ядрами и электронами другой. На определенном расстоянии между молекулами силы притяжения и отталкивания уравновешивают друг друга, и образуется устойчивая система.
Полярные молекулы, в которых центры тяжести положительного и отрицательного зарядов не совпадают, например HCl, H2O, NH3, ориентируются таким образом, чтобы рядом находились концы с противоположными зарядами. Между ними возникает притяжение.
Различают ориентационные, индукционные и дисперсионные силы. Ориентационные и индукционные силы возникают при взаимодействии полярных молекул. Дисперсионные силы обусловлены возникновением мгновенных дипольных моментов, вызванных флуктуацией электронной плотности.
Ориентационное взаимодействие.Такой вид межмолекулярного взаимодействияосуществляетсямежду полярными молекулами (диполь–диполь), т.е. молекулами с постоянными дипольными моментами (рисунок 2.2).

Рисунок 2.2. Схемы взаимодействия диполей.
Потенциал взаимодействия (U0) жестко ориентированных диполей является анизотропным, т.е. зависит от ориентации постоянного диполя. Он пропорционален квадратам дипольных моментов и обратно пропорционален температуре и расстоянию между диполями в шестой степени:
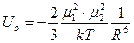 , 2.1
, 2.1
где m1 и m2 – моменты диполей; k – постоянная Больцмана; Т – температура, R – расстояние между диполями.
Притяжение диполей может осуществляться только тогда, когда энергия притяжения превышает тепловую энергию молекул. Обычно это имеет место в твердых и жидких веществах. Диполь-дипольное взаимодействие проявляется в полярных жидкостях (например, вода).
благодаря наличию у молекул свойства поляризуемости γ. Постоянный диполь может индуцировать дипольное распределение зарядов в неполярной молекуле. Под действием заряженных концов полярной молекулы электронные облака неполярных молекул смещаются в сторону положительного заряда и дальше от отрицательного. Неполярная молекула становится полярной, и молекулы начинают притягиваться друг к другу, только намного слабее, чем две полярные молекулы (рисунок 2.3).
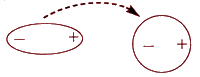
Рисунок 2.3. Схема взаимодействия полярной и неполярной молекул
Энергия взаимодействия наведенных диполей, называемая индукционной или поляризационной определяется по формуле 2.2:
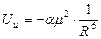 , 2.2
, 2.2
где a – коэффициент поляризации молекул.
Энергия притяжения между постоянным и наведенным диполем (энергия Дебая) определяется выражением:
EД = −2 μнав2 γ / R6, 2.3
где μнав – момент наведенного диполя.
Притяжение постоянного и наведенного диполей обычно очень слабое, поскольку поляризуемость молекул большинства веществ невелика. Оно действует только на очень малых расстояниях между диполями. Этот вид взаимодействия проявляется главным образом в растворах полярных соединений в неполярных растворителях.
то есть неполярная частица станет полярной. Это вызывает перераспределение зарядов в соседних молекулах, и между ними устанавливаются кратковременные связи (рисунок 2.4):

Рисунок 2.4. Схема установления связи между неполярными молекулами
Энергия такого взаимодействия (энергия Лондона) описывается уравнением:
Eд = −2 μмгн2 γ2 / R6, 2.4
где μмгн – момент мгновенного диполя.
Лондоновские силы притяжения между неполярными частицами (атомами, молекулами) являются весьма короткодействующими. Значения энергии такого притяжения зависят от размеров частиц и числа электронов в наведенных диполях. Эти связи очень слабые – самые слабые из всех межмолекулярных взаимодействий. Однако они являются наиболее универсальными, так как возникают между любыми молекулами.
Под воздействием внешнего поля (света) происходит смещение центров тяжести электрических зарядов молекул. Дисперсионное или лондоновское взаимодействие молекул описывается следующей формулой:
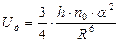 , 2.5
, 2.5
где h·n0 – термический или характеристический квант, который определяется на основе дисперсии света.
Среди перечисленных наиболее сильными, как правило, являются дисперсионные взаимодействия. Для небольших молекул энергия ван-дер-ваальсовых взаимодействий может составлять порядка 1-30 кДж/моль. Ван-дер-ваальсовое взаимодействие имеет место не только между молекулами, но и между нанообъектами, например углеродными нанотрубками. Несмотря на слабость этого взаимодействия, оно обеспечивает устойчивость молекулярных кристаллов, клатратов, супрамолекулярных комплексов, связь молекул с поверхностями (адсорбцию) и играет важную роль в процессах синтеза и построения молекулярных наноструктур.
Межмолекулярное отталкивание. Если бы молекулы только притягивались друг к другу, это привело бы к их слиянию. Но на очень малых расстояниях их электронные оболочки начинают отталкиваться. Энергия отталкивания описывается выражением 2.6:
E = + k / Rn, 2.6
где k – постоянная отталкивания, n принимает различные целые значения (5-15). Силы межмолекулярного отталкивания действуют на очень малых расстояниях.
Общее уравнение межмолекулярного взаимодействия при постоянной температуре (уравнение Леннарда-Джонсона) в большинстве случаев имеет вид
EM = − a / r6 + b/ r12 2.7
и носит название "потенциала 6-12", поскольку энергия притяжения пропорциональна 1 / r6, а энергия отталкивания – 1 / r12.
Силы взаимного притяжения молекул обратно-пропорциональны межмолекулярному расстоянию R6. Эти силы быстро убывают с увеличением расстояния и становятся очень малыми на расстояниях ~5А°. Важная роль во взаимодействиях между молекулами адгезива и субстрата принадлежит водородным связям. Энергия водородной связи, оцениваемая обычно = 4-7 ккал/моль, может достигать значений 20-30 ккал/моль.
Имеется еще один вид межмолекулярного взаимодействия – это поляризационная связь. Частным случаем этого взаимодействия являются связи с переносом заряда, т.е. образованием комплексов между адгезивом и субстратом. В результате переноса зарядов относительно неактивные молекулы могут приобрести реакционную способность. Энергия образования комплексов колеблется от десятых долей до нескольких ккал/моль.
Одним из видов межмолекулярного взаимодействия является донорно-акцепторное взаимодействие, приводящее к образованию комплексов. Различают слабые (с энергией связей ~2 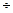 3 ккал/моль) и прочные (с энергией связей до 50 ккал/моль) комплексы, т.е. с энергиями, близкими к ван-дер-ваальсовым и химическим связям.
3 ккал/моль) и прочные (с энергией связей до 50 ккал/моль) комплексы, т.е. с энергиями, близкими к ван-дер-ваальсовым и химическим связям.
Донорами электронов с переносом заряда в органических комплексах являются ароматические углеводороды и некоторые их производные, полимеры с сопряженными связями. В качестве акцепторов выступают галогены, галогеноводороды, хлориды металлов, ангидриды ди- и поликарбоновых кислот, хлорангидриды, нитропроизводные, бензол, хиноны и их производные.
Между молекулами адгезива и субстрата возможно образование и химических связей – ковалентных, ионных, координационных с энергией от нескольких десятков до сотен ккал/моль.
Адгезионная прочности оценивается по сопротивлению разрушения адгезионного соединения. Для упрощения расчета предположим, что разрушение адгезионного соединения происходит путем одновременного нарушения молекулярных связей на определенной площади контакта (по методу нормального отрыва).
Теоретические значения механической прочности выражаются формулой 2.8:
Fm = 1,46·(U/r), 2.8
где U – потенциальная энергия частиц; r – расстояние между частицами.
Прочность композиционного материала зависит от природы материалов, входящих в состав КМ, прочности связи между молекулами адгезива и субстрата на границе раздела фаз.
Дата добавления: 2017-06-13; просмотров: 3382;











