Максимальная и максимально полезная работа
Изменение энтропии определяет направление и предел течения самопроизвольных процессов для изолированных систем, то есть для систем, внутренняя энергия и объем которых постоянны, или для систем, в которых постоянны энтальпия и давление.
Рассмотрим изотермические процессы.
1 Направление и предел течения самопроизвольных процессов для систем, находящихся при постоянных температуре и объеме (T=const.и V=const.), определяет изохорно - изотермический потенциал (изохорный потенциал) или энергия Гельмгольца:
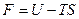 , (25)
, (25)
где U – внутренняя энергия системы, S – энтропия системы, T – абсолютная температура.
Изохорно-изотермический потенциал является функцией состояния, его изменение при переходе системы из состояния 1 в состояние 2 определяется разностью значений в конечном и начальном состояниях 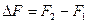 .
.
При переходе из состояния 1 в состояние 2 термодинамическая система выполнит максимальную работу, если этот переход является обратимым процессом.
Согласно первому закону термодинамики 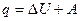 , следовательно, работа
, следовательно, работа 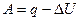 . Согласно второму закону термодинамики из уравнения (19) для обратимого процесса
. Согласно второму закону термодинамики из уравнения (19) для обратимого процесса 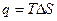 .
.
Следовательно, при переходе из состояния 1 в состояние 2 система совершит работу
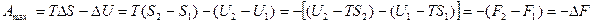 .
.
Функцию Fназывают свободной энергией при постоянном объеме. Свободная энергия – это та часть внутренней энергии процесса, которая может быть полностью превращена в работу. Эту работу ( 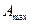 ) называют максимальной работой в изотермическом процессе. Ту часть внутренней энергии, которая не превращается в работу, (
) называют максимальной работой в изотермическом процессе. Ту часть внутренней энергии, которая не превращается в работу, ( 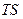 ) называют связанной энергией. С ростом энтропии системы ее связанная энергия возрастает.
) называют связанной энергией. С ростом энтропии системы ее связанная энергия возрастает.
Так как необратимые процессы сопровождаются возрастанием энтропии системы, величина связанной энергии будет увеличиваться, а величина свободной энергии - уменьшаться. Следовательно, процесс протекает самопроизвольно, если ΔF<0. Если ΔF>0, то самопроизвольно процесс протекать не может. Если ΔF=0, то система находится в равновесии.
Таким образом, в системах, находящихся при постоянных температуре и объеме (T=const. и V=const.), самопроизвольно могут протекать только те процессы, которые сопровождаются уменьшением изохорно-изотермического потенциала F.
Причем, пределом их протекания, то есть условием равновесия, является достижение некоторого минимального для данных условий значения функции F, то есть условие
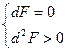 .
.
2 Направление и предел самопроизвольного протекания процесса для систем, находящихся при постоянных давлении и температуре (p=const.и T=const.), определяет изобарно-изотермический потенциал (изобарный потенциал) или энергия Гиббса:
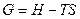 , (26)
, (26)
где Н – внутренняя энергия системы, S – энтропия системы, T – абсолютная температура.
Так как 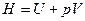 , то
, то 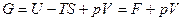 .
.
Изменение изобарно-изотермического потенциала для любого процесса
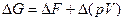 ; (27)
; (27)
для изобарного процесса (p=const.)
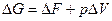 ; (28)
; (28)
для всякого изотермического процесса (T=const.)
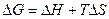 . (29)
. (29)
Максимально полезной работой 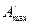 изотермического процесса называют величину
изотермического процесса называют величину
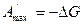 . (30)
. (30)
Так как 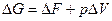 и
и 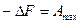 , то
, то
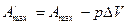 , (31)
, (31)
то есть максимальная полезная работа 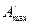 изотермического процесса равна максимальной работе
изотермического процесса равна максимальной работе 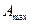 за вычетом работы против внешнего давления.
за вычетом работы против внешнего давления.
Таким образом, в системах, находящихся при постоянных температуре и давлении (T=const. и р=const.), самопроизвольно могут протекать только те процессы, которые сопровождаются уменьшением изобарно-изотермического потенциала G.
Причем, пределом их протекания, то есть условием равновесия, является достижение некоторого минимального для данных условий значения функции G, то есть условие
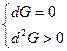 .
.
Если ΔG<0 – процесс протекает самопроизвольно; если ΔG=0– система находится в равновесии.
Процессы, которые сопровождаются увеличением изобарно-изотермического потенциала, происходят лишь по мере получения работы или энергии извне.
Изменение изобарно-изотермического потенциала для химической реакции определяется по уравнению:
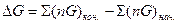 (32)
(32)
Стандартное значение 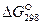 при 298К можно найти в справочных таблицах или рассчитать по уравнению Гиббса-Гельмгольца (26), подставив в него стандартные значения энтальпии и энтропии при 298К:
при 298К можно найти в справочных таблицах или рассчитать по уравнению Гиббса-Гельмгольца (26), подставив в него стандартные значения энтальпии и энтропии при 298К:
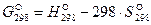 . (33)
. (33)
При анализе металлургических реакций, которые всегда протекают при высоких температурах, используют приближенные методы. Приближенные методы расчета 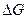 позволяют дать оценку термодинамической вероятности реакции и степени ее удаления от состояния равновесия, а так же сравнить вероятность протекания нескольких реакций, возможных в одной системе.
позволяют дать оценку термодинамической вероятности реакции и степени ее удаления от состояния равновесия, а так же сравнить вероятность протекания нескольких реакций, возможных в одной системе.
Таким образом, для оценки хода любого термодинамического процесса существует определенная характеристическая функция (G, F, U, H, S), изменение которой определяет характер течения данного процесса.
Выбрать функцию, которая является характеристической для процесса, протекающего при двух постоянных термодинамических параметрах, можно из рисунка 5.
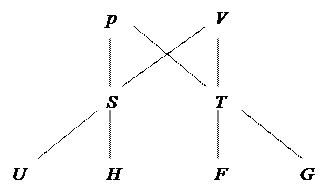
Рис. 5. Схема выбора характеристической функции процесса
При T=const.и V=const. характеристической функцией является изохорно-изотермический потенциал F.
При T=const. и р=const. – изобарно-изотермический потенциал G.
Изобарные процессы (р=const.) характеризует энтальпия Н.
Изохорные (V=const.) – внутренняя энергия U.
Термодинамические процессы (химические реакции) будут протекать в прямом направлении, соответствующем записи уравнения реакции (слева направо), если изменение соответствующей характеристической функции является отрицательным.
Исключение составляют адиабатические процессы (U и V - const. и Н и р - const.), характеристической функцией которых является энтропия S. В этом случае процесс протекает, если изменение энтропии будет положительным (ΔS >0).
Дата добавления: 2017-05-02; просмотров: 2948;











