Изомерия. Номенклатура.
Алканы с n=1,2,3 могут существовать только в виде одного изомера
Начиная с n=4, появляется явление структурной изомерии.

Число структурных изомеров алканов быстро растет с увеличением числа углеродных атомов, например, пентан имеет 3 изомера, гептан - 9 и т.д.
Число изомеров алканов увеличивается и за счет возможных стереоизомеров. Начиная с C7Н16 возможно существование хиральных молекул, которые образуют два энантиомера.
Номенклатура алканов.
Доминирующей номенклатурой является номенклатура IUPAC. В тоже время в ней присутствуют элементы тривиальных названий. Так, первые четыре члена гомологического ряда алканов имеют тривиальные названия.
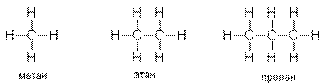
СН4 - метан
С2Н6 - этан
С3Н8 - пропан
С4Н10 - бутан.
Названия остальных гомологов образованы от греческих латинских числительных. Так, для следующих членов ряда нормального (неразветвленного) строения используются названия:
С5Н12 - пентан, С6Н14 - гексан, С7Н18 - гептан,
С8Н18 - октан, С9Н20 - нонан, С10Н22 - декан,
С11Н24 - ундекан, С12Н26 - додекан, С13Н28 - тридекан,
С14Н30 - тетрадекан, С15Н32 - пентадекан и т.д.
Основные правила IUPAC для разветвленных алканов
а) выбирают наиболее длинную неразветвленную цепь, название которой составляет основу (корень). К этой основе прибавляют суффикс “ан”
б) нумеруют эту цепь по принципу наименьших локантов,
в) заместитель указывают в виде префиксов в алфавитном порядке с указанием места нахождения. Если при родоначальной структуре находятся несколько одинаковых заместителей, то их количество указывают греческими числительными.
В зависимости от числа других углеродных атомов, с которыми непосредственно связан рассматриваемый углеродный атом, различают: первичные, вторичные, третичные и четвертичные углеродные атомы.
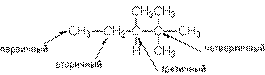
Пример:
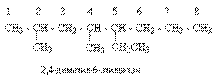
В качестве заместителей в разветвленных алканах фигурируют алкильные группы или алкильные радикалы, которые рассматриваются как результат отщепления от молекулы алкана одного водородного атома.
Название алкильных групп образуют от названия соответствующих алканов путем замены последних суффикса “ан” на суффикс “ил”.
СН3 - метил
СН3СН2 - этил
СН3СН2СН2 - пропил
Для названия разветвленных алкильных групп используют также нумерацию цепи:
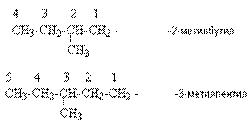
Начиная с этана, алканы способны образовывать конформеры, которым соответствует заторможенная конформация. Возможность перехода одной заторможенной конформации в другую через заслоненную определяется барьером вращения. Определение структуры, состава конформеров и барьеров вращения являются задачами конформационного анализа.
Методы получения алканов.
1. Фракционная перегонка природного газа или бензиновой фракции нефти. Таким способом можно выделять индивидуальные алканы до 11 углеродных атомов.
2. Гидрирование угля. Процесс проводят в присутствии катализаторов (оксиды и сульфиды молибдена, вольфрама, никеля) при 450-470оС и давлениях до 30 Мпа. Уголь и катализатор растирают в порошок и в суспензированном виде гидрируют, борботируя водород через суспензию. Получающиеся смеси алканов и циклоалканов используют в качестве моторного топлива.
3. Гидрирование СО и СО2.
СО + Н2 алканы
СО2 + Н2 алканы
В качестве катализаторов этих реакций используют Со, Fe, и др. d - элементы.
4. Гидрирование алкенов и алкинов.
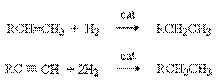
В качестве катализаторов используют Ni, Pt, Pd.
5. Металлоорганический синтез.
а). Синтез Вюрца.
2RHal + 2Na R R + 2NaHal
Этот синтез малопригоден, если в качестве органических реагентов используют два разных галогеналкана.
б). Протолиз реактивов Гриньяра.
R Hal + Mg RMgHal
RMgHal + HOH RH + Mg(OH)Hal
в). Взаимодействие диалкилкупратов лития (LiR2Cu) с алкилгалогенидами
LiR2Cu + R X R R + RCu + LiX
Сами диалкилкупраты лития получают двухстадийным способом
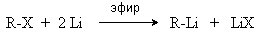
2R Li + CuI LiR2Cu + LiI
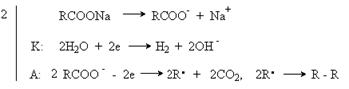
6. Электролиз солей карбоновых кислот (синтез Кольбе).
2RCOONa + 2H2O R R + 2CO2 + 2NaOH + H2
7. Сплавление солей карбоновых кислот со щелочами.
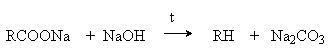
Реакция используется для синтеза низших алканов.
8. Гидрогенолиз карбонильных соединений и галогеналканов.
а). Карбонильные соединения. Синтез Клемменса.
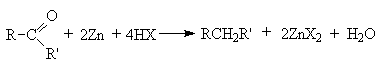
б). Галогеналканы. Каталитический гидрогенолиз.
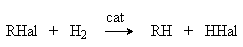
В качестве катализаторов используют Ni, Pt, Pd.
в) Галогеналканы. Реагентное восстановление.
RHal + 2HI RH + HHal + I2
Дата добавления: 2017-04-05; просмотров: 1963;











