Является специфическим маркером РПЖ и позволяет со значительно большей точностью отобрать пациентов для выполнения биопсии простаты.
В анализах крови в зависимости от стадии заболевания выявляются анемия, повышение СОЭ, в моче - гематурия, а с присоединением инфекции - лейко-цитурия, ложная протеинурия. При исследовании эякулята может обнаруживаться большое количество эритроцитов (гемоспермия).
Основными методами визуализации предстательной железы являются различные модификации УЗИ, КТ, МРТ, которые помогают установить окончательный диагноз и стадию заболевания.
Трансректальное УЗИ является стандартным методом диагностики РПЖ. Классический эхографический признак РПЖ - гипоэхогенные участки в периферической зоне простаты(рис. 11.41). Прорастание опухоли в семенные пузырьки и мочевой пузырь определяется в виде нарушения структуры указанных органов (рис. 11.42).
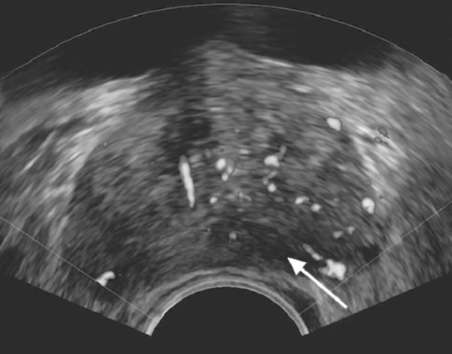
Рис. 11.41.Трансректальная сонограмма. РПЖ (стрелка)
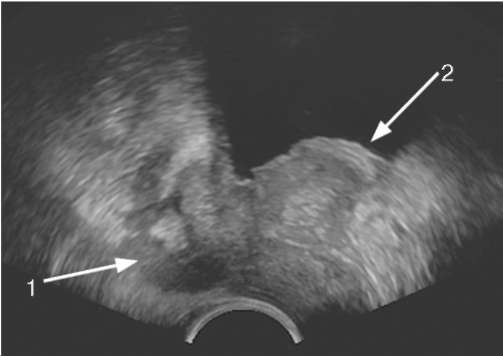
Рис. 11.42.Трансректальная сонограмма. РПЖ с инвазией в семенные пузырьки (1) и стенку мочевого пузыря (2)
По сравнению с ректальным пальцевым исследованием данный метод обладает более высокой чувствительностью и прогностической ценностью. Трехмерная трансректальная сонография с использованием цветовой и усиленной доплерографии в режиме реального времени позволяет получить объемное изображение простаты и оценить ее кровоснабжение (рис. 64, 65, см. цв. вклейку).
КТ недостаточно информативна в ранней диагностике РПЖ, так как ткань неизмененной простаты и опухоли по своей плотности практически не отличаются друг от друга. Ее применяют для выявления регионарных (тазовые лимфоузлы) и отдаленных (кости, легкие) метастазов у пациентов с гистологически подтвержденным РПЖ.
Значение позитронной эмиссионной томографии в ранней диагностике РПЖ до конца не изучено. Из-за низкой метаболической активности злокачественные клетки плохо накапливают изотоп и мало отличаются от неизмененных участков простаты. Метод показал свою эффективность при диагностике регионарных и отдаленных метастазов до и после радикальной простатэктомии.
МРТ за счет различной интенсивности сигнала от мягких тканей таза дает более четкое изображение мочевого пузыря, семенных пузырьков, простаты, прямой кишки и окружающей клетчатки. Именно поэтому она применяется для диагностики ранних стадий РПЖ, а также с целью уточнения локализации и распространенности опухоли (прорастание за пределы простаты, метастазы в регионарные лимфатические узлы и кости). МРТ с эндоректальным датчиком позволяет повысить точность стадирования РПЖ. Одновременная магниторезонансная спектроскопия простаты дает возможность получить изображения, отражающие концентрацию метаболитов в простате (томография по химическим сдвигам).

Рис. 11.43.Трансректальный ультразвуковой датчик (1)
с направляющей насадкой (2) для иглы и биопсийный пистолет (3)

Рис. 11.44.Игла для выполнения биопсии предстательной железы
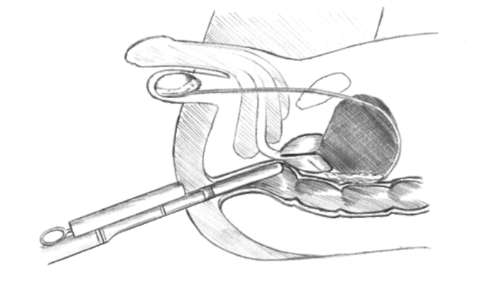
Рис. 11.45.Трансректальная мультифокальная биопсия предстательной железы
Остеосцинтиграфия и рентгенография костей выполняются для выявления костных метастазов у больных с установленным РПЖ.
Окончательно установить диагноз и стадию РПЖ позволяет мультифо-кальная биопсия предстательной железы специальной иглой через прямую кишку под контролем трансректального ультразвукового датчика(рис. 11.43,
11.44, 11.45).
Подготовка к биопсии предстательной железы заключается в про-
филактическом назначении антибактериальных препаратов и очистительной клизмы. Как правило, ее выполняют под местной анестезией (парапростати-ческая блокада 2% раствором лидокаина или введение геля с анестетиком в прямую кишку). Количество вколов и полученного биопсийного материала варьирует от 12 до 14 (рис. 11.46).
При больших объемах предстательной железы или необходимости повторного исследования выполняют сатурационную биопсию, включающую 24 и более вколов. Трансректальная биопсия позволяет установить патоморфологиче-ский диагноз, определить объем, распространенность и степень дифференци-ровки (по шкале Глисона) опухоли. Показаниями к первичной биопсии простаты являются: ПСА более 4 нг/мл, выявление подозрительных участков при пальцевом ректальном исследовании, наличие гипоэхогенных зон при трансректальной соно-графин, скорость прироста ПСА более 0,75 нг/мл в год и время удвоения его менее
12 мес.Повторную биопсию простаты выполняют при простатической инт-раэпителиальной неоплазии высокой степени, отрицательных результатах первичной биопсии, отсутствии снижения ПСА после антибактериальной терапии при хроническом простатите и сохраняющихся показаниях к данному исследованию.
Осложнения трансректальной пунк-ционной биопсии простаты встречаются нечасто. К ним относятся обострение инфекционного процесса в предстательной железе и мочевыводящих путях, повреждение мочеиспускательного канала, мочевого пузыря, семенных пузырьков, проявляющееся болями в промежности, гематурией, гемоспер-мией и в редких случаях образованием парапростатических гематом.
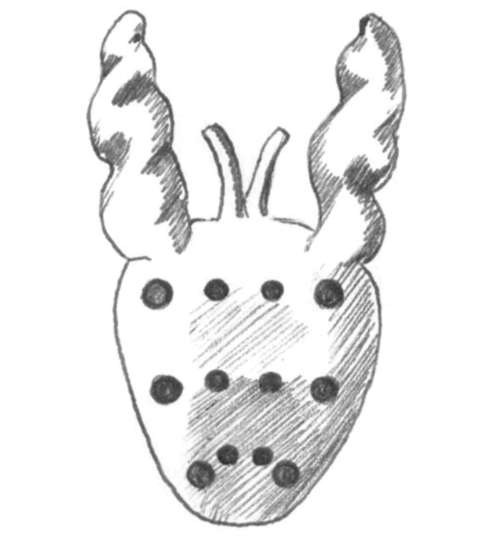
Рис. 11.46.Количество и локализация вколов при биопсии предстательной железы
Лечение РПЖ разделяется на консервативное и оперативное. Консервативная терапия включает назначение медикаментозных препаратов, применение лучевой терапии и малоинвазивных высокотехнологичных методов лечения.
Динамическое наблюдение (отсроченное лечение) оправдано за пожилыми больными при выявлении локализованного (T1-T2b, N0, M0) высокоили умеренно дифференцированного (G≤ 7) РПЖ с высоким риском смерти от сопутствующих заболеваний и ожидаемой продолжительностью жизни менее 10 лет. Опухолеспецифическая выживаемость этих пациентов в течение 10 лет составляет 87 %, а при низкодифференцированных опухолях - 34 %. Активное наблюдение проводится за больными с локализованным РПЖ (T1-T2b, N0, M0) и низким риском прогрессирования (G ≤ 7, ПСА < 10-20 нг/мл). При этом вопрос о радикальном лечении остается открытым. Появление признаков про-грессирования заболевания (удвоение ПСА в сроки от 2 до 4 лет или увеличение G > 7 в период от 1 до 4 лет) делает его целесообразным.
Медикаментозная терапия включает назначение гормональных препаратов. Прием их увеличивает выживаемость и улучшает качество жизни больных. Гормонотерапию, которая направлена на андрогенную депривацию, используют как самостоятельный метод, так и в сочетании с лучевым или оперативным лечением, то есть она является составной частью комбинированного лечения РПЖ.
Андрогенная депривация включает применение: 1) двусторонней орхэктомии; 2) агонистов лютеинизирующего рилизинг-гормона; 3) эстрогенов; 4) антиандроге-нов; 4) максимальной (комбинированной) андрогенной блокады.
Двусторонняя орхэктомия (хирургическая кастрация) - основной способ («золотой стандарт») гормональной депривации при РПЖ. Основными показаниями к ней являются невозможность проведения радикального лечения при локализованной опухоли (Т1-2N0M0); местно-распространенный (T3-4N0M0) и метастатический РПЖ (T1-4N1M0N1-4N0M1). К преимуществам двусторонней орхэктомии относятся быстрое снижение концентрации тестостерона в сыворотке крови (концентрация его падает на 95 % в течение 3-12 ч), простота выполнения и низкая стоимость лечения. Двусторонняя орхэктомия эффективна у 80-85 % больных с первично выявленным гормонально-чувствительным РПЖ. Ее побочные действия и осложнения включают перепады артериального давления, остеопороз, мышечную гипотонию, нарушения липидного обмена, гинекомастию и нервно-психические расстройства.
В качестве медикаментозной терапии назначают агонисты лютеинизирующего рилизинг-гормона - синтетические аналоги нативного гипоталамического лютеинизирующего рилизинг-гормона. После введения этих препаратов отмечается кратковременное повышение концентрации тестостерона на 3-5-й день (синдром вспышки) с последующим снижением ее на 21-28-й день до посткастрационного уровня. Для профилактики синдрома вспышки у больных с метастатическим РПЖ перед введением агониста лютеинизирующего рили-зинг-гормона и в течение первой недели терапии назначают антиандрогены. Показания, побочные эффекты и осложнения данного вида лечения такие же, как при двусторонней орхэктомии. Кроме того, он используется в качестве нео-адъювантной терапии перед радикальным оперативным или лучевым лечени-
ем. Основными агонистами лютеинизирующего рилизинг-гормона являются гозерелин, трипторелин и бусерелин.
Эстрогены были первой группой гормональных препаратов, которые стали применять для лечения РПЖ, однако они обладают выраженными побочными эффектами, наиболее опасным из которых является кардиоваскулярная токсичность. В связи с этим лечение эстрогенами в настоящее время в клинической практике используют редко. Наиболее эффективный препарат этой группы - диэтилстильбэстрол.
Антиандрогены являются конкурентами тестостерона и дегидротестос-терона на уровне рецепторов предстательной железы. Блокируя действие андрогенов, они вызывают апоптоз и угнетают рост опухоли. Различают стероидные (ципротерон - по 100-150 мг/сут или по 250-300 мг/сут внутрь ежедневно, мегестрол, хлормадинон) и нестероидные (флутамид - по 250 мг 3 раза в сутки перорально; нилутамид - по 150 мг 2 раза в сутки перорально в течение 4 нед, в дальнейшем в дозе 150 мг/сут; бикалутамид - по 50 или 150 мг/сут перорально ежедневно) антиадрогены. К их побочным эффектам относятся сердечно-сосудистые осложнения, снижение либидо и потенции, гинекомастия, болезненность грудных желез и гастроинтестинальные расстройства.
Гормональная терапия эффективна у 80-90 % пациентов с РПЖ и позволяет добиваться ремиссии заболевания или стабилизации опухолевого процесса в течение длительного времени. Из средств консервативной терапии РПЖ наибольший эффект оказывает максимальная андрогенная блокада, которая заключается в сочетании хирургической или медикаментозной кастрации с назначением антиандрогенов.
Гормонорефрактерный (резистентный к гормональной терапии) РПЖ развивается в результате потери зависимости опухолевых клеток от уровня тестостерона из-за мутации андрогенных рецепторов, гиперэкспрессии андрогенных рецепторов вследствие амплификации генов, стимуляции рецепторов факторами роста и активаторами протеинкиназы. Такая форма РПЖ плохо поддается лечению и имеет неблагоприятный прогноз. Средняя продолжительность жизни больных не превышает 6-12 мес. Для его лечения применяют различные варианты терапии, направленные на патогенетические механизмы развития гормон-рефрактерности: отмену или замену антиандрогенов, назначение препаратов, блокирующих синтез андрогенов надпочечников (кетоконазол, ами-ноглутатемид), назначение больших доз антиандрогенов (бикалутамид в дозе 150 мг), ингибиторов факторов роста и протеинкиназы. Используют также моно- и полихимиотерапию (эстрамустин, винбластин, этопозид, доцетаксел, цисплатин, доксорубицин) в различных режимах.
Лучевая терапия широко применяется при любых стадиях РПЖ как в качестве самостоятельного метода, так и в сочетании с медикаментозным и оперативным лечением. Цель лучевой терапии - максимально точное достижение терапевтической дозы ионизирующего излучения в ткани предстательной железы при минимальном воздействии на окружающие органы и ткани. Среди существующих методов радиационного лечения лучшим считается трехмерная конформная дистанционная лучевая терапия с модуляцией интенсивности

Рис. 11.47.Промежностная брахитерапия
излучения. Она позволяет максимально увеличить суммарную дозу облучения - до 86 Гр с учетом индивидуальных границ и формы простаты, точно и равномерно распределить ее по всему объему органа. В результате удается существенно уменьшить лучевую нагрузку на мочевой пузырь и прямую кишку и тем самым значительно сократить число осложнений, характерных для стандартной (конвенциальной) дистанционной лучевой терапии. Рецидивом болезни
после проведенной лучевой терапии принято считать три последовательных повышения уровня ПСА после минимального его значения, достигнутого по окончании лучевой терапии.
Промежностная брахитерапия (рис. 11.47), являясь одним из видов лучевой терапии, в то же время открыла эру новых высокотехнологичных и малоинва-зивных методов лечения РПЖ. Она показана при местно локализованном раке простаты и органе небольших размеров. Брахитерапия заключается в имплантации в предстательную железу радиоактивных микроисточников (зерен), что обеспечивает длительное внутритканевое лучевое воздействие на опухоль.
Применяют временную (высокодозную) и постоянную (низкодозную) бра-хитерапию. Для временного введения используют изотоп 192Ir; после подведения необходимой дозы к предстательной железе радиоактивные иглы удаляют. Высокодозную брахитерапию используют при местно-распространенном РПЖ (T3N0M0) в сочетании с дистанционным облучением.
Постоянную брахитерапию применяют при локализованном РПЖ (T1c-Т2a, ПСА < 10 нг/мл, G < 7) и объеме простаты более 50 см3. В предстательную железу вводят радиоактивные зерна (гранулы) 125I, а реже 103Pd. Благодаря более гомогенному распределению ионизирующего излучения брахитерапия позволяет подвести более высокую суммарную очаговую дозу непосредственно к предстательной железе с меньшим лучевым воздействием на окружающие ткани, чем при дистанционной лучевой терапии.
Радиоактивные источники внедряют через промежность под контролем трансректального УЗИ (рис. 11.48) или компьютерного томографа. Обзорная рентгенограмма костей таза позволяет определить количество, локализацию и распределение радиоактивных зерен, имплантированных в предстательную железу (рис. 11.49).
Брахитерапия противопоказана при опухолях с плохим прогнозом сумма баллов по шкале Глисона > 7), объеме предстательной железы более 50 см3. При наличии инфравезикальной обструкции и больших размерах простаты ее проводят с предварительной ТУР большей части объема простаты. У больных с местно-распространенным РПЖ брахитерапию выполняют только в комбинации с дистанционным облучением, при этом радиоактивные источники имплантируют через 2 нед после наружной лучевой терапии.
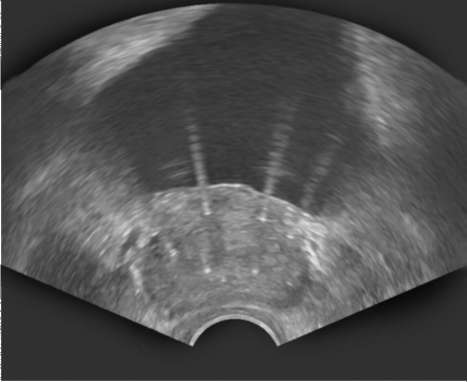
Рис. 11.48.Трансректальная сонограмма после проведения промежностной брахитерапии РПЖ. В ткань предстательной железы имплантированы радиоактивные микроисточники
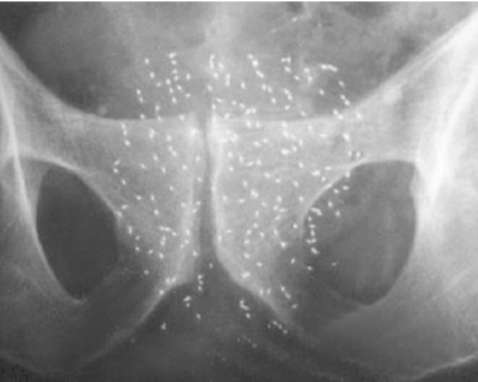
Рис. 11.49.Обзорная рентгенограмма костей таза после проведения промежностной брахитерапии РПЖ. Множественные радиоактивные зерна в предстательной железе
К наиболее частым осложнениям лучевой терапии относятся гематурия, недержание мочи и пострадиационные уретрит, цистит, проктит.
Высокотехнологичным методом лечения РПЖ является высокофокусиро-ванная ультразвуковая аблация предстательной железы (High Intensity Focused Ultrasound - HIFU) (рис. 11.50). Она также используется при локализованном раке с небольшим объемом предстательной железы и является альтернативой брахитерапии и радикальной простатэктомии. Ультразвуковая абла-ция заключается в фокусировании генерируемых эндоректальным датчиком ультразвуковых волн на ткань предстательной железы. При этом происходят локальное повышение температуры (до 100 °С) и некроз клеток в зоне воздействия.
У пациентов с локализованным РПЖ и небольшим ее объемом лучевые методы лечения (брахитерапия) и высокофокусированная ультразвуковая терапия по своим результатам приближаются к радикальной простат-эктомии.
Хирургическое лечение. Радикальное оперативное лечение локализованного РПЖ заключается в удалении единым блоком предстательной железы с семенными пузырьками, простатическим отделом мочеиспускательного канала, парапростатичес-кой жировой клетчаткой, фасциями, а также в расширенной лимфаденэк-томии. Данная операция показана

Рис. 11.50.Лечение пациента с РПЖ сфокусированным ультразвуком на аппарате Ablatherm
пациентам с локализованным РПЖ (T1b-T2N0M0), низким и промежуточным риском прогрессирования (G ≤ 7, ПСА < 20 нг/мл) и ожидаемой продолжительностью жизни более 10 лет. Дискутабельным остается вопрос о ее выполнении с паллиативной целью при локально инвазивном РПЖ (Т3) для удаления основной массы опухоли и повышения эффективности консервативных методов лечения.
В настоящее время в зависимости от доступа и используемого оборудования различают позадилонную, промежностную, лапароскопическую и роботассистированную радикальную простатэктомию. Радикальная про-статэктомия вне зависимости от доступа и объема органа в настоящее время является основным и наиболее эффективным методом лечения локализованного РПЖ. Среди открытых операций наибольшее распространение получила позадилонная простатэктомия, которая в отличие от промежност-ной позволяет достичь лучшей визуализации операционного поля, широко, в пределах здоровых тканей, удалить простату вместе с семенными пузырьками, дистальными отделами семявыносящих протоков, жировой клетчаткой и, что немаловажно, выполнить тазовую лимфодиссекцию. Лучшей модификацией ее является разработанная P. Walsh в 1982 году техника, позволяющая сохранить сосудисто-нервные пучки и тем самым уменьшить кровопотерю, достичь лучшего удержания мочи и сохранить потенцию.
За последние годы в результате внедрения в урологию современного высокотехнологичного оборудования все чаще радикальную простатэктомию стали выполнять лапароскопическим или роботассистированным способом (рис. 70, см. цв. вклейку).
Осложнениями радикальной простатэктомии являются кровотечения, травма прямой кишки, стриктура уретроцистоанастомоза, недержание мочи и эректильная дисфункция.
Прогноз и послеоперационное наблюдение. Прогноз при ранних стадиях опухоли, своевременном и адекватном лечении благоприятный. Пятилетняя безрецидивная выживаемость больных с I-II стадией РПЖ после проведения радикального лечения (радикальной простатэктомии или лучевой терапии) составляет 70-90 %, общая выживаемость - 85-97 %. При выявлении заболевания на стадии метастазирования средний период до прогрессирования процесса на фоне лечения составляет 24-36 месяцев.
Вне зависимости от стадии заболевания и вида лечения за всеми больными РПЖ следует проводить послеоперационное диспансерное наблюдение. Оно предусматривает регулярные, каждые 3 месяца в течение первого года, а в последующем каждые 6 месяцев, посещения врача - уролога-онколога. При каждом визите пациенту проводят пальцевое ректальное исследование, выполняют определение уровня ПСА, клинические, биохимические анализы крови, мочи и сонографию. Повышение уровня ПСА после радикальной про-статэктомии более 0,2 нг/мл требует особой настороженности и более тщательного обследования пациента, так как может свидетельствовать о рецидиве заболевания.
Дата добавления: 2021-06-28; просмотров: 524;











