Доброкачественная гиперплазия (аденома) предстательной железы
В процессе изучения данного заболевания для его обозначения были использованы различные определения: гипертрофия простаты, простатическая болезнь, простатома, гиперплазия простаты и др. В советское время в нашей стране наибольшую распространенность получил термин «аденома предстательной железы», который до сих пор широко используется урологами России. При тщательном патоморфологическом исследовании операционного материала было установлено, что удаленная ткань является не аденомой (доброкачественной опухолью, развивающейся из железистого эпителия), а результатом гиперплазии (пролиферации) железистого эпителия. В связи с этим в нашей стране и за рубежом все чаще данное заболевание называют доброкачественной гиперплазией предстательной железы (ДГПЖ).
Эпидемиология. ДГПЖ является одним из самых распространенных заболеваний у мужчин старше 45 лет во всем мире. В США среди мужчин старше 50 лет она выявляется у каждого третьего, а в России - практически у каждого второго. К 80-летнему возрасту ДГПЖ встречается у 81,4 % мужчин. Симптомы заболевания у 43 % больных начинают появляться в возрасте 60 лет, хотя, по данным аутопсий, патолого-морфологические признаки ДГПЖ уже имеются в 30-летнем возрасте, и к 45 годам ее частота достигает 30 %, а у мужчин старше 60 лет - 70 %. Неуклонный рост заболеваемости ДГПЖ объясняется, прежде всего, увеличением продолжительности жизни мужского населения. Ожидается, что по мере старения популяции распространенность ДГПЖ будет увеличиваться на 2 % в год. В распространенности заболевания существуют расовые различия. Имеются сведения о довольно низком уровне ДГПЖ среди чернокожего населения и, наоборот, более высоком у жителей Юго-Восточной Азии, в частности Китая и Японии. Проведенные исследования не выявили зависимости развития ДГПЖ от сексуальной активности мужчин, курения, групповой принадлежности крови, заболеваний сердца, сахарного диабета, цирроза печени или инфекций органов мочеполовой системы.
Этиология и патогенез. Предстательная железа имеет три основные функциональные зоны: центральную (25 %), периферическую (70 %) и переходную, или транзиторную (5 %). С современной точки зрения суть патологического процесса заключается в формировании множественных пролиферативных центров (узловой гиперплазии) главным образом из эпителиальных и в меньшей степени
из стромальных клеток переходной зоны простаты, а также ацинарных клеток слизистых (парауретральных) желез.По мере увеличения гиперплазированная ткань сдавливает простатический отдел уретры, который удлиняется, меняет угол изгиба, а его просвет приобретает щелевидную форму. В результате развивается инфравезикальная обструкция (или подпузырное сдавливание уретры), препятствующая адекватному опорожнению мочевого пузыря. Увеличивающаяся в размерах доброкачественная опухоль отдавливает к периферии собственную ткань простаты, которая постепенно атрофируется. На границе между ними образуется фиброзный слой ткани, получивший название хирургической капсулы.
К наиболее значимым факторам риска относятся возрастные изменения гормонального статуса, связанные со снижением продукции тестостерона яичками в процессе старения и повышением уровня эстрогенов. Установлено, что у мужчин, кастрированных до достижения половой зрелости, не происходит развития ДГПЖ. В результате гормонального дисбаланса увеличивается выработка стромальными клетками специфических факторов роста, приводящих к нарушению стромально-эпителиального соотношения. В настоящее время развитие гиперплазии простаты объясняется усилением пролиферации и нарушением генетического контроля за естественной гибелью (апоптозом) ее клеток. Большое значение в развитии ДГПЖ играет повышение концентрации и активности фермента 5-α-редуктазы, который существует в виде изофер-ментов I и II типа, локализующихся на наружной мембране клеточного ядра эпителиальных клеток предстательной железы. Под их воздействием тестостерон внутри клетки превращается в дегидротестостерон, превосходящий его по своей активности более чем в 5 раз. Дегидротестостерон связывается с андро-геннымм рецепторами ядра клетки, изменяя ее геном. В результате активизируется синтез белка и стимулируется клеточная пролиферация. Установлено, что при ДГПЖ повышается адренергическая иннервация, что связано исключительно с увеличением плотности гладкой мускулатуры (гипертрофии), а не с высокой активностью α-адренорецепторов. В строме предстательной железы определяется до 98 % α-адренорецепторов, из них 60-85 % представлены селективными α1А-адренорецепторами. В детрузоре сосредоточено около 66 % ат-адренорецепторов. Возбуждение α1А-адренорецепторов сопровождается повышением тонуса гладкомышечных волокон простаты, ее капсулы, шейки мочевого пузыря и задней уретры (динамическая инфравезикальная обструкция). Раздражение α1D-адренорецепторов (афферентых нервов) приводит к гиперчувствительности мочевого пузыря, нарушению функции накопления и появлению частых позывов к мочеиспусканию (поллакиурии). При возбуждении α1B-адренорецепторов возникает спазм сосудов, вызывающий ишемию детру-зора и снижение его сократительной активности. В 60-100 % ДГПЖ сопровождается асептическим воспалением простаты (простатитом), которое приводит к ее отеку и, как следствие, к увеличению степени обструкции уретры, болевому синдрому и дизурии.
Таким образом, основными причинами нарушения мочеиспускания у больных ДГПЖ являются инфравезикальная обструкция и изменения функции детрузора.Инфравезикальная обструкция складывается из двух компонентов:
1) механический (или статический) - возникает за счет сдавливания уретры увеличенной в размерах предстательной железой, вследствие гиперплазии железистой ткани, разрастания фибромускулярной стромы и воспалительного отека;
2) динамический - характеризуется повышением тонуса и спазмом гладко-мышечных волокон простаты, шейки мочевого пузыря и задней уретры.
Функция детрузора нарушается в результате спазма сосудов и ишемии стенки мочевого пузыря, нарушения биоэнергетики мышечных клеток и нейротро-фических изменений, наступающих как в процессе старения, так и на фоне ин-фравезикальной обструкции.
Классификация. Клиническая классификация ДГПЖ подразделяет заболевание на три стадии: компенсации (I стадия), субкомпенсации (II стадия) и декомпенсации (III стадия). Они отражают постепенное нарушение сократительной функции детрузора по мере прогрессирования инфравезикальной обструкции
(рис. 11.30).
I стадия характеризуется компенсаторной гипертрофией детрузора, позволяющей преодолеть уретральное сопротивление и полностью опорожнить мочевой пузырь, поэтому функция верхних мочевых путей и почек не изменяется. Появляются слабовыраженные СНМП. В результате утолщения мышечных пучков при цистоскопии определяется трабекулярность стенки мочевого пузыря (рис. 20, см. цв. вклейку). Во II стадии, субкомпенсации, в процессе постоянной нагрузки на мышечный аппарат мочевого пузыря его сократительный ресурс постепенно истощается и гипертрофия детрузора сменяется гипотрофией. Силы его сокращения не хватает для полного опорожнения мочевого пузыря, и после каждого мочеиспускания в нем определяется нарастающее увеличение количества остаточной мочи (норма менее 50 мл). Наступает хроническая задержка мочеиспускания. При повышении внутрипузырного давления
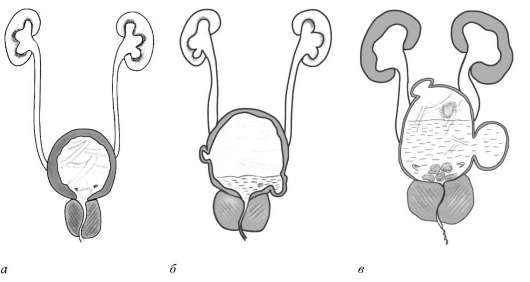
Рис. 11.30.Изменения в мочевыводящих путях по мере прогрессирования инфравезикальной обструкции в результате роста ДГПЖ: а - I стадия; б - II стадия; в - III стадия
нарушается эвакуация мочи из почек, начинается расширение верхних мочевых путей, возникает ПМР. Функция почек снижается, развивается хроническая почечная недостаточность. Стенка мочевого пузыря истончается и выпячивается наружу между мышечными волокнами, образуя ложные дивертикулы (рис. 20, см. цв. вклейку). Постоянный застой мочи создает благоприятные условия для ее инфицирования и камнеобразования.
Без лечения в III стадии наступает декомпенсация детрузора, он истончается и окончательно теряет свои сократительные свойства. Возникает полная задержка мочеиспускания. Нарушение эвакуаторной функции и увеличение количества остаточной мочи (нередко до 1 л и более) приводит к перерастяжению не только детрузора, но и сфинктера мочевого пузыря. В результате моча выделяется из него непроизвольно по каплям, то есть возникает парадоксальная ишурия. Моча двигается по пути наименьшего сопротивления, заполняя верхние мочевые пути и приводя к развитию двустороннего гидро-уретернефроза, обструктивной нефропатии и терминальной почечной недостаточности.
Симптоматика и клиническое течение. Расстройства мочеиспускания, дизурия или симптомы нижних мочевых путей (СНМП) возникают более чем у 50 % пациентов с ДГПЖ, однако не у всех больных с СНМП имеется ДГПЖ. Не существует корреляции между жалобами больного, СНМП и размерами простаты.
СНМП при ДГПЖ делятся на две группы - обструктивные и ирритативные. Обструктивные симптомы связаны с инфравезикальной обструкцией. К ним относятся задержка перед началом мочеиспускания, тонкая и вялая струя мочи, затрудненное мочеиспускание, прерывистое и длительное мочеиспускание, чувство неполного опорожнения мочевого пузыря, задержка мочеиспускания и парадоксальная ишурия. Последняя возникает в результате гипотонии сфинктера мочевого пузыря при длительном его перерастяжении большим количеством остаточной мочи. Таким образом, на фоне хронической задержки мочи происходит ее недержание, в этом и заключается парадоксальность ситуации. Ирритативные симптомы (раздражения) возникают в результате нарушения функции нейромышечного аппарата мочевого пузыря и проявляются в виде императивных (неудержимых) позывов к мочеиспусканию, поллакиурии, нок-турии (более одного мочеиспускания за ночь), учащенного и болезненного мочеиспускания, болей и чувства тяжести над лоном.
Большее клиническое значение имеет направление роста простаты. При внутрипузырном характере роста обструктивные симптомы появляются рано, так как ДГПЖ даже небольших размеров может быстро перекрыть отток мочи из мочевого пузыря. В этих случаях наименее благоприятен интратригональ-ный рост (в сторону мочепузырного треугольника Льето), который приводит к сдавливанию устьев мочеточников и нарушению оттока мочи из верхних мочевых путей. Подпузырный рост (по направлениию к прямой кишке), наоборот, долго может протекать без СНМП, пока ДГПЖ не достигнет значительных размеров.
Частое и опасное осложнение ДГПЖ - острая задержка мочеиспускания, которая может возникнуть в любой стадии заболевания.Она связана с отеком про-
статы вследствие нарушения кровообращения в малом тазу на фоне приема алкоголя, переохлаждения или нарушения функции кишечника (запоров). Этим больным требуется неотложная помощь в виде катетеризации, пункции мочевого пузыря, троакарной или открытой эпицистостомии. Основной фактор риска воспалительных осложнений - нарушение адекватного опорожнения мочевого пузыря. Присоединение инфекции у ослабленных больных может привести к циститу, восходящему пиелонефриту и даже уросепсису. Значительно реже встречаются уретрит и эпидидимит.
Еще одно частое осложнение ДГПЖ - микро- и макрогематурия. Она возникает при повышении венозного давления в сосудах малого таза из варикозно расширенных вен шейки мочевого пузыря и может приводить к его тампонаде сгустками крови.
К другим осложнениям заболевания относятся острая задержка мочеиспускания, камни, дивертикулы мочевого пузыря, хронический цистит, пиелонефрит, гидроуретеронефроз и хроническая почечная недостаточность.
Диагностика ДГПЖ включает:
■ сбор анамнеза, заполнение дневника мочеиспусканий (регистрация суточной частоты и объема мочеиспусканий);
■ физикальное обследование и пальцевое ректальное исследование;
■ выполнение общего анализа мочи;
■ определение креатинина крови для оценки суммарной функции почек;
■ определение уровня ПСА для исключения рака предстательной железы
■ заполнение анкет IPSS (International Prostate Symptom Score, международная суммарная оценка симптомов заболеваний предстательной железы) и QOL (Quality of Life качества жизни) при заболеваниях предстательной железы.
Собирая анамнез, обращают внимание на длительность и динамику СНМП, виды предшествующего лечения, имеющиеся заболевания, вызывающие похожие расстройства мочеиспускания (травмы и патология позвоночника, сахарный диабет, оперативные вмешательства на прямой кишке и др.), соматический статус пациента.
Осмотр позволяет обнаружить, особенно у худых пациентов, выбухающий над лоном, переполненный мочевой пузырь (см. гл. 4, рис. 4.1). Перкуссия и пальпация подтверждают визуальную картину и дают возможность определить наличие остаточной мочи после мочеиспускания. Пальцевое ректальное исследование предстательной железы позволяет оценить ее размеры, болезненность, консистенцию, поверхность, четкость контуров, глубину междолевой борозды. При ДГПЖ простата увеличена в размерах (более 3 см), безболезненна; она эластичная, гладкая, с четкими контурами, междолевая борозда сглажена. Пальцевое ректальное исследование следует в обязательном порядке производить всем больным с подозрением на любое заболевание предстательной железы.Пальпация семенных пузырьков более доступна в положении больного на корточках.
По международной системе суммарной оценки симптомов (IPSS) пациента просят самостоятельно заполнить анкету из семи вопросов, касающихся степени выраженности симптомов нарушения мочеиспускания (табл. 11.1).
Таблица 11.1.Анкета международной суммарной оценки симптомов заболеваний предстательной железы
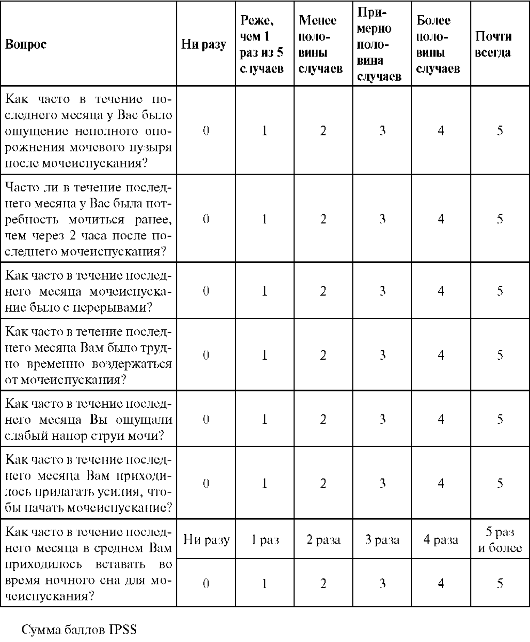
В зависимости от степени выраженности СНМП сумма баллов колеблется от 0 до 35. При сумме баллов от 0 до 7 (легкая степень) лечения не требуется; 8-19 (умеренная степень) показана консервативная терапия; 20-35 (тяжелая степень) показано оперативное лечение.
Для оценки влияния СНМП на качество жизни пациентов разработан опросник QOL (табл. 11.2). Он включает только один вопрос, на который дается семь ответов от «С огорчением» до «Очень хорошо».
Таблица 11.2.Опросник для оценки влияния СНМП на качество жизни пациентов

Таким образом, симптоматический статус пациента оценивается следующим образом: IPSS = (0-35), QOL = (0-6).
Простатический специфический антиген определяют для исключения рака предстательной железы. Его следует обязательно включить в алгоритм обследования мужчин с СНМП.В норме его значение не превышает 4 нг/мл (подробно ПСА будет рассмотрен в главе 11.6.2).
Дальнейшее обследование заключается в выполнении сонографии простаты и мочевого пузыря. Трансабдоминальное УЗИ представляет собой неин-вазивный скрининг-метод, с помощью которого можно определить размеры, структуру органа, кисты и кальцинаты предстательной железы, наличие дивертикулов, камней, опухолей и количество остаточной мочи в мочевом пузыре; выявить расширение мочеточников и лоханок (рис. 11.31).
Более точную информацию о предстательной железе дает УЗИ трансректальным датчиком, позволяющее определить направление роста, истинные границы, размер и объем гиперплазированной ткани простаты(рис. 11.32). Предстательная железа считается увеличенной, если ее размеры превышают 4 см, а объем - более 25 см3.Новые аппараты, работающие в режиме 3D, дают трехмерное послойное изображение органа. С помощью трансректальной доплеровской дуплекс-сонографии выясняют особенности кровотока в простате.
Урофлоуметрия служит основным методом количественной оценки объемной скорости потока мочи. В качестве основных параметров используют максимальную скорость потока мочи Qmax, мл/с и выделенный
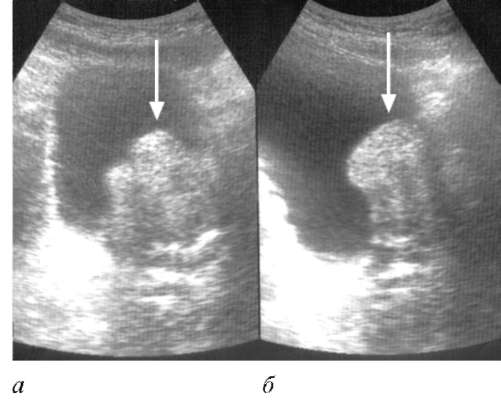
Рис. 11.31.Трансабдоминальная сонограмма во фронтальной (а) и саггитальной (б) проекциях. ДГПЖ с выраженным внутрипузырным ростом (стрелка)
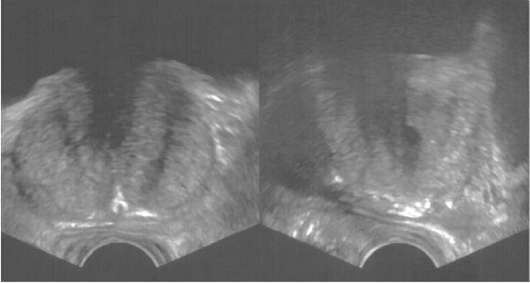
Рис. 11.32.Трансректальная сонограмма. ДГПЖ
объем мочи Vcomp мл. Результаты исследования считаются достоверными, если оно проводилось не менее 2 раз в условиях физиологического наполнения мочевого пузыря до 200-350 мл при появлении естественного позыва к мочеиспусканию. Снижение Qmax до значений менее 15 мл/с свидетельствует об инфравезикальной обструкции или недостаточности сократительной функции детрузора (рис. 11.33).
Для дифференциальной диагностики этих состояний выполняют цисто-метрию (измерение внутрипузырного давления), с помощью которой уточняют истинную причину замедленного мочеиспускания.
Обзорная и экскреторная урография позволяет обнаружить у больных с ДГПЖ вторичные камни в мочевом пузыре, степень нарушения функционального состояния верхних мочевых путей и почек. Гидроуретеронефроз развивается в результате деформации и сдавливания увеличенной и отечной предстательной
железой мочепузырного треугольника и устьев. Это проявляется характерными крючкообразными изгибами предпузырных отделов мочеточников (симптом рыболовных крючков). На нисходящей цистограмме определяется округлый дефект наполнения в области шейки мочевого пузыря (рис. 11.34).
Мультиспиральная КТ и МРТ дают подробное представление о состоянии предстательной железы и расположенных рядом органов, но ввиду достаточной информативности вышеуказанных методов исследования чаще применяются для дифференциальной диагностики заболеваний предстательной железы.

Рис. 11.33.Урофлуограмма при ДГПЖ
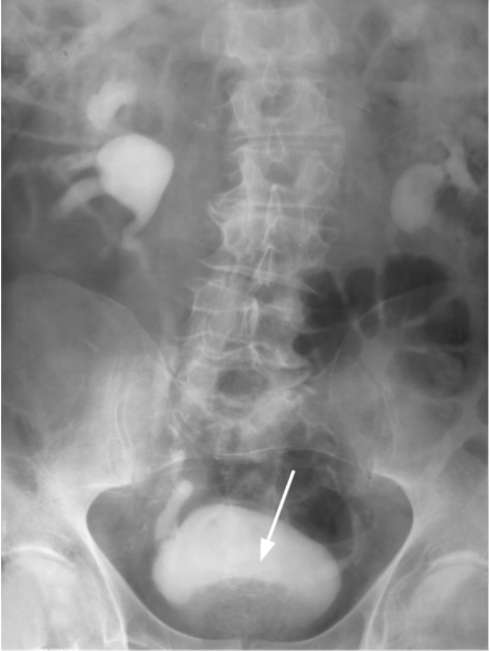
Рис. 11.34.Экскреторная урограмма. Округлый дефект в шейке мочевого пузыря, обусловленный ДГПЖ (стрелка)
Заключительным этапом диагностики, а скорее первым этапом эндоскопического оперативного лечения ДГПЖ является уретроцистоскопия. Она позволяет определить размеры, количество долей гиперплазирован-ной предстательной железы, ход и деформацию мочеиспускательного канала и характерные для нее изменения в мочевом пузыре (трабекуляр-ность стенки, ложные дивертикулы, камни).
Дифференциальная диагностика. ДГПЖ следует отличать от других заболеваний предстательной железы, мочевого пузыря, мочеиспускательного канала и нейрогенных расстройств мочеиспускания, имеющих сходную ирритативную и обструктивную симптоматику. Простатит и воспалительные заболевания нижних мочевых путей (цистит, уретрит) могут проявляться аналогичными расстройствами мочеиспускания. Однако при них,
в отличие от ДГПЖ, отсутствует обструктивная симптоматика. Инфекция мочевых путей всегда сопровождается лейкоцитурией и бактериурией.
Рак предстательной железы часто сочетается с доброкачественной гиперплазией. Однако они развиваются из различных отделов простаты и являются отдельными самостоятельными заболеваниями.При раке предстательная железа также увеличена, но в отличие от ДГПЖ ректальное пальпаторное исследование выявляет плотные бугристые участки. Как правило, при раке отмечаются высокие цифры ПСА (> 4 нг/мл). К сонографическим признакам рака простаты относятся гипоэхогенные участки в периферических зонах предстательной железы. Окончательно установить диагноз позволяет трансректальная мультифо-кальная биопсия простаты.
Сходная обструктивная симптоматика имеет место при сужениях, камнях и опухолях мочеиспускательного канала. Правильно установить диагноз позволяют диагностическое бужирование, ретроградная уретрография и уретроскопия.
Нейрогенные расстройства мочеиспускания характеризуются наличием в анамнезе неврологических заболеваний, соответствующей им симптоматики и отсутствием увеличения предстательной железы. Для дифференциальной диагностики выполняют урофлоуметрию, комплексное уродинамическое исследование, электромиографию и др.
Факторы риска (прогрессирования) ДГПЖ. В настоящее время доказано, что ДГПЖ является медленно прогрессирующим заболеванием. Средний прирост объема простаты у пациентов с ДГПЖ без лечения в течение четырех лет
составляет примерно 15 %, а при ПСА более 1,5 нг/мл достигает 20 %. Согласно рекомендациям Европейской ассоциации урологов и совещания Совета экспертов РФ по лечению ДГПЖ, к доказанным факторам риска прогрессирова-ния заболевания относятся:
■ объем предстательной железы ≥ 30 см3;
■ уровень ПСА ≥ 1,5 нг/мл;
■ наличие СНМП (IPSS > 7 баллов);
■ возраст ≥ 50 лет.
Дополнительными прогностическими критериями считаются скорость потока мочи менее или равная 10-12 мл/с, объем остаточной мочи более 50 мл, эпизоды острой задержки мочеиспускания, хроническая почечная недостаточность, инфекция мочевых путей, неэффективность консервативной терапии. Перечисленные факторы в три раза и более увеличивают вероятность острой задержки мочеиспускания и риск оперативного лечения.
Лечение. Динамическое наблюдение показано только пациентам со слабо-выраженными СНМП, которые мало влияют на качество их жизни. Оно допустимо при IPSS < 7, ПСА < 1,5 нг/мл и объеме предстательной железы менее 30 см3. Больные должны 1 раз в 3 месяца обращаться к урологу и проходить контрольное обследование, так как субъективная оценка пациентом (особенно в пожилом возрасте) СНМП (IPSS и QOL), как правило, не соответствует истинной клинической картине ДГПЖ.
Основными критериями к назначению медикаментозной терапии являются определение риска прогрессировать заболевания и обеспокоенность пациента по поводу появления и нарастания СНМП. Переход от динамического наблюдения к медикаментозному лечению ДГПЖ обоснован при IPSS > 7, ПСА > 1,5 нг/мл и объеме предстательной железы более 30 см3 даже при отсутствии других факторов прогрессирования заболевания.Эффективность медикаментозной терапии при неосложненном течении ДГПЖ составляет до 80 %. В зависимости от сроков медикаментозного лечения ДГПЖ задачи делятся на: 1) краткосрочные - уменьшение СНМП и профилактика острой задержки мочеиспускания; 2) долгосрочные - улучшение уродинамики, предотвращение хирургических вмешательств, осложнений и прогрессирования заболевания; 3) общие - сохранение и улучшение качества жизни, минимизация побочных эффектов лечения.
Лекарственная терапия должна быть направлена на все компоненты инфра-везикальной обструкции:
■ уменьшение размеров предстательной железы (статический компонент обструкции);
■ расслабление гладкомышечных элементов, ее капсулы, шейки мочевого пузыря и задней уретры (динамический компонент);
■ устранение ишемии детрузора (трофический) и снятие отека простаты (воспалительный компонент).
Идеального препарата для лечения ДГПЖ нет, поэтому подбирать терапию надо строго индивидуально с учетом ее эффективности и безопасности.В настоящее время предложено большое количество лекарственных средств для лечения ДГПЖ:
1) α-адреноблокаторы (α-АБ): селективные (α1) - празозин, альфузозин, доксазозин, теразозин и др.; суперселективные (α1А) - тамсулозин;
2) ингибиторы 5-α-редуктазы: синтетические - финастерид, дутастерид; растительные - экстракты Serenoa repens, Pygeum africanum и др.;
3) тканевые препараты - простаты экстракт (раверон, простатилен);
4) полиеновые антибиотики - леворин, ипертрофан;
5) гормоны: аналоги лютеинезирующего рилизинг-гормона - гозерелин (золадекс), бусерелин; антиандрогены - флутамид, бикалутамид (касодекс), ципротерон (андрокур); гестагены - депостат; андрогены, эстрогены, антиэстрогены, ингибиторы ароматазы, антагонисты пролактина;
6) фитопрепараты - экстракты пальмы сабал, уртирон, масло семян тыквы и др.;
7) гомеопатические средства - афала.
Среди большого арсенала лекарственных препаратов только α1-адреноблокаторы и ингибиторы 5-α-редуктазы являются основными средствами медикаментозного лечения ДГПЖ. Их эффективность доказана международными исследованиями и многолетней клинической практикой. Применение α-ад-реноблокаторов приводит к расслаблению гладкомышечных элементов шейки мочевого пузыря и простаты, устранению гипоксии и улучшению энергетического метаболизма в детрузоре. Они представляют собой препараты первой линии лечения больных ДГПЖ при наличии СНМП (IPSS > 8-35), так как: 1) обеспечивают быстрое симптоматическое улучшение (по шкале IPSS) уже на 1-2-й неделе лечения независимо от размеров простаты; 2) эффективны в отношении обструктивных и ирритативных симптомов; 3) не влияют на уровень ПСА; 4) удобны в применении (прием 1 или 2 раза в сутки). Желаемого результата при использовании всех α-адреноблокаторов, за исключением тамсулози-на, можно добиться за счет увеличения дозы и кратности приема препарата.
В клинической практике используют селективные α-адреноблокаторы (теразозин, доксазозин, альфузозин и др.) и суперселективные α1А-адренобло-каторы (тамсулозин). Все селективныеα-адреноблокаторы имеют примерно одинаковую клиническую эффективность и частоту побочных реакций (10-16 %) в виде недомогания, слабости, головокружения, головной боли, ортостатической гипотензии (2-5 %), тахикардии и тахиаритмии.Наименьшими побочными явлениями обладает тамсулозин.
α1-Адреноблокаторы устраняют динамический компонент инфравезикаль-ной обструкции, но не влияют на прогрессирование ДГПЖ. Замедляют рост предстательной железы ингибиторы 5-α-редуктазы II типа - финастерид и ду-тастерид. Аналогичным механизмом действия, но со значительно меньшей эффективностью обладают растительные препараты - экстракты Serenoa repens, Pygeum africanum и др. При длительной, не менее 6-12 мес, терапии ингибиторами 5-α-редуктазы риск прогрессирования ДГПЖ снижается почти на 70 %, так как уменьшаются объем простаты, выраженность СНМП (IPSS), уровень ПСА, вероятность острой задержки мочеиспускания и риск оперативного вмешательства. Среди редких нежелательных явлений терапии следует отметить эректильную дисфункцию, снижение либидо, уменьшение объема эякулята и гинекомастию. Прием ингибиторов 5-α-редуктазы снижает кровоток в простате
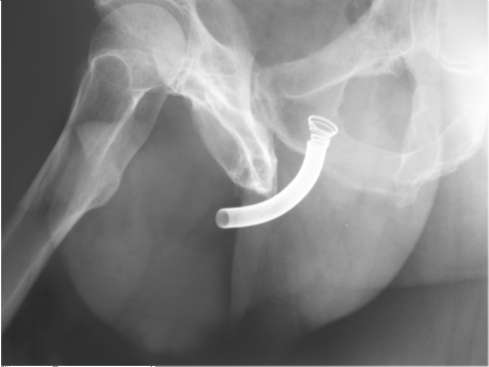
Рис. 11.35.Обзорная рентгенограмма. Спиралевидный металлический эндопротез, установленный больному с ДГПЖ в простатический отдел уретры
и уменьшает гематурию, связанную с самим заболеванием и хирургическими вмешательствами на простате.
Пациентам с ДГПЖ, имеющим СНМП (IPSS >8-35), и с установленным риском прогрессирования заболевания (объем простаты более 30 см, уровень ПСА от 1,5 до 10 нг/мл) показана наиболее эффективная комбинированная терапияα-адреноблокатора-ми и ингибиторами 5-α редуктазы, так как она обеспечивает быстрое симптоматическое улучшение и уменьшение объема предстательной железы.
Остальные лекарственные средства относятся к препаратам второго ряда и применяются в лечении боль-
ных ДГПЖ как вспомогательные средства для уменьшения выраженности симптомов или в комплексной терапии в сочетании с α1-адреноблокаторами и/или ингибиторами 5-α-редуктазы.
Малоинвазивные методы лечения: установка постоянных, временных (съемных) или рассасывающихся стентов (эндопротезов) в простатическом отделе уретры под эндовидеорентгенологическим контролем (рис. 11.35), термальные методы - используются при абсолютных противопоказаниях к хирургическим вмешательствам.
Уретральные стенты препятствуют сдавливанию просвета мочеиспускательного канала гиперплазированной тканью простаты, но имеют высокий риск осложнений, связанный с инкрустацией солями, инфекцией и болевым синдромом.
Многочисленные термальные методы основаны на физическом воздействии на гиперплазированную ткань высоких и низких температур от тепловых, радиочастотных (электромагнитных), лазерных и ультразвуковых источников, установленных в уретре или прямой кишке на уровне простаты. В зависимости от вида и фокуса излучения по мере повышения температуры от 42-45 до 120 °C в ткани гиперплазированной простаты возникают морфологические изменения, характеризующиеся нарушением микроциркуляции, разрушением о -адренорецепторов, подавлением клеточной пролиферации, дистрофией и образованем очагов некроза с их последующим склерозированием.
К неэндоскопическим методам электромагнитного воздействия относятся трансректальная (40-42 °C) и трансуретральная гипертермия (40-45 °C), трансуретральная термотерапия (45-70 °C), термодеструкция или термоаб-лация (70-82 °C). Трансуретральная радиочастотная термотерапия (TUMT) и термодеструкция (TUNA) приводят к образованию очагов коагуляционного некроза в глубине простаты. В отличие от вышеперечисленных методов высокоинтенсивный фокусированный ультразвук (HIFU) с помощью специального трансректального зонда и компьютерной программы наведения позволяет создать локальное повышение температуры до 80-120 °C. В результате деструк-
ция возникает только в заданных точках простаты, не затрагивая окружающие органы и ткани.
Наименее безопасной считается интерстициальная лазерная коагуляция, которая заключается в непосредственном введении в ткань простаты остроконечных световодов, нагревающих ее до 66-100 °C.
Хирургическое лечение.Показаниями к оперативному лечению ДГПЖ являются:
■ отсутствие эффекта от длительной медикаментозной терапии с нарастанием обструктивных и ирритативных симптомов, отрицательно влияющих на повседневную активность пациента;
■ увеличение количества остаточной мочи (более 100 мл);
■ повторяющиеся острые задержки мочеиспускания;
■ рецидивирующая инфекция мочевыводящих путей;
■ камни мочевого пузыря;
■ неоднократная макрогематурия, рефрактерная к терапии ингибиторами 5-а-редуктазы;
■ гидроуретеронефроз и хроническая почечная недостаточность. Оперативное вмешательство не следует выполнять на ранних стадиях ДГПЖ,
Дата добавления: 2021-06-28; просмотров: 620;











