Взаимодействие КВЧ-излучения с биообъектами
Взаимодействие ЭМИ с биологическими объектами приводит к возникновению разнообразных как с количественной, так и с качественной стороны ответных биологических реакций. Результат этого взаимодействия зависит от интенсивности, частоты, времени облучения, поляризации, вида модуляции ЭМИ, величины поглощенной энергии, а также от особенностей самого облучаемого биологического объекта. Само взаимодействие складывается из процессов поглощения энергии падающей электромагнитной волны и характера распределения поглощенной энергии излучения в объекте. Поэтому изучение воздействия ЭМИ целесообразно начинать с оценки общих принципов взаимодействия ЭМИ на уровне организма, и уже далее переходить к рассмотрению отдельных механизмов, проявляющихся на разных уровнях биологической организации. Механизмы взаимодействия обычно рассматривают на более простых уровнях организации: молекулярном, мембранном и клеточном. Биологические макромолекулы.Поскольку биологические макромолекулы - белки и нуклеиновые кислоты в водных растворах несут положительные и отрицательные заряды, они приобретают полярный характер. Полярность таких молекул сохраняется даже при характерных для изоэлектрического состояниявеличинах рН, когда свободный заряд равен нулю. Полярныесвойства белков определяют их высокую диэлектрическую проницаемость в электрических полях низкой частоты. Однако с повышением частоты электрического поля молекулы не успевают следовать за его изменением, и тогда их диэлектрическая проницаемость начинает падать. Причем, чем больше молекула и чем она асимметричнее, тем в более низкочастотной частиэлектромагнитного спектра расположена эта область. Поляризация в растворе макромолекул протекает по нескольким механизмам, основными из которых являются ориентациядиполей и характерная для полиэлектролитов миграция зарядов. Дипольный момент всей макромолекулы складывается из диполей отдельных звеньев по правилу сложения векторов. Дипольные моменты, например, для молекул белков велики и имеют порядок 102–103 Д, что определяется молекулярной массой и длиной диполя. Молекулы белков имеют различные формы и в целях упрощения анализа их поведения в электрическом поле их аппроксимируют простыми моделями—в виде шара, цилиндра или эллипсоида вращения (рис. 6).
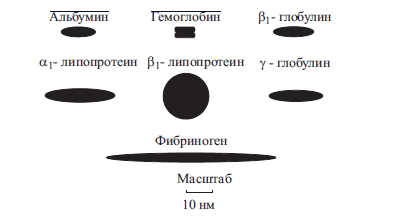
Рис. 6. Аппроксимированные формы молекул некоторых белков сыворотки крови.
Молекулы некоторых белковасимметричны, а их дипольный момент не совпадает с однойиз главных молекулярных осей. Благодаря этому ориентация ивращение такой молекулы в переменном электрическом поле может, в зависимости от частоты, происходить по нескольким осям или их результирующим, следствием чего отмечается нескольковремен релаксации. В простейшем случае у асимметричной молекулы различают два неодинаковых времени релаксации: одно - для поворота вокруг длинной оси, другое - вокруг короткой. Необходимым условием для существования обоих временрелаксации является наличие дипольного момента вдоль обеих молекулярных осей. Поведение больших и малых молекул с различными временами релаксации τМ в переменном электрическом поле в упрощенном виде представлено на рис. 7.
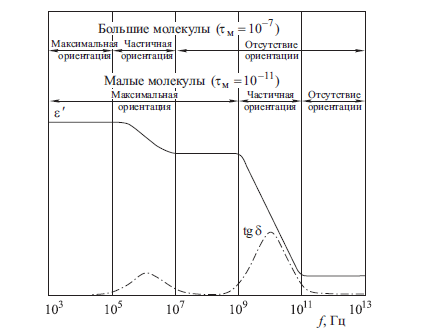
Рис. 7. Схематическое представление частотной зависимости диэлектрической проницаемости и тангенса угла электрических потерь биологических молекул с большими и малыми временами релаксации в диапазоне частот 103–1013 Гц.
Для очень больших молекул ориентация в переменном электрическом поле связана, в основном, с ориентацией сегментовмолекул и их полярных групп. В соответствии со статистическимраспределением полярных групп ориентированные сегменты могут быть любого размера—от одной полярной группы до целой молекулы. Водные растворы биологических макромолекул характеризуются как минимум тремя основными релаксационными областями, где может наблюдаться дисперсия электрических параметров, например, диэлектрической проницаемости (рис. 8). Длямолекул белка, имеющих сферическую форму, возникновениеβ-дисперсии связано с их релаксационным поведением диполей с постоянным дипольным моментом. Появление областей β1- иγ-дисперсий обусловлено присутствием в биологических макромолекулах связанной воды.Молекулы воды, ассоциированной с белком, могут быть подразделены на два типа: внутренние и внешние. К внутренниммолекулам воды относится небольшое число прочно связанныхво внутренней полости белка,которые могут рассматриваться как его неотделимая часть.
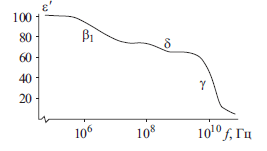
Рис. 8. Частотная зависимость диэлектрической проницаемости водного раствора белка.
Менее прочно связанные и, следовательно, более подвижные внешние молекулы воды распределены по внешней поверхности молекулы белка. К последним относятся молекулы, связанные с заряженными и незаряженными гидрофильными боковымигруппами на поверхности белка, а также более удаленные молекулы воды, которые образуют переходный слой между белком иокружающей его массой воды.Состояние воды в свободной или связанной форме отражается на процессах релаксации биологических макромолекул вовнешнем переменном электрическом поле. Для того чтобы молекула смогла бы свободно вращаться, необходим разрыв водородной связи между макромолекулой и молекулой воды. Для молекул воды, связанных с поверхностью макромолекул, энергиясвязей будет значительно выше, чем водородные связи в жидкой воде, благодаря присутствию сил ион-дипольного взаимодействия. Поэтому молекулы связанной воды испытывают значительное ограничение в своем вращении. Снижение подвижности молекул воды, связанных с гидрофильными группами на поверхности макромолекул, существенно меняет их поведение какдиэлектрика. Поскольку мерой свободы молекулярного вращенияво внешнем электрическом поле является время релаксации, тодля связанной воды по сравнению с молекулами свободной, онобудет больше и находится в пределах 10-8–10-10. В результатеэтого область дисперсии для гидратационной воды, связаннаяс ограничением вращения в переменном электрическом поле,наблюдается в диапазоне частот от 100МГц до 1 ГГц. Релаксация расположенных на поверхности макромолекул противоионов способствует возникновению очень высокой поляризации и обусловливает дисперсию электрических параметровна низких частотах, что характерно для области α-дисперсии.Подобные релаксационные процессы наблюдаются не только удостаточно больших молекул, например, ДНК, но и в мембранах, находящихся в суспензиях клеток и непосредственно в целых тканях. Однако для всей ткани величина релаксации в областичастот α-дисперсии для отдельных молекул белка настольконезначительна, что ею можно пренебречь. Клетки и ткани. Наличие α-, β-, γ- и δ-дисперсий в частотной зависимости электрических свойств клеток и тканейопределяется происходящими в них процессами поляризации,которые включают ряд рассмотренных ранее механизмов: поверхностной, структурной (Масквелла–Вагнера) и дипольной(Дебая) релаксаций. В целях более подробного анализа принято использовать эквивалентные электрические схемы, которые удовлетворительно описывают изменение электрических характеристик биологических объектов в широком диапазоне частот. Наиболее распространенная из таких эквивалентных электрических схем для суспензии клеток, предложенная Шваном, приведена на рис. 9.В этой эквивалентной схеме клеточная мембрана представлена в виде параллельного соединения емкости СМ и электрической проводимости GM и содержит внутреннюю электрическую проводимость клетки Gвнутр и электрическую проводимость межклеточной среды Gвнешн.
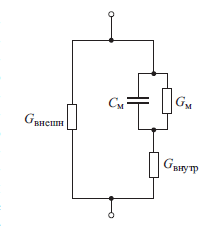
Рис. 9. Эквивалентная электрическая схема суспензии клеток.
Из электрических параметров клеточной суспензии и их частотной зависимости можно извлечь много полезной информации, в частности означениях емкости См, электрической проводимости клеточной мембраны Gм и внутреннего содержимого клетки Gвнутр. На основании подобных измерений Фрике определил значение (См = 0,82 мкФ/см2) и, исходя из представлений о липидной природе клеточной мембраны и приняв для нее диэлектрическую проницаемость равную трем, оценил толщину мембраны равной 3,3 нм. Следует особjотметить, что эти результаты, полученные Фрике еще в 1925 г.,явились первым указанием на молекулярные размеры мембраныживой клетки. Несмотря на выполненные другими методами исследования, результаты Фрике до настоящего времени остаютсяодними из лучших, если не самыми лучшими, которые былиполучены из измерения электрических параметров клеток ещезадолго до применения электронного микроскопа в биологических исследованиях. Согласно современным данным значение См для большинства мембран составляет примерно 1 мкФ/см2 при их толщине около 10 нм. Физический смысл эквивалентной электрической схемы заключается в существовании трех общих путей, по которым переменный электрический ток в зависимости отчастоты проходит через суспензию клеток. Первый путь - через межклеточную жидкость с проводимостью Gвнеш;второй - через межклеточную жидкость к клетке, затемчерез мембрану клетки благодаря ее проводимости Gм, черезвнутриклеточную жидкость с проводимостью Gвнутр сквозьмембрану противоположной стороны и далее снова через межклеточную жидкость, и, наконец, третий - через межклеточнуюжидкость к клетке, затем через мембрану клетки благодаря ееемкостиCм, через внутриклеточную жидкость, сквозь мембранупротивоположной стороны и далее вновь через межклеточнуюжидкость (рис. 10).
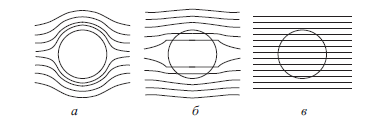
Рис. 10.Схема путей прохождения электрического тока через суспензиюклеток в проводящей жидкости на низких (а), средних (б) и высоких (в) частотах.
Каждый из путей прохождения электрического тока черезсуспензию клеток в зависимости от частоты имеет свою специфику. На низких частотах, вплоть до нескольких единиц килогерц, находящиеся в проводящей жидкости клетки представляютсобой суспензию непроводящих ток шарообразных включений.Поскольку проводимость мембраны очень мала, присутствиев проводящей жидкости непроводящих включений уменьшает электрическую проводимость суспензии пропорционально их
концентрации (рис. 10а). С повышением частоты, начиная с десятков килогерц, мембрана благодаря своей емкости См начинаетпринимать все большее участие в прохождении электрическоготока через внутреннее содержимое клетки (рис. 10б). На болеевысоких частотах, которые для большинства клеток составляютдесятки мегагерц, проводимость мембраны стремится к своему конечному значению (Gм → 0) и уже не оказывает влияния на прохождение электрического тока (рис. 10в). Таким образом, на частотах от десятков до сотен мегагерц электрические свойства суспензии клеток определяются концентрацией вне- и внутриклеточных ионов и их подвижностью. В этой области частот на значение электрической проводимости начинают оказывать влияние релаксационные и электрофоретические силы ионной атмосферы внутриклеточных ионов (эффект Дебая–Фалькенгагена). Дисперсия электрической проводимости суспензии клеток на этих частотах позволяет определить содержание свободных внутриклеточных ионов, которые в отличие отсвязанных, являются причиной возникновения самой дисперсии.
Анализ эквивалентной схемы (см. рис. 9) показывает, что на низких частотах (в области α- и в самом начале β-дисперсии)суммарный потенциал, приложенный к клетке, разряжается через емкость См, а на более высоких—внутри клетки. Клеточнуюмембрану в упрощенном виде можно рассматривать как конденсатор, разделяющий две проводящие фазы, которые в своем составе содержат ионы в различных концентрациях. Подобнолюбому конденсатору, клеточная мембрана обладает емкостью См, величина которой, в зависимости от вида клеток, варьируетв пределах от 0,8 до 1,2 мкФ/см2. Емкость мембраны См в основном определяется образующими бислой липидными полярнымимолекулами, а также и мембранными белками, как внешними,так и интегральными и не зависит от частоты внешнего электрического поля. Напротив, удельная электрическая проводимость мембраны Gм в определенных пределах достаточно вариабельна и находится в интервале значений от 10-7 до 10-4 См/м, поскольку определяется и существенно зависит от проницаемости для ионов.
Таким образом, анализ механизмов взаимодействия ЭМИ РЧ- и МКВ-диапазонов с биологическими объектами (молекулярного, клеточного и тканевого уровней организации) и их электрических свойств в этих диапазонах частот позволяет оценить характер воздействия излучений в различных по сложности биологических структурах.
Дата добавления: 2017-01-08; просмотров: 2728;











