СХЕМА ФАЗОВЫХ ПРЕВРАЩЕНИЙ ОДНОКОМПОНЕНТНЫХ СИСТЕМ
Углеводородные газы, подобно всем индивидуальным веществам, изменяют свой объём при изменении давления и температуры. На рис. 3.1 представлена диаграмма фазового состояния для чистого этана. Каждая из кривых соответствует фазовым изменениям при постоянной температуре и имеет три участка. Слева от пунктирной линии отрезок соответствует газовой фазе, горизонтальный участок – двухфазной газожидкостной области, левый участок – жидкой фазе. Отрезок пунктирной линии вправо от максимума в точке С называется кривой точек конденсации (или точек росы), а влево от максимума – кривой точек парообразования (кипения). В точке С пунктирной линии кривые парообразования и конденсации сливаются. Эта точка называется критической.
С приближением температуры и давления к критическим значениям свойства газовой и жидкой фаз становятся одинаковыми, поверхность раздела между ними исчезает, и плотности их уравниваются. Следовательно, с приближением к критической точке по кривой начала кипения плотность жидкой фазы будет непрерывно убывать. Если же к ней приближаться по линии точек конденсации, то плотность пара будет непрерывно возрастать.
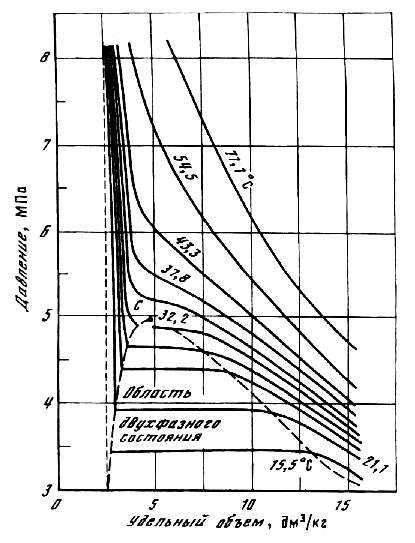
Рис. 3.1. Диаграмма фазового состояния чистого этана.
Для индивидуальных углеводородов граничным давлением между жидкой и газовой фазой является давление упругости паров (при данной температуре), при котором происходит конденсация или испарение. Обе фазы (жидкость и пар) при данной температуре присутствуют в системе только в том случае, если давление равно упругости насыщенного пара над жидкостью. Давление при котором газ начинает конденсироваться называется давлением насыщениядля газа.
Фазовые превращения углеводородов можно также представить в координатах давление-температура (рис. 3.2). Для однокомпонентной системы кривая давления насыщенного пара на графике давление-температура является одновременно кривой точек начала кипения и линией точек росы. При всех других давлениях и температурах вещество находится в однофазном состоянии.
Фазовая диаграмма индивидуальных углеводородов ограничивается критической точкой С (рис. 3.2). Для однокомпонентных систем эта точка определяется наивысшими значениями давления и температуры, при которых ещё могут существовать две фазы одновременно.
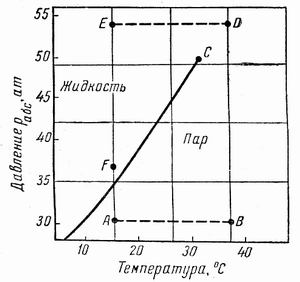
Рис. 3.2. Диаграмма фазового состояния чистого этана в координатах Т-Р.
Из рисунка 3.2 следует, что путём соответствующих изменений давления и температуры углеводороды можно перевести из парообразного состояния в жидкое, минуя двухфазную область. Газ, характеризующийся параметрами точки А (рис. 3.2), можно изобарически нагреть до температуры точки В, а затем, повысив давление в системе при постоянной температуре, перевести вещество в область точки D, расположенную выше критической точки С, и далее в область точки Е. Свойства системы при этом изменяются непрерывно, и разделения углеводорода на фазы не произойдёт. При дальнейшем охлаждении системы (от точки D до точки Е), а затем при снижении давления до точки F вещество приобретёт свойства жидкости, минуя область двухфазного состояния.
Значительно сложнее закономерности фазовых переходов двух- и многокомпонентных систем.
В смеси углеводородов каждый компонент имеет собственные значения упругости насыщенных паров, поэтому процессы конденсации и испарения не будут проходить при конкретных значениях давления и температуры, а в определённом диапазоне значений давления и температуры. Границы диапазона будут тем больше, чем больше разница между критическими значениями давления и температуры индивидуальных компонентов, входящих в систему. Для многокомпонентных систем, в силу их неидеальности, возможны существование двух фаз при температурах или давлениях выше критических величин. Явления существования двух фаз при изотермическом или изобарическом расширении (сжатии) смеси в области выше критических температур и давлений называются ретроградными явлениями или процессами обратного испарения и конденсации. Изотермические ретроградные явления происходят только при температурах выше критической и ниже максимальной двухфазной температуры. Изобарические процессы испарения и конденсации наблюдаются между критическим и максимальным двухфазным давлением. Такие явления характерны, в основном, для газоконденсатных месторождений, имеющих высокие пластовые температуры и давления.
Степень насыщения газоконденсатной залежи высококипящими углеводородами (конденсатом) определяется величиной газоконденсатного фактора. По аналогии с газовым фактором (Го) для нефтяных месторождений (см. разд. 2.1.) понятие газоконденсатный фактор (Ко)применяется для конденсатных залежей и представляет собой отношение количества (дебита) газа в м3 к количеству стабильного конденсата в м3. Величина, обратная газоконденсатному фактору, называется выход конденсата. Нефть и конденсат, полученные непосредственно на промысле при данных температурах и давлениях, называются сырыми.Нефть и конденсат прошедшие процессы дегазации (сепарации), стабилизации при стандартных условиях называются стабильными.
Дата добавления: 2016-12-27; просмотров: 1780;











