Термодинамические функции газа: теплоемкость и энтальпия.
Теплоемкостью С называют количество теплоты, необходимое для нагревания единицы массы или объема вещества на 1° С. Удельная теплоемкость - отношение теплоёмкости к единице количества газа.
Для газов обычно различают теплоемкости при постоянном объеме Сv и постоянном давлении Сp. Сv связана с процессом, характеризующимся тем, что при неизменности объема вся энергия, сообщаемая газу в форме теплоты, затрачивается на увеличение внутренней энергии газа. Сp связана с процессом, характеризующимся тем, что, нагревая тело, предоставляют ему возможность расширяться при неизменном давлении. Таким образом, часть сообщенной телу теплоты идет на производство работы расширения. Поэтому Сp> Сv.
Для идеальных газов между Сp и Сv существует следующее соотношение
Сp = Сv+ R, где R — газовая постоянная.
В области давлений, где газы считаются идеальными, значения теплоемкостей постоянны. Однако для реальных газов значения теплоемкости изменяются в зависимости от давления и температуры.
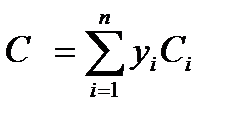 Для смеси газов теплоемкость определяется по сумме теплоемкости входящих компонентов по формуле
Для смеси газов теплоемкость определяется по сумме теплоемкости входящих компонентов по формуле
где Сi— теплоемкости отдельных компонентов смеси; yi – объемное (молярное) содержание компонентов в долях единицы; n – число компонент
Энтальпия — это количество энергии, которая доступна для преобразования в теплоту при определенной температуре и давлении.
Энтальпию часто определяют как полную энергию вещества, так как она равна сумме его внутренней энергии (и) в данном состоянии наряду с его способностью проделать работу (pv). Но в действительности энтальпия не указывает полную энергию вещества при данной температуре выше абсолютного нуля (-273°С). Следовательно, вместо того, чтобы определять энтальпию как полную теплоту вещества, более точно определять ее как общее количество доступной энергии вещества, которое можно преобразовать в теплоту: H = U + pVгде U – внутренняя энергия газа.
10. Дросселирование газа. Коэффициент Джоуля Томсона.
Дросселирование газа — понижение давления в потоке газа при прохождении его через дроссель — местное гидродинамическое сопротивление (диафрагма, клапан, кран, вентиль), сопровождающееся изменением температуры.
Дросселирование используется для сжижения и глубокого охлаждения газов. Последнее осуществляется на установках низкотемпературной сепарации при подготовке газа к дальнему транспорту. Кроме того, дросселирование применяется при трубопроводном транспортировании природного газа — для регулирования давления и изменения расхода газа.
Дросселирование может привести к обмерзанию запорных, регулирующих и измерительных устройств, а также образованию в газопроводах газовых гидратов.
Эффектом Джоуля-Томпсона называется изменение температуры газа при адиабатическом (процесс, при котором система не обменивается тепловой энергией с окружающим пространством) дросселировании — медленном протекании газа под действием постоянного перепада давлений сквозь дроссель (пористую перегородку). Данный эффект является одним из методов получения низких температур.
Изменение температуры при снижении давления на 1атм (0,1Мпа) называется коэффициентом Джоуля - Томсона. Этот коэффициент изменяется в широких пределах и может иметь положительный или отрицательный знак.  Для приблизительных расчетов D можно принять равным 0,3 °С/атм.
Для приблизительных расчетов D можно принять равным 0,3 °С/атм.
Для оценки изменения температуры газа при его дросселировании можно пользоваться специальными графиками. Коэффициент Д-Т рассчитывается и по данным непосредственных замеров температур и давлений до и после дросселирования.
Дата добавления: 2016-12-27; просмотров: 3099;











