Внутренняя энергия произвольной массы газа
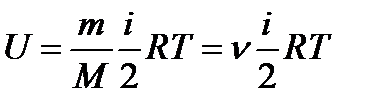 ,
,
m – масса газа; М – молярная масса; 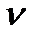 - количество вещества; k - постоянная Больцмана; R–молярная газовая постоянная; NA – постоянная Авогадро; i– число степеней свободы молекулы; Т– термодинамическая температура.
- количество вещества; k - постоянная Больцмана; R–молярная газовая постоянная; NA – постоянная Авогадро; i– число степеней свободы молекулы; Т– термодинамическая температура.
Первое начало термодинамики
Первое начало термодинамики – закон сохранения и превращения энергии применительно к термодинамическим процессам.
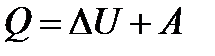
Теплота, сообщаемая системе, расходуется на изменение ее внутренней энергии и на совершение ею работы против внешних сил.
В дифференциальной форме: 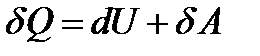
Работа, совершаемая идеальным газом при его расширении
Элементарная работа: 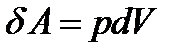
Полная работа при изменении объема от V1до V2
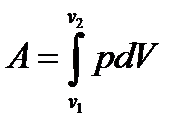
Теплоемкости. Уравнение Майера
· Теплоемкость: 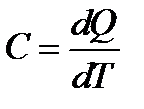 - Величина, определяемая количеством теплоты, которое необходимо сообщить телу (системе), чтобы повысить его температуру на 1К (Дж/К)
- Величина, определяемая количеством теплоты, которое необходимо сообщить телу (системе), чтобы повысить его температуру на 1К (Дж/К)
· Удельная теплоемкость 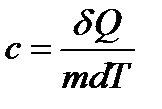 (Дж/кг∙К)
(Дж/кг∙К)
· Молярная теплоемкость 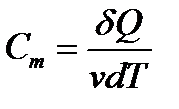 (Дж/моль∙К)
(Дж/моль∙К)
· Связь удельной и молярной теплоемкостей 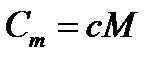 (M - молярная масса; m–масса вещества;
(M - молярная масса; m–масса вещества; 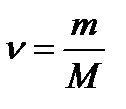 - количество вещества.
- количество вещества.
Дата добавления: 2016-12-16; просмотров: 2316;











