Международная практическая шкала (шкала Цельсия)
Градуируется в градусах Цельсия (0С). Определяется двумя реперными точками: 00С и 1000С – соответственно температуры замерзания и кипения воды при давлении 1,013∙105 Па.
Термодинамическая температурная шкала (шкала Кельвина)
Градуируется в кельвинах (К). Определяется по одной реперной точке, в качестве которой взята тройная точка воды ( температура, при которой лед, вода и насыщенный пар при давлении 609 Па находятся в термодинамическом равновесии). Температура этой точки по данной шкале равна 273,16 К (точно). Температура Т=0 К называется нулем Кельвина.
В термодинамической шкале температура замерзания воды равна 273,15 К (при том же давлении, что и в Международной практической шкале).
Термодинамическая температура (Т) и температура tпо Международной практической шкале связаны соотношением Т =273,15 + t.
Законы, описывающие поведение идеальных газов
Идеальные газы
Свойства:
Собственный объем молекул газа пренебрежительно мал по сравнению с объемом сосуда.
Между молекулами газа отсутствуют силы взаимодействия.
Столкновения молекул газа между собой и со стенками сосуда абсолютно упругие.
Эта модель может быть использована при изучении реальных газов, так как они в условиях, близких к нормальным, а также при низких давлениях и высоких температурах близки по свойствам к идеальному газу.
Основные понятия молекулярно-кинетической теории
Атом– наименьшая часть химического элемента, являющаяся носителем его свойств.
Молекула– наименьшая устойчивая частица вещества, обладающая его основными химическими свойствами и состоящая из атомов, соединенных между собой химическими связями.
Количество вещества– физическая величина, определяемая числом специфических структурных элементов – молекул, атомов и ионов, из которых состоит вещество (единица количества вещества – моль).
Постоянная Авогадро- 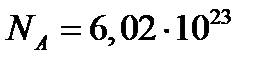 моль-1.
моль-1.
Молярная масса - 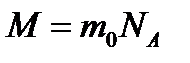 (
( 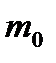 - масса одной молекулы;
- масса одной молекулы; 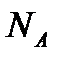 - постоянная Авогадро). Единица молярной массы – 1 кг/моль.
- постоянная Авогадро). Единица молярной массы – 1 кг/моль.
Молярный объем –Vм = ᴠ/ 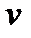 единица молярного объема – 1м3/моль.
единица молярного объема – 1м3/моль.
Дата добавления: 2016-12-16; просмотров: 2509;











