Основы строения и реакционной способности оргаических соединений
ГЛАВА 1. НОМЕНКЛАТУРА И ИЗОМЕРИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ.
Вопросы к занятию.
1. Электронное строение атома углерода (типы гибридизации углеродного атома в органических соединениях).
2. Основные положения теории А.М. Бутлерова.
3. Понятие о гомологических рядах.
4. Классификация органических соединений.
5. Принципы составления названий по номенклатуре для органических соединений.
6. Основные правила номенклатуры ИЮПАК и её использование.
7. Явление изомерии и её основные типы.
8. Пространственное строение органических соединений.
9. Конформации органических молекул и их энергетика. Проекции Ньюмена.
В конце 60-х годов ХIХ в. установлено, что химия органических веществ подчиняется тем же основным закономерностям, что и неорганических. В 1861 г. на съезде немецких естествоиспытателей и врачей в Шпейере выступил А.М. Бутлеров с докладом о новых воззрениях в органической химии. В нем он изложил основные положения теории химического строения, сформулированные им еще в 1858 г. А.М. Бутлеров выдвинул новое понятие – „структура”, которое отражало последовательность расположения атомов в молекуле и связь ее со свойствами веществ.
Теория А.М. Бутлерова была основана на атомистическом учении М.В. Ломоносова и Дж. Дальтона. Дальнейшее развитие органической химии связано с именами А.Е. и Б.А. Арбузовых, А.Н. Белозерского, Н.Д. Зелинского, М.И. Коновалова, М.Г. Кучерова, А.М. Зайцева, В.В. Марковникова, Ю.А. Овчинникова, М.М. Шемякина и др. ученых в России, а также с именами Л. Поллинга, Ф.Х.К. Крика, Дж. Уотсона, Ниренберга, С. Очоа, А. Корнберга, Э. Дж. Кори и многих других зарубежных ученых.
Теория строения органических соединений А.М. Бутлерова.
- Атомы в молекулах веществ соединены согласно их валентности. Углерод в органических соединениях всегда четырехвалентен, а его атомы способны соединяться друг с другом, образуя различные цепи. Последовательность соединения атомов в молекуле называется химическим строением (структурой)
Н Н Н Н Н Н
| \ / \ | /
Н − С − Н Н − С − С − Н Н − С − С −С − Н
| / \ / | \
Н Н Н Н Н Н
метан этан пропан
- Свойства вещества определяются не только их качественным и количественным составом, но и порядком соединения атомов в молекуле, т.е. химическим строением вещества.
Данное положение теории явилось ключом к объяснению явления изомерии: два или более вещества, характеризующиеся одинаковым качественным или количественным составом (и относительной молекулярной массой), но отличающиеся порядком взаимосвязи атомов в молекуле, т.е. строением, и, следовательно, физическими и химическими свойствами, называются изомерами.
Например, формуле С4Н10 отвечают два вещества, структуры которых можно представить:
Н Н Н Н Н Н Н
| | | | | | |
Н − С − С − С − С −Н (I) Н − С − С − С − Н (II)
| | | | | | | изобутан (II)
Н Н Н Н Н | Н (температура кипения -11,7°С)
бутан (I) Н − С − Н
(температура кипения -0,5°С) |
Н
В одном случае атомы углерода образуют неразветвленную цепь (I), а во втором - разветвленную цепь (II). Вещества (I) и (II) имеют различное строение (различный порядок взаимосвязи атомов) и поэтому их свойства тоже будут отличаться друг от друга, т.е. будут изомерами (бутан, изобутан). Явление изомерии – одна из причин многообразия органических веществ (19 млн).
- Свойства органических соединений зависят не только от состава вещества и порядка соединения атомов в его молекуле, но и от взаимного влияния атомов и групп атомов друг на друга.
(Наибольшее влияние оказывают атомы, непосредственно связанные друг с другом. Влияние атомов или групп атомов, не связанных непосредственно, ослабевает по мере их удаления друг от друга.)
Например, влияние углеводородного радикала на подвижность атома водорода в ОН – группе:
а) 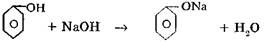 ; б) СН3СН2ОН +NaOH → реакция не идет;
; б) СН3СН2ОН +NaOH → реакция не идет;
а) в феноле R – ароматический - циклический;
б) в этаноле R – ациклический.
Основы строения и реакционной способности оргаических соединений
Дата добавления: 2019-09-30; просмотров: 490;











