Изомерия комплексов
Под изомерией понимают способность веществ образовывать несколько соединений одинакового состава, отличающихся взаимным расположением атомов в молекуле, а следовательно, различных по свойствам. Изомеры – это вещества, имеющие одинаковый химический состав, но разные физико-химические характеристики. Различают структурную и пространственную изомерию. Структурная изомерия обусловлена различным порядком связи атомов в молекуле.
В частности, изомерия комплексных соединений обусловлена различным положением и связью лигандов во внутренней сфере. Так гидратная изомерия имеет место при переходе воды из внутренней сферы во внешнюю, например, [Cr(H2O)6]Cl3, [Cr(H2O)5Cl]Cl2 ∙ H2O, [Cr(H2O)4Cl2]Cl ∙ 2H2O.
Ионизационная изомерия определяется различным распределением ионов между внутренней и внешней сферами, например: [Co(NH3)5Br]SO4 и [Co(NH3)5SO4]Br, [Pt(NH3)4Cl2]Br2 и [Pt(NH3)4Br2]Cl2.
Пространственная изомерия обусловлена различным положением атомов в молекуле относительно друг друга и в пространстве. В частности, в комплексных соединениях наблюдается геометрическая изомерия.
Геометрическая изомерия вызвана неодинаковым размещением лигандов во внутренней сфере относительно друг друга. Необходимым условием геометрической изомерии является наличие во внутренней координационной сфере не менее двух различных лигандов. Геометрическая изомерия проявляется преимущественно у комплексных соединений, имеющих октаэдрическое строение, строение тригональной бипирамиды, плоского квадрата или квадратной пирамиды. Комплексные соединения с тетраэдрическим, треугольным и линейным строением геометрических изомеров не имеют, поскольку места расположения лигандов двух разных видов вокруг центрального атома равноценны.
Для различия геометрических изомеров к названию комплексных соединений добавляют приставку цис- , если одинаковые по составу лиганды занимают соседнее положение по отношению к комплексообразователю, или транс- , когда лиганды находятся в противоположных положениях. Например, комплексный ион дигидроксотетраамминкобальтат может существовать в цис-, так и в транс- форме (Рис.4.1).
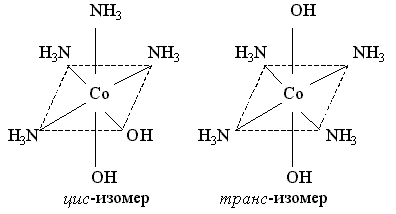
Рис. 4.1. Цис- и транс-изомеры комплексного иона дигидроксотетраамминкобальтата [Co(NH3)4(OH)2]+
Например, дихлородиамминплатина(II) [Pt(NH3)2Cl2]0 имеет два геометрических изомера (квадратные комплексы), в одном одинаковые лиганды расположены в противоположных углах квадрата (транс-изомер), в другом – в соседних углах (цис-изомер):
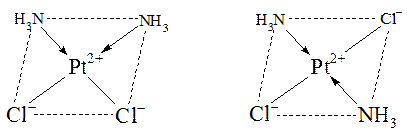
Соответственно названия этих изомеров будут: цис-дихлородиамминплатина(II) и
транс-дихлородиамминплатина(II).
Комплексы (комплексные, координационные соединения) - это молекулы или ионы, обладающие высокой симметрией, имеющие атом в центре симметрии - центральный атом, комплексообразователь, электронная валентность которого больше стехиометрической. Вокруг центрального атома располагаются атомы или группы атомов - лиганды, которые и образуют симметричную фигуру.
Дата добавления: 2021-03-18; просмотров: 855;











