Алканы. Поворотная изомерия, конформации
В молекулах предельных углеводородов и их производных вращение вокруг простых связей не вполне свободно, т.к. молекулы при вращении переходят из одной формы в другую, отличающуюся энергией. Отдельные состояния, через которые проходят молекулы в процессе вращения и отличающиеся расположением заместителей у атомов углерода, связанных простой связью, относительно которой происходит вращение, называются конформациями.
Конформации переходят друг в друга без разрыва химических связей, а
только вращением вокруг простой 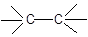 связи и отличаются энергией.
связи и отличаются энергией.
Например, для этана известны две конформации – заторможенная и заслоненная, имеющие энергетический барьер около 3 ккал/моль. Однако выделить их не удается, так как теплового движения достаточно, что бы они могли переходить друг в друга. Изомеры, возникающие при вращении атомных группировок вокруг простой σ-связи, называют поворотными, а изомерия – поворотной, вращательной изомерией. Они представляют одно и то же вещество и имеют одну и ту же структурную формулу.
Заторможенная конформация для этана оказывается более выгодной, вследствие взаимного отталкивания электронных оболочек атомов водорода. При комнатной температуре большинство молекул этана существует в заторможенной конформации.
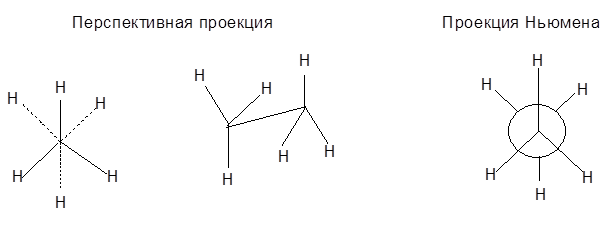
Заторможенная конформация
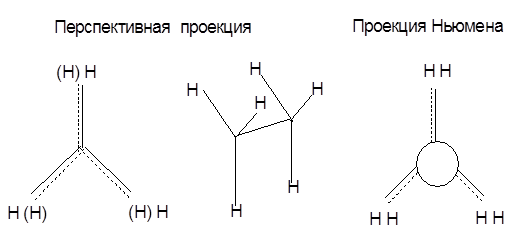
Заслоненная конформация
Для дибромэтана заторможенная форма молекулы выгоднее уже на 19 кДж/моль, а кроме этого появляется еще одна конформация – скошенная конформация.
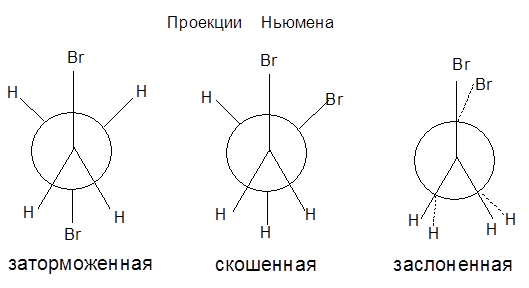
Чем ниже температура, тем меньше энергия теплового движения, тем больше молекул находится в виде более устойчивого поворотного изомера (конформации).
Кривая изменения потенциальной энергии дибромэтана (ДБЭ) при изменении поворота (φ)
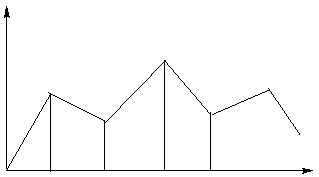
Минимум энергии соответствует заторможенной конформации, т.е. термодинамически наиболее устойчивому поворотному изомеру. Аналогичную кривую можно начертить и для бутана:
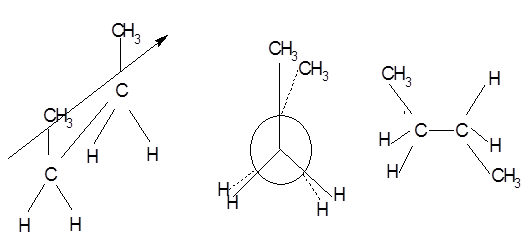
В проекции Ньюмена молекулу рассматривают вдоль С – С-связи, относительно которой происходит вращение. Три линии, расходящиеся под углом 1200 из центра круга, обозначают связи ближайшего к наблюдателю углеродного атома; линии «высовывающиеся» из-за круга – связи удаленного углеродного атома.
Однако уже в пентане надо учитывать вращение вокруг двух «внутренних» связей С – С. По мере усложнения молекул число возможных конформаций возрастает, а графическое изображение их становится сложным.
Дата добавления: 2020-07-18; просмотров: 1382;











