Делеция при болезни Альцгеймера (ДАТ)
Издавна известная особенность болезни Альцгеймера (ДАТ) – это большие семьи с большим количеством заболевших, с распределением через родословное древо по доминантному типу [40; 58]. Схематическое изображение нормальной клетки и клетки, поражённой болезнью Альцгеймера изображено на рисунке 3.5.

Рис. 3.5. Схематическое изображение нормальной нервной клетки (справа) и клетки, поражённой болезнью Альцгеймера.
У пациентов с ДАТ также обнаружены отклонения от нормы в обмене веществ – липопротеинов. Выделяют раннее и позднее начало заболевания. При раннем начале заболевания (моложе 55 лет), благодаря исследованиям генетического сцепления, выявлен каузальный ген конкретно в хромосомах 1, 14, 21. Рано начинающиеся случаи заболевания ДАТ в семье могут быть вызваны мутантными генами.
Известны несколько мутантных генов, которые могут объяснить большую часть семейных случаев болезни ДАТ (моложе 55 лет) [57].
Семейные деменции при болезни Альцгеймера, начинающиеся в более позднем возрасте (после 65-го года жизни), являются комплексными в генетическом отношении расстройствами. Возникновению поздно начинающегося расстройства могут содействовать различные гены. У пациентов с ДАТ чаще других присутствует аллель Аро – Е4, другие два аллеля – Аро – Е2 и Е3 – встречаются реже [21]. У лиц, семейно отягощённых ДАТ, отчётливо наблюдается более высокая частота Аро – Е4, чем при изолированных заболеваниях ДАТ. Кроме того, выявлен ген – доза – эффект (Gen – Dosis - Effect) : носители двух Аро – Е4 – аллелей (гомозиготы) обнаруживали по сравнению со всеми другими генотипами максимальный риск заболевания. Носители только одного аллеля Аро – Е4 показывали повышенный риск по сравнению с лицами одного с ними возраста без аллеля Аро – Е4. Следовательно, Аро – Е4 – не каузальный ген, а ген субцептильности. Другие субцептильные гены для ДАТ в настоящее время не известны [30].
Шизофрения
Уже почти 30 лет проводятся исследования генетического сцепления и ассоциаций с целью обнаружить каузальные или сопутствующие шизофрении гены [25]. Выявлено характерное повышение вторичных случаев болезни у родственников больных шизофренией по сравнению с родственниками здоровых лиц (1-16% против 0-2%) [33;41;43]. В результате реплицируемых исследований генетического сцепления удалось отграничить несколько регионов на геноме, в которых с высокой вероятностью лежат гены, способствующие возникновению шизофрении. Результаты анализа сцепления указывают на возможную вовлечённость 1,5,6,8,10,11,13,15,18 и 22 хромосом. Схематическое изображение хромосомы 6 (отмечены участки, в которых могут быть расположены соответствующие гены) приведено на рис. 3.6.
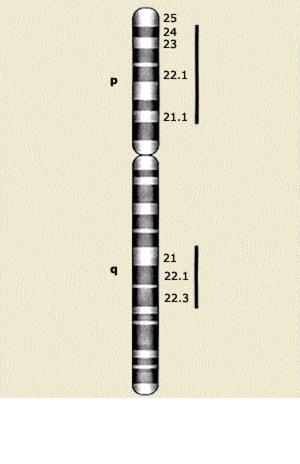
Рис. 3.6Схематическое изображение 6 хромосомы и её областей, имеющих возможное отношение к наследственной детерминации шизофрении (p - короткое плечо, q - длинное плечо хромосомы).
Ни один из этих генов или генных продуктов до сих пор не идентифицирован. Но совершенно очевидно, что каждый из них может объяснить не более10% этиологической вариантности шизофрении [45;48]. Предполагается, что генетическую основу шизофрении образует не один каузальный ген, а несколько неизвестных до настоящего времени генов [36]. Важнейшими задачами на сегодняшний день в области психогенетических исследований шизофрении являются следующие:
· Уточнение генетической классификации шизофрении (выделение частных
нозологических фенотипов для анализа сцепления).
· Изучение нейробиологических дисфункций (эндофенотипов),
сопутствующих шизофрении с целью вовлечения их в анализ сцепления.
· Разработка статистических моделей для изучения мультифакторальной
этиологии и гетерогенной природы шизофрении.
Дата добавления: 2016-12-09; просмотров: 1730;











