Спектр атома водорода по теории Бора. Потенциал ионизации.
Постулаты, выдвинутые Н. Бором, позволили рассчитать спектр атома водорода и водородоподобных систем – систем, состоящихиз ядра с зарядом Ze и одного электрона (например, ионы He+, Li2+, Be3+), а также теоретически вычислить постоянную Ридберга.
Рассмотрим электрон, который движется вокруг ядра по круговой орбите радиуса r. При этом сила кулоновского взаимодействия между ядром и электроном сообщает электрону центростремительное ускорение. Тогда по второму закону Ньютона:
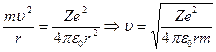
Из первого постулата Бора
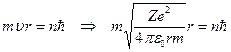 (23.4.1)
(23.4.1)
Из уравнения (23.4.1) следует, что радиус n-й стационарной орбиты:
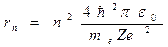 , ,
| (23.4.2) |
где n= 1, 2, 3, ...– номер орбиты
Для атома водорода (Z = 1) радиус первой орбиты электрона при n = 1, называемый первым боровским радиусом (а), равен
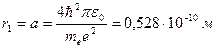
| (23.4.3) |
Полная энергия электрона в водородоподобной системе складывается из его кинетической энергии ( 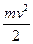 ) и потенциальной энергии в электростатическом поле ядра (
) и потенциальной энергии в электростатическом поле ядра ( 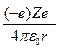 ):
):
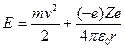
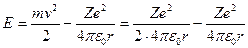
Отсюда следует, что
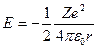
| (23.4.4) |
Подставляя выражение (23.4.3) в (23.4.4) получим, что энергия электрона может принимать только следующие дискретные значения:
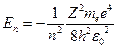 (n=1, 2, 3, 4,...), (n=1, 2, 3, 4,...),
| (23.4.5) |
где знак минус означает, что электрон находится в связанном состоянии.
 |
Целое число п в выражении (23.4.5), определяющее энергетические уровни атома, называетсяглавным квантовым числом. Энергетическое состояние с n = 1 является основным (нормальным) состоянием; состояния с n > 1 являютсявозбужденными. Энергетический уровень, соответствующий основному состоянию атома, называетсяосновным (нормальным) уровнем; все остальные уровни являютсявозбужденными.
Придавая различные значения п, получим для атома водорода различные энергетические уровни представленный на рис.23.2. Энергия атома водорода с увеличением n возрастает и энергетические спектры сближаются к границе, соответствующей значению n=∞. Таким образом, атом водорода обладает минимальной энергией Е1=13,55 эВ при п=1 и максимальной Е∞=0 при n=∞. Значение Е∞=0 соответствует ионизации атома (т.е. отрава от него электрона).
Согласно второму постулату Бора, при переходе атома водорода из стационарного состояния n в стационарное состояние m с меньшей энергией испускается квант:
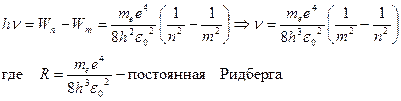
Значение постоянной Ридберга, рассчитанная, таким образом, теоретически полностью совпала с экспериментальными данными. Это совпадение доказывает правильность формулы Бора (энергия, соответствующей различным энергетическим уровням).
Дата добавления: 2016-12-09; просмотров: 2226;











