КИНЕТИКА ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ
1. Влияние концентрации фермента на скорость ферментативной реакции.
2. Влияние концентрации субстрата на скорость ферментативной реакции.
I. Кинетика – наука, изучающая закономерности изменения скорости химических реакций во времени. Кинетической закономерности подчиняются и ферментативные реакции. Особенностью их является образование фермент-субстратного комплекса, насыщение фермента субстратом.
Под скоростью ферментативной реакции понимают активность фермента. Её можно измерить либо по количеству превращаемого субстрата, либо по нарастанию концентрации продукта реакции в единицу времени.
Зависимость скорости ферментативной реакции от концентрации фермента описывается уравнением:
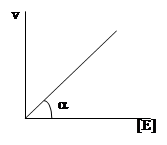 v = k[E],
v = k[E],
где v - скорости ферментативной реакции; k – константа пропорциональности; [E] – концентрация фермента. Величина k зависит от химической природы фермента и субстрата.
Графически это уравнение представляет собой прямую линию. Однако такая зависимость наблюдается только в начальный период реакции, когда концентрация субстрата [S] находится в избытке по отношению к концентрации фермента [E]: [S] >> [E].
|

 [E] + [S] [ES] + P,
[E] + [S] [ES] + P,
где [S] – концентрация субстрата; [ES] – концентрация фермент-субстратного комплекса; k1 – константа скорости образования [ES]; k-1 – константа скорости распада [ES]; Р – продукты реакции.
Обозначим: [E0] – общая концентрация фермента; ([E0] – [ES]) – концентрация свободного фермента. Согласно закону действия масс можно записать:
([E0] – [ES]) × [S] × k1 = [ES] × k-1
Разделив обе части на уравнения на k1, обозначим отношении k-1/k1 = ks. ks – константа диссоциации комплекса ES; она представляет собой обратную величину химического сродства фермента к субстрату: чем < ks, тем > ES.
([E0] – [ES]) × [S] = [ES] × ks
[ES] – величина, трудно определяемая экспериментально, от неё необходимо избавиться:
[E0] [S] - [ES] [S] = ks [ES]
[E0] [S] = [ES] (ks + [S])
[E0]×[S]
[ES] = ---------- (1)
kS + [S]
Следовательно скорость ферментативной реакции в общем случае определяется величиной [ES].
Максимальная скорость реакции (Vmax) будет наблюдаться, когда весь фермент будет участвовать в образовании комплекса ES. Следовательно:
Vmax [ES]
v = ---------- (2)
[E0]
подставив в уравнение (2) значение [ES] (1) получим:

 Vmax [S]
Vmax [S]
v = ----------
KS + [S]
Дата добавления: 2016-12-09; просмотров: 2029;











