ОБЩАЯ ХАРАКТЕРИСТИКА ФЕРМЕНТОВ
I. Ферменты – биологические катализаторы белковой природы, способные во много раз ускорять химические реакции, протекающие ворганизме, но сами не входящие в состав конечных продуктов реакции.
Вещества, на которое действует фермент, называют субстратами.
Все многообразие биохимических реакций, протекающие в микроорганизмах, растениях и животных катализируется соответствующими ферментами. Велика роль ферментов в технологии пищевых продуктов. В основе производства любого пищевого продукта лежат либо биохимические (ферментативные), либо физико-химические процессы, либо эти процессы взаимосвязаны.
В отличие от неорганических катализаторов ферменты имеют свои особенности:
Ø Скорость ферментативного катализа на несколько порядков выше (от 103 до 109), чем не биологического катализатора;
Ø действие каждого фермента высокоспецифично, т.е. каждый фермент действует только на свой субстрат или группу родственных субстратов;
Ø ферменты катализируют химические реакции в мягких условиях, т.е. при обычном давлении, высокой температуре (20-50°С) и при значениях рН среды, в большинстве случаев близких к нейтральной.
С точки зрения локализации ферментов в клетке их подразделяют на внеклеточные и внутриклеточные.
Внеклеточные ферменты выделяются живой клеткой во внешнюю среду, внутриклеточные – находятся либо в клеточных органеллах, либо в комплексе с надмолекулярными структурами.
Особую группу ферментов составляют полиферментные комплексы, в состав которых входит ряд ферментов, катализирующих последовательные реакции превращения какого-либо субстрата. Эти комплексы локализованы во внутримолекулярных структурах таким образом, что каждый фермент располагается в непосредственной близости от фермента, катализирующего реакцию в цепи данной последовательности реакций. Благодаря такому расположению ферментов процесс диффузии субстрата и продуктов реакции сводится к минимуму.
II. Ферменты – высокомолекулярные белковые соединения.
Как и другие белки, ферменты имеют 4 уровня структуры, им присущи все физико-химические свойства белков, и лишь одна отличительная особенность – способность ускорять химические реакции. Ферменты могут быть простыми – однокомпонентными и сложными двухкомпонентными.
Однокомпонентные ферменты – построены из полипептидных цепей и при гидролизе распадаются только до аминокислот.
Двухкомпонентные ферменты – состоят из белковой части – апоформента и небелковой части – кофактора. Оба компонента в отдельности лишены ферментативной активности. Только соединившись вместе (холофермент) они приобретают свойства, характерные для биокатализаторов. Роль кофактора может выполнять какой-либо ион (Zn2+, Mg2+, Fe2+, Cu2+, реже K+ и Na+) или органическое соединение (витамины, нуклеотиды). Кофакторы органической природы называются коферментами.
Тип связи между кофактором и апоферментом может быть различным. В некоторых случаях они существуют отдельно и связываются только во время протекания реакции; в других случаях кофактор и апофермент связаны постоянно, иногда прочными, ковалентными связями.
Активный центр ферментов–это локальный участок молекулы фермента, который участвует в акте катализа. В однокомпонентных ферментахактивный центр образуется в результате определенной ориентации аминокислотных остатков полипептидной цепи. Обычно в его формировании принимает участие небольшое количество аминокислот, в пределах 12-16. Функциональные группы этих аминокислот могут принадлежать звеньям полипептидной цепи, удаленным друг от друга. Их сближение связано с формированием третичной структуры ферменты.
В двухкомпонентных ферментах активный центр представляет собой комплекс кофактора и некоторых примыкающих к нему аминокислотных остатков.
В активном центре различают контактный (якорный) участок, функция которого – связывать субстрат, и каталитический – где происходит превращение субстрата в продукты реакции после его связывания контактным участком. В формировании этих участков принимают участие следующие функциональные группы: СООН-группы дикарбоновых аминокислот или концевые группы полипептидной цепи; имидазольная группа гистидина; ОН-группа серина; NH2- группа лизин и концевые группы полипептидной цепи; фенольная группа тирозина и гидрофобные остатки алифатических аминокислот.
III. Скорость любой ферментативной реакции определяется энергетическим барьером, который необходимо преодолеть реагирующим молекулам. По Аррениусу, химическая реакция с точки зрения энергетики процесса описывается уравнением
N = N0e-(Eакт/RT),
где N – число активных молекул; N0 - общее число реагирующих молекул; е – основание натурального логарифма; R – газовая постоянная; T – абсолютная температура; Еакт – энергия активации.
 Энергия активации – дополнительное количество энергии, необходимое для того, чтобы все молекулы преодолели энергетический барьер реакции и вступили в неё. Эта энергия представляет собой разность общей энергии реагирующих молекул и энергии возбужденного переходного состояния. Чем больше энергия активации в реагирующей системе, тем выше энергетический барьер и тем ниже скорость реакции.
Энергия активации – дополнительное количество энергии, необходимое для того, чтобы все молекулы преодолели энергетический барьер реакции и вступили в неё. Эта энергия представляет собой разность общей энергии реагирующих молекул и энергии возбужденного переходного состояния. Чем больше энергия активации в реагирующей системе, тем выше энергетический барьер и тем ниже скорость реакции.
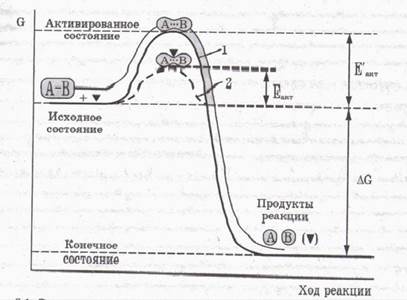
Важнейшая функция фермента – снижение энергии активации катализируемого процесса. На рис. 1 представлен график изменения энергии неферментативной (1) и ферментативной (2) реакций. Фермент снижает высоту энергетического барьера (Еакт < Е¢акт).
Механизм ферментативного катализа во многом остается пока еще не выясненным. Однако большую роль в создании ферментативной кинетики сыграли работы М. Михаэлиса и М. Ментен, в которых было развито представление о фермент-субстратном комплексе. Образование этого комплекса и ведет к снижению энергии активации реакции.
Процесс ферментативного катализа можно условно подразделить на три стадии:
1. Стерическое связывание субстрата S с активным центром фермента Е (образование фермент-субстратного комплекса ЕS).
2. Преобразование первичного комплекса ЕS в активированный
переходный комплекс ЕS≠.
3. Отделение конечного продукта Р реакции от фермента.
Первая стадия непродолжительна по времени и зависит от концентрации субстрата и фермента в среде, от скорости диффузии субстрата к активному центру фермента. В образовании комплекса ЕS могут участвовать в различных сочетаниях как ковалентные, координационные, ионные связи, так и менее прочные формы связей — электростатическое притяжение полярных групп, ван-дер-ваальсовы силы сцепления между неполярными участками молекул, водородные связи. Характер этих связей обусловлен химическими особенностями и субстрата, и функциональных групп, входящих в активный центр фермента.
Вторая стадия является, собственно, актом катализа, т.е. актом разрыва или образования в субстрате новых связей; она наиболее медленная и лимитирует скорость протекания химической реакции. На этой стадии и происходит снижение энергии активации ферментативной реакции, за счет образования активного переходного комплекса ЕS≠.
На молекулярном уровне более четкое представление о механизме действия ферментов дает теория кислотно-основного катализа.Любая реакция, идущая с разрывом ковалентных связей, предполагает участие двух противоположных по характеру электронных компонентов. Электроны разрываемой связи должны оттягиваться к электро-фильному компоненту и уходить от нуклеофильного. Реагенты, которые могли бы обусловить такую электронную перестройку — это кислота и основание. Однако в одном и том же растворе создать одновременно высокие концентрации обоих компонентов невозможно, поскольку они нейтрализуют друг друга. В белковой молекуле фермента благодаря закреплению на каталитической площадке электрофильных и нуклеофильных групп не происходит прямой реакции нейтрализации. Это, собственно, и определяет акт катализа. Находясь на определенном расстоянии друг от друга, электрофильные и нуклеофильные группы каталитического участка фермента не только связываются с реагирующими группами субстрата, но и оказывают сильное поляризующее действие на группы субстрата. К этому следует добавить возможность флуктуации зарядов в комплексе ЕS, которая создает высокую степень эффективности данной поляризации. Это и является причиной снижения величины энергии активации при ферментативном катализе.
В соответствии с теорией ковалентного катализа некоторые ферменты взаимодействуют со своими субстратами, образуя нестабильные, ковалентно связанные фермент-субстратные комплексы. Из этих комплексов в ходе последующей реакции образуются продукты реакции, причем значительно быстрее, чем в случае некатализируемых реакций.
Таким образом, третья стадия, завершающаяся образованием продуктов реакции, обеспечивается процессами, протекающими на предыдущих стадиях.
Дата добавления: 2016-12-09; просмотров: 6198;











