Кристаллическая структура твердых тел
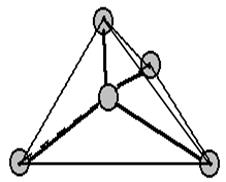 Рис. 1.7.Элементарнаякри-сталлическаяячейка алмаза Рис. 1.7.Элементарнаякри-сталлическаяячейка алмаза
|
В кристалле ионы находятся в потенциальных ямах (см. рис. 1.2) и расположены упорядоченно. Упорядоченное расположение атомов принято называть кристаллической решеткой. Для описания кристал-лических решеток удобно воспользоваться понятием элементарной ячейки кристалла - минимального объема кристалла, полностью отражающего его геометрические свойст-ва. При трансляции (параллельном пере-мещении) элементарной ячейки можно за-полнить сколь угодно большой кристалл.
У элементов четвертой группы ковалентная насыщенная и направленная связь, и у каждого атома четыре соседа. Число ближайших соседей принято называть координационным числом K. Элементарную решетку можно представить в виде тетраэдра с одним атомом в центре и четырьмя атомами по вершинам тетраэдра. Кристаллическую решетку с такой элементарной ячейкой имеют элементарный кремний, германий, углерод в модификации алмаза. Этот тип кристаллической решетки принято называть решеткой алмаза (рис. 1.7).
Кристаллические решетки с ионной связью более компактны, координационное число K достигает 6. Это связано с тем, что ионная связь не насыщенна, хотя и направленна. Типичным представителем веществ с таким видом связи является поваренная соль, соединение NaCl. Ее кристаллическую решетку можно представить в виде примитивного куба, в вершинах которого расположены ионы хлора и натрия. Элементарная ячейка показана на рис. 1.8.
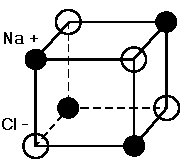 Рис. 1.8. Элементарная кристаллическая
ячейка NaCl
Рис. 1.8. Элементарная кристаллическая
ячейка NaCl
|
При образовании металлической связи кристаллические решетки становятся еще более компактными. Координационные числа K достигают значений 8 и 12. В металлических материалах, как правило, формируются три типа кристаллических решеток: объемноцентрированная кубическая (ОЦК), гранецентрированная кубическая (ГЦК) и гексагональная плотноупакованная (ГПУ). Они показаны на рис. 1.9.
 а б в
Рис. 1.9. Элементарные ячейки кристаллических решеток металлов:
а – ОЦК, б – ГЦК, в – ГПУ
а б в
Рис. 1.9. Элементарные ячейки кристаллических решеток металлов:
а – ОЦК, б – ГЦК, в – ГПУ
|
ОЦК решетку имеют такие металлы, как вольфрам, молибден, ниобий, щелочные металлы, низкотемпературные модификации железа, высокотемпературная модификация титана. Серебро, медь, алюминий, никель, высокотемпературная модификация железа имеют ГЦК решетку. ГПУ решетка у магния, цинка, кадмия, титана.
Плотность кристаллической решетки (объем, занятый атомами) удобно характеризовать также коэффициентом заполнения Z, т.е. отношением объема, занимаемого атомами, ко всему объему кристалла, обычно выраженным в процентах. Очевидно, чем выше координационное число K , тем больше плотность упаковки атомов и соответственно коэффициент заполнения кристаллической ячейкиZ. Нетрудно вычислить эти параметры для разных типов кристаллических решеток, результаты приведены в табл. 1.3.
Таблица 1.3
| Тип решетки | Алмаз | Простая кубическая | ОЦК | ГЦК | ГПУ |
| К | |||||
| Z, % |
Металлы с плотноупакованной решеткой, как правило, обладают лучшей проводимостью, чем металлы с менее плотноупакованной решеткой. Это связано с тем, что у металлов с плотноупакованной решеткой повышена плотность электронного газа, а следовательно, повышена концентрация основных носителей заряда – свободных электронов.
Дата добавления: 2016-11-04; просмотров: 2136;











