Влияние катализатора
Скорость химической реакции может резко измениться в присутствии катализатора.
Катализатором называют вещество, участвующее в реакции и увеличивающее ее скорость, но остающееся химически неизменным в результате реакции.
Влияние катализатора на скорость химической реакции в основном заключается в его участии в этой реакции и изменении ее механизма. Катализатор (Кат) образует с реагентами промежуточные, реакционноспособные соединения, которые в дальнейшем превращаются в продукты реакции и свободный катализатор:
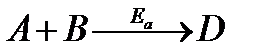
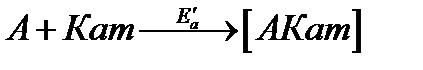
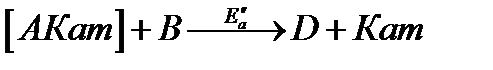
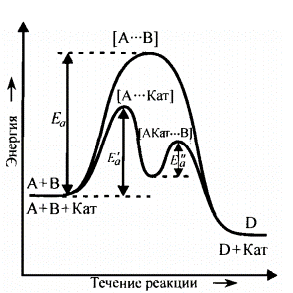
Энергетический профиль реакции без катализатора и с катализатором
Таким образом, в присутствии катализатора изменяется механизм реакции, и она направляется по пути с меньшими значениями энергии активации каждой стадии ( 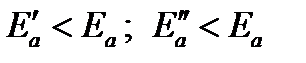 ), что и приводит к возрастанию скорости реакции. Кроме того, катализатор может способствовать определенной ориентации молекул в пространстве, удобной для данного химического взаимодействия, и влиять на энтропию переходного состояния, способствуя ее возрастанию.
), что и приводит к возрастанию скорости реакции. Кроме того, катализатор может способствовать определенной ориентации молекул в пространстве, удобной для данного химического взаимодействия, и влиять на энтропию переходного состояния, способствуя ее возрастанию.
На скорость реакции в ряде случаев также влияет присутствие в системе ингибитора. В отличие от катализатора, ингибитор уменьшает скорость реакции. Механизм его действия не связан с повышением энергии активации. Ингибиторы просто препятствуют обычному течению химической реакции, вступая во взаимодействие с каким-либо промежуточным веществом, тем самым удаляя его из реакционной смеси. Это затрудняет протекание всей последовательности стадий в сложной реакции.
[1]
Дата добавления: 2021-02-19; просмотров: 712;











