КАРБАМИД. Эксперимент с ним
Гидролиз карбамида. При нагревании с растворами кислот или щелочей карбамид подвергается гидролизу. При этом образуются аммиак и углекислый газ:
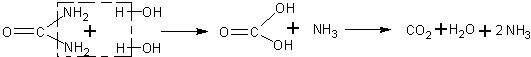
а) В колбу с 30 мл воды помещают 5 г карбамида и приливают половинный объем концентрированного раствора гидроксида натрия. Смесь нагревают, а выделяющийся аммиак обнаруживают при помощи палочки, смоченной концентрированной соляной кислотой.
б) Растворяют 0,5 г карбамида в 2—3 мл воды (в пробирке), добавляют двойной объем прозрачной баритовой воды и смесь кипятят. Влажной лакмусовой бумажкой и по запаху обнаруживают выделяющийся аммиак. Наблюдают образование осадка карбоната бария в результате взаимодействия угольной кислоты со щелочью.
Взаимодействие карбамида с азотной кислотой. Несмотря на наличие аминогруппы в молекуле, амиды кислот, как правило, не проявляют основных свойств. В этом сказывается влияние карбонила на аминогруппу. В связи с тем что в молекуле карбамида содержатся две аминогруппы, он проявляет свойства очень слабого основания и по одной из аминогрупп образует соли с некоторыми кислотами, например с азотной:
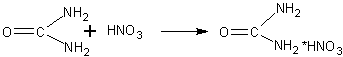
В демонстрационную пробирку помещают 20 мл воды и 3—4 г карбамида. К раствору приливают вдвое меньший объем концентрированной азотной кислоты. Смесь взбалтывают и охлаждают холодной водой из-под крана. Выпадает осадок соли азотной кис-
лоты. Опыт можно проводить аналогично предыдущему, но с меньшими количествами реактивов (берут 1-2 мл раствора карбамида).
Взаимодействие карбамида с щавелевой кислотой. Наглядной является реакция карбамида с щавелевой кислотой, Поскольку щавелевая кислота двухосновная, а в карбамиде основные свойства проявляет одна аминогруппа, то кислота реагирует сразу с двумя молекулами карбамида:
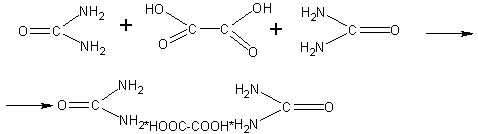
Готовят насыщенные на холоду небольшие количества растворов карбамида и щавелевой кислоты. Сливают в пробирке или колбе равные объемы растворов. Вскоре образуется кристаллический осадок.
Образование биурета. Характерной реакцией карбамида является превращение его при нагревании в биурет:
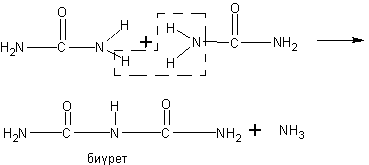
Нагревают в пробирке несколько кристалликов карбамида. Сначала он плавится, затем начинает разлагаться с выделением аммиака, который может быть обнаружен по запаху, при помощи стеклянной палочки, смоченной концентрированным раствором соляной кислоты, или другими способами. В пробирке образуется твердое белое вещество — биурет. Когда пробирка остынет, растворяют биурет в небольшом количестве воды при слабом нагревании. Затем добавляют немного раствора гидроксида натрия и 1-2 капли раствора сульфата меди. Образуется характерное для биурета (и
подобной группировки атомов в белках) красно-фиолетовое окрашивание.
Дата добавления: 2018-11-26; просмотров: 2849;











