Состав и характеристика атомного ядра
Ядра атомов состоят из двух видов элементарных частиц – протонов и нейтронов. Эти частицы носят название нуклонов.
Протон (р) – ядро атома водорода. Он обладает зарядом +e и массой
mp = 1,672×10-27кг (энергия покоя Е0р = 938,2 МэВ).
Нейтрон (n) – не обладающая электрическим зарядом частица с массой
mn = 1,675×10-27кг (энергия покоя Е0п = 939,5 МэВ).
Количество протонов z, входящих в состав ядра, определяет его заряд и называется зарядовым числом ядра.
Число нуклонов А в ядре называется массовым числом ядра. При превращениях ядер зарядовое и массовое числа сохраняются.
Для обозначения ядер применяют символ 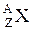 , где под X подразумевается химический символ элемента. Вверху ставится массовое число, внизу – атомный номер (зарядовое число).
, где под X подразумевается химический символ элемента. Вверху ставится массовое число, внизу – атомный номер (зарядовое число).
Масса ядра mя всегда меньше суммы масс входящих в него частиц. Это обусловлено тем, что при объединении в ядро выделяется энергия связи нуклонов друг с другом. Энергия связи Есв равна той работе, которую нужно совершить, чтобы разделить образующие ядро нуклоны и удалить их друг от друга на такие расстояния, при которых они практически не взаимодействуют друг с другом. Согласно закону взаимосвязи массы и энергии, энергия связи нуклонов в ядре равна:
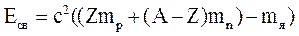 . (38)
. (38)
Радиоактивность
Радиоактивностью называется самопроизвольное превращение одних атомных ядер в другие, сопровождаемое испусканием элементарных частиц. К числу радиоактивных процессов относятся: 1) a-распад, 2) b-распад, 3) g-излучение ядер, 4) спонтанное деление тяжелых ядер, 5) протонная радиоактивность.
Закон радиоактивного превращения выражается формулой
N=N0e-lt , (39)
где N0 – количество ядер в начальный момент времени, N – количество нераспавшихся ядер в момент времени t, l – характерная для радиоактивного вещества константа, называемаяпостоянной распада.
Время, за которое распадается половина первоначального количества ядер, называется периодом полураспада Т1/2. Из (39) следует, что
T1/2 = (ln2)/l . (40)
Активностью радиоактивного препарата А называется число распадов, происходящих в препарате за единицу времени:
A = dNрасп/dt = lN . (41)
Альфа-распад
Альфа лучи представляют собой поток ядер гелия 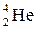 . Распад протекает по схеме
. Распад протекает по схеме
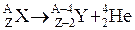 . (42)
. (42)
Из схемы распада видно, что атомный номер дочернего ядра Y на две единицы, а массовое число на четыре единицы меньше, чем у исходного (материнского) ядра Х.
Бета-распад
Наиболее распространенный вид b-распада – электронный распад – протекает по схеме
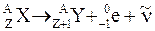 . (43)
. (43)
Из схемы видно, что дочернее ядро имеет атомный номер, на единицу больший, чем у материнского ядра, массовые числа обоих ядер одинаковы. Наряду с электроном испускается также антинейтрино 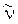 .
.
Ядерные реакции
Ядерной реакцией называется процесс сильного взаимодействия атомного ядра с элементарной частицей или с другим ядром, приводящий к преобразованию ядра (или ядер). Взаимодействие реагирующих частиц возникает при их сближении до расстояний порядка 10-15м благодаря действию ядерных сил.
Наиболее распространенным видом ядерной реакции является взаимодействие легкой частицы а с ядром X, в результате которого образуется легкая частица b и ядро Y:
Х + а ® Y + b .
Уравнение таких реакций принято записывать сокращенно в виде
Х(а,b)Y . (44)
В качестве легких частиц а и b могут фигурировать нейтрон (n), протон (р), дейтрон (d), a-частица (a) и g-фотон (g).
Ядерные реакции могут сопровождаться как выделением, так и поглощением энергии. Количество выделяющейся энергии Q называется энергией реакции.
Она определяется разностью масс исходных и конечных ядер (частиц):
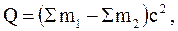 (45)
(45)
где å m1 – сумма масс ядер, вступающих в реакцию,
å m2 – сумма масс ядер, получившихся в результате реакции.
Если сумма масс образующихся ядер превосходит сумму масс исходных ядер, реакция идет с поглощением энергии и энергия реакции будет отрицательной (Q<0).
Дата добавления: 2016-10-26; просмотров: 1974;











