Семиполярная (или донорно-акцепторная) связь
В ряде органических соединений встречаются связи, совмещающие в себе свойства ковалентных и ионных. Типичным примером подобного рода является одна из связей N–O в нитрогруппе. Действительно, если мы изобразим связи в нитроорганическом соединении R–NO2 с помо- щью пар валентных электронов с соблюдением требований правила ок- тета, то приходим к следующей структуре:
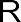
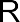
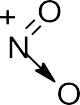

Эта структура показывает, что связи атома азота с двумя атомами кислорода неравноценны. Если одна из них является типичной двойной ковалентной связью, то во второй, помимо пары валентных электронов, образующих ковалентную связь, имеют место разноименные заряды на атомах азота и кислорода. Таким образом, связь N–O в нитрогруппе яв- ляется, с одной стороны, ковалентной, а с другой – ионной. Такие связи и называют семиполярными (по-русски – полуполярными), или донорно- акцепторными.
Водородная связь
Водородные связи могут образовываться между атомом водорода, связанным с атомом электроотрицательного элемента, и электроотрица- тельным элементом, имеющим свободную пару электронов (О, F, N). Водородная связь обусловлена электростатическим притяжением, кото- рому способствуют малые размеры атома водорода, и отчасти донорно- акцепторным взаимодействием. Обозначается водородная связь несколькими точками:
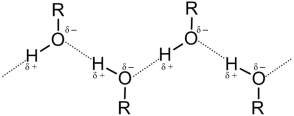
Водородная связь может быть межмолекулярной и внутримолеку- лярной.
Водородная связь гораздо более слабая, чем ионная или ковалент- ная, но более сильная, чем межмолекулярное взаимодействие. Водород- ные связи обусловливают некоторые физические свойства веществ (на- пример, высокие температуры кипения). Особенно распространены во- дородные связи в молекулах белков, нуклеиновых кислот и других био- логически важных соединений, обеспечивая им определенную про- странственную структуру (организацию).
Дата добавления: 2021-01-26; просмотров: 689;











