Пара-аминосалициловая кислота (ПАСК)
Обладает противотуберкулезным действием. В медицинской практике обычно используется в виде натриевой соли парааминосалицилата натрия.
Структурный изомер парааминосалициловой кислоты - метааминосалициловая кислота – высокотоксична и в качестве лекарственных препаратов не используется.
Отдельные представители карбоновых кислот
НСООН – при попадании на кожу вызывает ожог – в медицинской практике используется наружно, в виде спиртовых растворов при ревматических болях.
СН3СООК – ацетат калия применяется для лечения отеков.
(CH3COO)2Pb·3H2O – тригидрат ацетата свинца; CH3COOPbOH – основный ацетат свинца. Эти препараты применяются наружно в качестве вяжущих средств при воспалительных процессах кожи и слизистых оболочек.
Изовалериановая кислота – содержится в корнях валерианы, входит в состав валидола.
СаС2О4 – оксалат кальция – в организме участвует в образовании камней в почках и мочевом пузыре.
Дикарбоновые кислоты:
Янтарная и глутаровая лежат в основе биологически важных
a-аминокислот: аспарагиновой и глутаминовой соответственно.
Молочная кислота образуется в результате молочнокислого брожения углеводов, например глюкозы:
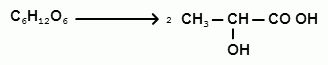
[глюкоза = 2 молочной к-ты]
Молочная кислота содержится в кисломолочных продуктах, квашеной капусте, соленых овощах. Молочная кислота обнаруживается в желудочном содержимом при пониженной его кислотности. В норме в желудочном соке молочной кислоты быть не должно.
Соль молочной кислоты – лактат кальция – в медицинской практике используется при аллергических, кожных заболеваниях, воспалениях, переломах, кровотечениях, а также в качестве противоядия при отравлении щавелевой кислотой и другими веществами.
Яблочная кислота содержится в яблоках, рябине, фруктовых соках; в организме участвует в обменных процессах. Лимонная кислота – содержится в цитрусовых, винограде, крыжовнике. Её соль – цитрат натрия – используется в медицине как консервант крови.
Контрольные вопросы
1. Карбоновые кислоты, их классификация, номенклатура, изомерия.
2. Электронное строение карбоксилат-аниона.
3. Химические свойства карбоновых кислот. Реакции диссоциации, галогенирования, декарбоксилирования, этерификации.
4. Медико-биологическое значение карбоксильных соединений.
5. Гидроксикислоты и кетонокислоты, их строение, изомерия, номенклатура.
6. Химические свойства гидрокси- и кетонокислот. Реакции диссоциации, декарбоксилирования, этерификации.
7. Реакции окисления молочной кислоты, β-гидроксимасляной кислоты, яблочной кислоты. Пути превращения
β-гидроксимасляной кислоты в организме. Реакция окислительного декарбоксилирования пировиноградной кислоты.
8. Медико-биологическое значение гидрокси- и кетонокислот и их производных. Салициловая кислота и фармпрепараты на ее основе, их получение и применение в медицине.
Типовые задания
Задание 1. Опишите влияние заместителей на кислотные свойства карбоновых кислот. Расположите соединения в ряд по уменьшению кислотности: уксусная кислота, дихлоруксусная кислота, трихлоруксусная кислота.
Решение. Электронодонорные заместители снижают кислотность, электроноакцепторные заместители – усиливают. Галогены относят к электроноакцепторным заместителям, причем увеличение числа атомов галогена усиливает кислотность. Таким образом, соединения по уменьшению кислотности располагаются в ряд: трихлоруксусная
Дата добавления: 2016-10-18; просмотров: 2703;











