ОСНОВНЫЕ ПОНЯТИЯ И ЗАКОНЫ ХИМИИ
1.ПРИВЕДЕНИЕ ОБЪЕМА ГАЗА К НОРМАЛЬНЫМ УСЛОВИЯМ (н.у.)
Какой объем при н.у. займут 0,4 л газа, находящегося при 500С и давлении 95,4 кПа?
РЕШЕНИЕ: для приведения объема газа к н.у. воспользуемся уравнением, объединяющим законы Бойля-Мариотта и Гей-Люссака:
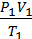 =
= 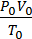 ,
,
где P0V0/ T0 – нормальные условия.
Из уравнения следует, что V0 = P1V1T0/ P0T1. Переведем размерность параметров в систему Си:
V1= 0,4л =4  10-4м3; Т1= 500С = 323К; Р1= 95,4кПа = 9,54
10-4м3; Т1= 500С = 323К; Р1= 95,4кПа = 9,54  104Па.
104Па.
Подставим значения величин в уравнение:
V0= 9,54  104Па
104Па  4
4  10-4м3
10-4м3  273К / 1,013
273К / 1,013  105Па
105Па  323К = 3,18
323К = 3,18  10-4 м3.
10-4 м3.
2.ВЫЧИСЛЕНИЕ МОЛЯРНОЙ МАССЫ ГАЗА ПО ЗАДАННОМУ ОБЪЕМУ
Вычислить молярную массу газа, если при 130С (286К) его масса составляет 1,01 г, находится под давлением 1,04  105Па и занимает объем 3,27
105Па и занимает объем 3,27  10-4 м3 .
10-4 м3 .
РЕШЕНИЕ: расчет проведем по уравнению состояния идеального газа.
М = 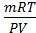 ,
,
М = 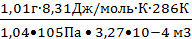 = 70,7 г/моль.
= 70,7 г/моль.
2. ОПРЕДЕЛЕНИЕ ПАРЦИАЛЬНОГО ДАВЛЕНИЯ ГАЗА В СМЕСИ
Смешивают (V0) 3л СО2 с 4л О2 и 6л N2. До смешения давления газов составляли соответственно (P0) 96, 108 и 90,6 кПа. Общий объем смеси (V1) 10л. Определить парциальное давление газов (P1) и общее давление смеси.
РЕШЕНИЕ: Так как температура постоянна, то P1V1 =P0V0. Рассчитаем парциальные давления газов в смеси:
Р1(СО2) = P0V0/V1= 96 кПа  3л/ 10л = 28,8 кПа .
3л/ 10л = 28,8 кПа .
Р1(О2) = P0V0/V1= 108 кПа  4л/ 10л = 43,2 кПа .
4л/ 10л = 43,2 кПа .
Р1(N2) = P0V0/V1= 90,6 кПа  6л/ 10л = 54,4кПа .
6л/ 10л = 54,4кПа .
Общее давление газовой смеси равно сумме парциальных давлений ее компонентов Робщ= Р1(СО2) + Р1(О2) + Р1(N2) =28,8 + 43,2 + 54,4 = 126,4 кПа.
4. РАСЧЕТ АБСОЛЮТНОЙ МАССЫ МОЛЕКУЛЫ ВЕЩЕСТВА
Рассчитать абсолютную массу молекулы газа (mм), если масса 1,5л газа при н.у. составляет 1,785 г.
РЕШЕНИЕ. Известно, что для газов количество вещества определяется как
n = 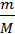 =
= 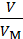
М = mVM / V = 1,785г ∙ 22,4л/моль / 1,5л = 26,7 г/моль.
Масса молекулы рассчитывается как частное от деления молярной массы вещества на число Авогадро mм = М / Na= 26,7 г/моль / 6,02  1023 моль-1 = 4,44
1023 моль-1 = 4,44  10-23г.
10-23г.
5.ОПРЕДЕЛЕНИЕ АТОМНОЙ МАССЫ МЕТАЛЛА ПО ЕГО ЭКВИВАЛЕНТНОЙ МАССЕ.
Дата добавления: 2021-01-26; просмотров: 562;











