Свойства триоксида урана различного происхождения
| Свойства | Термическая диссоциация | |||
| уранилнитрата | полиуранатов аммония | пероксида урана | аммоний- уранилтрикарбоната | |
| Плотность утряски, г/см3 | 3,6-4,0 | 0,65-1,7 | 0,7-1,6 | 1,28-1,76 |
| Средний размер частиц, мкм | 0,99 | 0,44-0,08 | 0,05 | 0,43 |
| Средний размер агрегатов, мкм | 80-110 | – | ||
| Удельная поверхность, м2/г | 0,73 | 1,6-9,0 | 1,4 | 2,30 |
| Состояние | Кристаллическое | Аморфное | Аморфное | Аморфное |
Например, наиболее крупные кристаллы триоксида получаютя при разложении уранилнитрата, наиболее мелкие – при термической диссоциации пероксида урана. В то же время размер агрегатов триоксида урана, получающегося из уранилнитрата, меньше, чем полученного из пероксида урана.
От физических свойств триокида урана зависят как скорость и эффективность последующего процесса его восстановления, так и в значительной мере физические свойства образующегося при этом диоксида. Триоксид, полученный из полиуранатов аммония, восстанавливается водородом быстрее, чем изготовленный из уранилнитрата. Это вызвано, по-видимому, различием в условиях фазового контакта твердого вещества и газа.
Влияние состава исходной соли, а также температуры восстановления триоксида урана водородом на физические свойства диоксида урана характеризуется данными, приведенными в табл. 1.2.4.
Таблица 1.2.4
Влияние состава исходной соли и температуры восстановления на свойства диоксида урана
| Соль, из которой получен триоксид урана | Размер частиц триоксида, мкм | Свойства диоксида | |||
| восстановление при 700 °С | восстановление при 850 °С | ||||
| диаметр частиц, мкм | удельная поверх-ность, м2/г | диаметр частиц, мкм | удельная поверх-ность, м2/г | ||
| Диуранат аммония Уранилнитрат Аммонийуранилтрикарбонат | 0,08 0,59 0,43 | 0,032 0,330 0,320 | 17,40 1,82 1,90 | 0,086 1,52 0,39 | 6,40 0,39 1,60 |
В общем случае, чем более крупнокристаллической является триоксид урана, тем больше размер кристаллов получаемого из него диоксида; повышение температуры восстановления обычно приводит к увеличению размера частиц и к уменьшению удельной поверхности порошка.
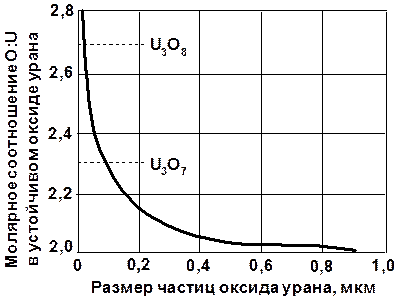 Рис. 1.2.1 Влияние размера частиц на соотношение кислорода и урана в устойчивых оксидах урана (при 25 °С, в воздушной среде)
Рис. 1.2.1 Влияние размера частиц на соотношение кислорода и урана в устойчивых оксидах урана (при 25 °С, в воздушной среде)
|
Скорость гидрофторирования диоксида урана фтороводородом зависит прежде всего от его реакционной способности, от размера кристаллов и агрегатов. Диоксид урана, полученный из диураната аммония, состоит из больших агрегатов сравнительно мелких частиц и обладает высокой удельной поверхностью. В связи с этим скорость гидрофторирования подобных образцов довольно значительна даже при низкой температуре; повышение температуры приводит к закупориванию пор агрегатов в результате спекания образовавшегося тетрафторида урана.
Диоксид урана, полученный из уранилнитрата, менее склонен к образованию агрегатов, но размер кристаллов его довольно велик; поэтому реакционная способность диоксида урана, приготовленного из уранилнитрата, ниже.
Примерно такие же закономерности характерны и для процесса окисления диоксида урана кислородом воздуха. Диоксид с размером частиц порядка сотых долей микрона и ниже пирофорен уже при 0 °С; интенсивное окисление диоксида урана с размером частиц 0,4 мкм протекает при 150 °С. При обычной температуре окисление диоксида, как правило, не приводит к образованию стехиометрических соединений закиси-окиси или триокида урана; состав полученных продуктов сильно меняется, причем степень этого изменения и степень окисления диоксида урана всецело определяются размером частиц (рис. 1.2.1).
Для любой другой температуры эти кривые сдвигаются в область более высоких соотношений кислорода и урана.
Дата добавления: 2019-05-21; просмотров: 792;











