Контрольные задания
4.1.Определите число молей и концентрацию молекул газа, объем которого V = 2,4·10-4 м3, температура t = 270 С и давление Р=0,5·105Па.
4.2. В сосуде находится смесь m1 = 0,02 кг углекислого газа и m2 = 0,015 кг кислорода. Определите плотность этой смеси при температуре t = 270 С и давлении Р = 1,5·105 Па.
4.3.В закрытом сосуде объемом V=0,5 м3 находится m1=0,45 кг воды и m2 = 0,8 кг азота. Определите давление в сосуде при температуре t = 5000 С, полагая, что при этой температуре вся вода превращается в пар.
4.4. В закрытом сосуде находится m1=0,015 кг азота и m2=0,018кг кислорода при температуре t=270 С и давлении Р=5·105 Па. Определите объем и молярную массу смеси газов.
4.5.При каком давлении следует наполнить воздухом баллон объемом V1 = 2·10-3 м3, чтобы при соединении его с баллоном объемом V2 = 4·10-3 м3, содержащим воздух при давлении Р2 = 0,1 МПа, установилось общее давление Р = 0,25 МПа ?
4.6. В баллоне объемом V = 6·10-2 м3 находится кислород при температуре t = 270С. Определите массу израсходованного кислорода, если давление в баллоне уменьшилось на ΔP = 100 кПа. Процесс считать изотермическим.
4.7.В баллоне объемом V = 0,01 м3 находится гелий под давлением Р = 106 Па и при температуре t = 270С. Определите давление в баллоне после того, когда из баллона выпустили m = 0,01 кг гелия, а температура понизилась до 170С.
4.8. В сосуде находится смесь m1=0,06 кг углекислого газа и m2=0,010 кг азота. Определите плотность этой смеси при t=37о С и давлении P=1,5·105 Па.
4.9.В сосуде емкостью V = 0,02 м3 содержится смесь водорода и азота при температуре t = 270С и давлении Р = 1,2·106 Па. Масса смеси m = 0,145 кг. Определите массу водорода и азота в сосуде.
4.10. Определите плотность углекислого газа, находящегося в сосуде под давлением Р = 2·105 Па и имеющего температуру t = 70C.
Основы равновесной термодинамики
Основные формулы
· Молярные теплоёмкости при постоянном объёме ( 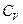 ) и постоянном давлении (
) и постоянном давлении ( 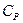 ):
):
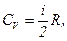
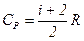 ,
,
где 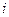 – число степеней свободы,
– число степеней свободы, 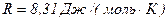 - универсальная газовая постоянная.
- универсальная газовая постоянная.
· Связь между удельной ( 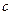 ) и молярной (
) и молярной ( 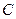 ) теплоёмкостями:
) теплоёмкостями:
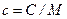 ,
,
где 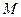 – молярная масса.
– молярная масса.
· Внутренняя энергия идеального газа:
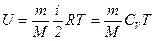 ,
,
где 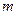 - масса газа,
- масса газа, 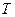 - абсолютная температура.
- абсолютная температура.
· Изменение внутренней энергии идеального газа:
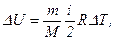
· Работа расширения газа:
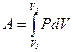 - в общем случае,
- в общем случае,
где 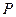 - давление газа,
- давление газа, 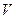 - объём газа.
- объём газа.
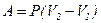 - при изобарном процессе.
- при изобарном процессе.
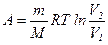 - при изотермическом процессе.
- при изотермическом процессе.
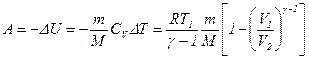 - при адиабатном процессе,
- при адиабатном процессе,
где 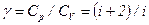 .
.
· Первое начало термодинамики:
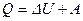 ,
,
где 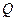 – количество теплоты, сообщённое системе;
– количество теплоты, сообщённое системе; 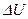 - изменение внутренней энергии системы;
- изменение внутренней энергии системы; 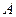 – работа, совершённая системой против внешних сил.
– работа, совершённая системой против внешних сил.
· Уравнение Пуассона для адиабатного процесса:
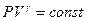 .
.
· Уравнение адиабаты идеального газа в переменных 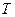 и
и 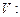
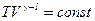 .
.
· Коэффициент полезного действия цикла Карно:
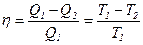 ,
,
где 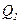 - количество теплоты, полученное от нагревателя;
- количество теплоты, полученное от нагревателя; 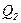 - количество теплоты, переданное холодильнику;
- количество теплоты, переданное холодильнику; 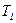 - температура нагревателя;
- температура нагревателя; 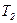 - температура холодильника.
- температура холодильника.
Дата добавления: 2020-10-25; просмотров: 550;











