Вплив корозійного середовища на швидкість корозії. Електрохімічний захист.
Одним з основних факторів визначаючих характер і швидкість корозії металів і сплавів є склад корозійного середовища. Тому зменшення агресивності середовища шляхом її обробки є ефективним методом боротьби з корозією.
1. Обробка середовища при газовій корозії.
Для сталевих деталей захисною атмосферою є така, що не викликає окислювання, зневуглецювання і навуглесення Розрахунок складу захисної атмосфери для даного металу роблять з використанням констант рівноваги, що встановлюються в системі метал - газ, так при взаємодії заліза з оксидом вуглецю (IV) установлюється рівновага:
Fe (т) + CO2 (г) « Fe (т) + CO (г)
Константа цієї реакції при t° = 900°
K = PCO / PCO2 = 2,2
при концентрації PCO / PCO2 > 2,2 залізо не окисляється.
При PCO / PCO2 < 2,2 реакція зміщається вправо - відбувається окислювання заліза.
При взаємодії заліза з водою встановлюється рівновага
Fe (т) + H2O (г) « Fe (т) + H2 (г)
Константа при t = 850°С
K = PH2 / PH2O = 2
при PH2 / PH2O > 2 реакція зміщається вліво окислювання заліза не відбувається, а при PH2 / PH2O < 2 реакція зміщається вправо - залізо окисляється.
В атмосфері водню - рівновага стали:
Fe3C (т) +2H2 (г) « 3Fe (т) + CH4 (г)
При t = 800°C; PCH4 / P2H2 = 20
при PCH4 / P2H2 > 20 реакція зміщається вліво - відбувається навуглесення.
При PCH4 / P2H2 < 20 реакція зміщається вправо - відбувається зневуглецювання.
Для створення захисних атмосфер у промисловості застосовують суміші наступних типів:
1. Водень - водяна пара – азот.
2. Водень - водяна пара - оксид вуглецю (II) - азот.
3. Оксид вуглецю (II) - оксид вуглецю (IV) - водень - водяна пара - азот.
Склад атмосфери може сприяти полегшенню утворення на металі захисних плівок.
2. Обробка розчинів електроліту.
Зводиться до зменшення змісту деполяризатора і введенню в неї чи сповільнювачів інгібіторів корозії.
У кислих розчинах (електролітах) відбувається корозія з водневою деполяризацією - зменшенняїї досягається видаленням кисню з електроліту. Наприклад нейтралізацію шахтних вод роблять уведенням негашеного вапна чи їдкого натру.
2H+ + Ca = Ca2+ + H2O
H+ + OH- = H2O
Зменшення кисню у воді досягається хімічним, термічним і десорбційним, способами. При хімічному обескисеневміщенні у воду додають відновлювачі які вступають у взаємодію з розчиненим киснем і зв'язують його. Так відновлювачами є:
сульфат натрію: 2Na2SO4 + O2 = 2Na2SO4
гидразин: Na2H4 ∙ H2O + O2 = 2Na + 3H2O
Видалення кисню з води відбувається також при пропущенні її через шар свіжих залізних стружок при t = 85°С. При цьому залізо кородує з кисневою деполяризацією в результаті чого кисень зв'язується в оксид заліза Fe3O4.
3Fe + 2O2 = Fe3O4
Електрохімічний захист.
Швидкість електрохімічної корозії можна значно зменшити, якщо металеву конструкцію піддати поляризації. Цей метод одержав назву електрохімічного захисту. У залежності від виду поляризації розрізняють катодний і анодний захист.
Катодний захист - найбільш розповсюджений вид електрохімічного захисту. Її використовують для боротьби з корозією таких металів, як сталь, мідь, латунь, алюміній, в умовах несильно агресивних середовищ.
Катодну поляризацію можна здійснювати шляхом приєднання конструкції, що захищається, до негативного полюса зовнішнього джерела струму чи до металу, що має більш електронегативний електродний потенціал. В останньому випадку немає потреби в зовнішнім джерелі струму, тому що утвориться гальванічний елемент із тим же напрямком струму, тобто деталь, що захищається, стає катодом, а більш електронегативний метал, називаний протектором - анодом.
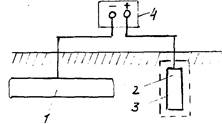
Рис.1 Схема катодного захисту зовнішнім струмом.
I - казан ; 2 - джерело струму; 3 – анод
Схема катодного захисту зовнішнім струмом представлена на мал.1 Негативний полюс зовнішнього джерела струму 4 приєднаний до металевої конструкції, що захищається, 1, а позитивний полюс - до допоміжного електрода 2, що працює як анод. У процесі захисту анод активно руйнується і підлягає періодичному відновленню.
Як матеріал анода застосовують чавун, сталь, вугілля, графіт, металевий брухт (старі труби, рейки й ін.).Для збільшення електропровідності аноду, його як правило поміщають у засипання 3 - товстий шар коксу, у який додають 3-4 ч (по масі) гіпсу і 1 ч повареної солі. Засипання має високу електропровідність, завдяки чому знижується перехідний опір ґрунт - анод.
Для захисту споруджень у воді аноди встановлюють на дні рік, озер, морів. У цьому випадку засипання не потрібно,
Напругу, що накладається для захисту, вибирають з необхідності забезпечення захисної щільності струму визначеної величини.
Перевищення оптимальної величини захисної щільності струму небажано, тому що може привести до деякого зниження катодного захисту (ефект "перезахисту"). Ефективність катодного захисту характеризується величиною захисного ефекту
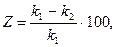
де k1 - показник швидкості корозії металу без катодного захисту;
k2 - те ж, при катодному захисті.
і величиною коефіцієнта захисної дії
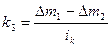
де Δm1 - зменшення маси металу в корозійному середовищі без катодного захисту ;
Δm2 - те ж, при катодному захисті;
ik – катодна щільність струму.
Катодний захист зовнішнім струмом широко застосовують як додатковий засіб захисту до ізоляційного покриття.
Застосовують катодний захист і до конструкцій, що мають значні корозійні ушкодження, що дозволяє призупинити подальше поширення корозії.
Катодний захист зовнішнім струмом недоцільний в умовах атмосферної корозії, у пароподібному середовищі, в органічних розчинниках, тому що в цьому випадку корозійне середовище не має достатню електропровідність. В таких випадках(морській річковій воді, ґрунти та інших нейтральних середовищах використовують протекторний захист.
Протекторний захист
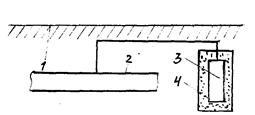
Рис. 2 Схема протекторного захисту трубопроводу.
Схема протекторного захисту трубопроводу показана на мал. 2. До конструкції, що захищається, 2 приєднують більш електронегативний метал - протектор 3 який, розчиняючи в навколишнім середовищі, посилає електрони конструкції 2 Після повного розчинення протектора його необхідно відновляти.
Як протектор найчастіше використовують магній, цинк і їхні сплави. Алюміній застосовують рідше, тому що він швидко покривається дуже щільною оксидною плівкою, що пасивує його й обмежує срумовіддачу.
Як і у випадку катодного захисту зовнішнім струмом ефективність протекторного захисту зростає при її спільному використанні з захисними покриттями. Так, нанесення бітумного покриття на трубопроводи значно поліпшує розподіл захисного струму, зменшує число анодів і збільшує довжину ділянки трубопроводу, що захищається за допомогою одного протектора. Якщо одним магнієвим анодом можна забезпечити захист непокритого трубопроводу довжиною усього 30 м, то захист покритого бітумом трубопроводу діє на довжину до 8 км.
Анодний захист зовнішнім струмом, при якій конструкцію, що захищається, приєднують до позитивного полюса зовнішнього джерела струму, а допоміжний електрод (катод) - до негативного.
Метод анодного захисту має відносно обмежене застосування, тому що анодний захист потенційно небезпечний: у випадку перерви подачі струму можливий активування металу і його інтенсивне анодне розчинення. Тому анодний захист вимагає наявності ретельної системи контролю.
Метод анодного захисту використовують для металів і сплавів, які легко пассивирують при анодній поляризації. У хімічній промисловості його успішно застосовують для зниження швидкості корозії низьковугдеродної сталі в сірчаній кислоті й у розчинах, що містять аміак і нітрат амонію.
Література
1.М.А.Шлугер. Корозія та захист металів М «Металургія»,1981 г. 215 с
2.И.В.Семенова.Коррозія та захист від корозії. М. «Фізметліт» ,2006г,371 с.
Лекція №4
Дата добавления: 2016-07-27; просмотров: 2129;











