Кислотные и основные свойства
Спирты являются слабыми ОН – кислотами. Эти свойства проявляются при их взаимодействии с щелочными и щелочноземельными металлами, а также с амидами и гидридами этих же металлов. При взаимодействии с реактивами Гриньяра образуют магнийгалогеналкоголяты:
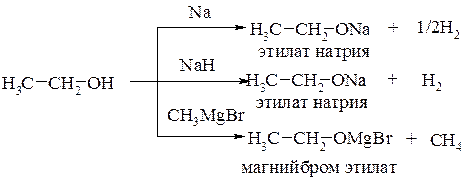
Этанол является более сильной кислотой, чем аммиак, но более слабой, чем вода.
Вещества, образующиеся при замещении атома водорода, называются алкоголятами. Эти соединения, как правило, нестойкие и в присутствии следов влаги гидролизуются с образованием спирта и соответствующего гидроксида металла:

Кислотные свойства спиртов в газовой фазе убывают от третичных к первичным:
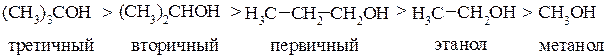
В жидкой фазе, а также в водных растворах наблюдается прямо противоположная зависимость.
Говоря о спиртах, как об основаниях, следует исходить из системы определений по Брёнстеду-Лоури и Льису: наличие неподеленной пары электронов у атома кислорода свидетельствует о нуклеофильности, как частном случае проявления основных свойств.
Спирты могут образовывать катионы оксония только с сильными Н – кислотами, или жесткими кислотами по Пирсону типа BF3, ZnCl2:
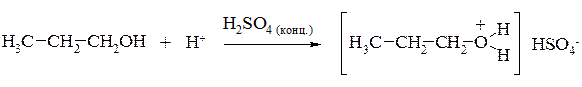
Дата добавления: 2020-10-01; просмотров: 665;











